Презентация на тему: «Металлы» химия 10 класс

МЕТАЛЛЫ Выполнила: Семёнова Дарья 10 – А Cu AI Ni Fe Mg Co Cr Na Zn

Что такое металлы ? Металлы – химические элементы, образующие в свободном состоянии простые вещества с металлической связью.
Роль металлов в развитии цивилизации В древности человеку были известны только 7металлов: Золото(Au), Серебро(Ag), Медь(Cu), Олово(Sn), Свинец(Pb), Железо(Fe) Ртуть(Hg).

Медь Установлено, что египтяне за несколько тысячелетий до нашей эры уже умели изготавливать изделия из меди. Иногда в очаг попадали небольшие самородки меди, которые размягчались в огне. Люди заметили, что раскаленный кусок меди меняет форму при ударе. Это свойство позволило выковывать из меди ножи, шилья и другие предметы. Затем люди научились выплавлять медь из руды. Расплавленную медь заливали в форму и получали медное изделие нужного вида.

Бронза Первыми людьми, из древнего мира которые выплавили бронзу, были египтяне. Они создали прочный по тем временам сплав – бронзу, смешав олово и медь. Это позволило усовершенствовать орудия труда и победить соседей, не обладавших бронзой.

Железо Первое железо люди выплавляли из метеоритов, оно было очень дорогим. Даже победителям Олимпийских игр наряду с золотыми медалями давали кусок железа. Железный клинок был обнаружен в гробнице Тутанхамона. Позднее люди научились выплавлять железо из руд, и оно стало массовым.
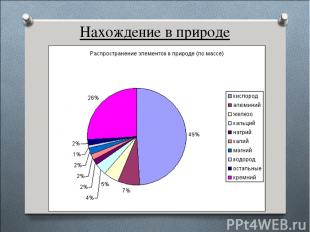
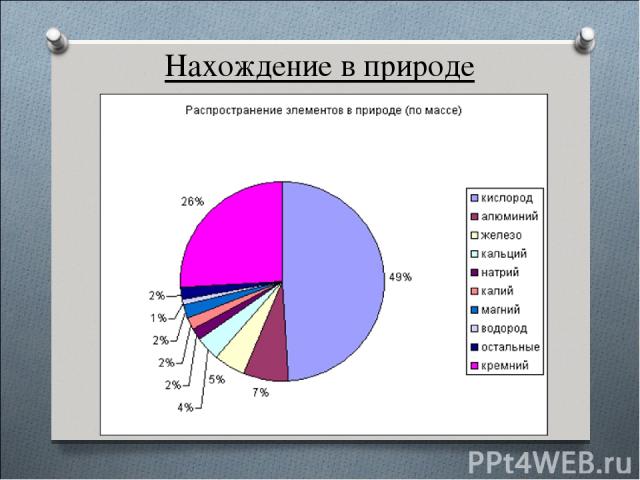
Нахождение в природе

Закономерность изменения свойств металлов в группе. Заряд ядра увеличивается, так как увеличивается порядковый номер. R увеличивается, так как увеличивается количество энергетических уровней. Число электронов на последнем уровне постоянно. Способность к отдаче электронов увеличивается. Восстановительные способности и металлические свойства увеличиваются.

Закономерность изменения свойств металлов в периоде. Заряд ядра увеличивается, так как увеличивается порядковый номер. R уменьшается, так как заряд ядра больше, способность притягивать электроны возрастает, за счет этого происходит стягивание электронных оболочек. Число электронов на внешнем уровне увеличивается, так как растёт номер группы. Восстановительные способности и неметаллические свойства уменьшаются.

Получение металлов Пирометаллургический способ -восстановление углеродом, оксидом углерода (II), водородом при высокой температуре. Алюминотермический способ – восстановление металлов с помощью алюминия. Гидрометаллургический способ – получение из руды более активным металлом или из растворов Электролиз – с помощью электрического тока из расплавов или растворов
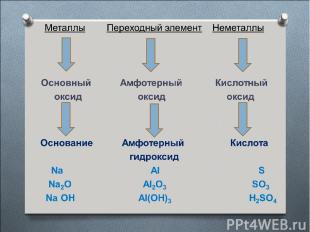

Все металлы- твердые вещества, кроме ртути. Самый мягкий – калий. Самый твердый – хром.

Физические свойства металлов. Модели кристаллических решёток металлов: а) кубическая гранецентрированная; б) кубическая объёмноцентрированная; в) гексагональная
Плотность Лёгкие (Li–самый легкий, K, Na, Mg) Тяжелые (осмий – самый тяжёлый Ir, Pb)

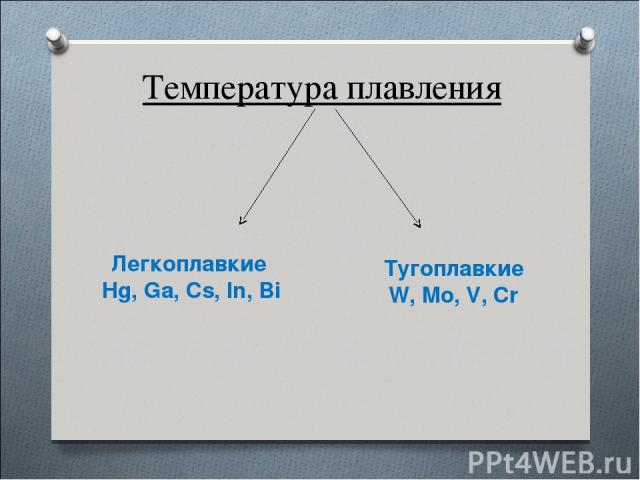
Температура плавления Легкоплавкие Hg, Ga, Cs, In, Bi Тугоплавкие W, Mo, V, Cr

Взаимодействие с простыми веществами - С элементами VII группы (при обычных условиях) 2Na + Cl2 = 2 Na Cl - С элементами VI группы (труднее) Mg + O2 = 2Mg O - C элементами V группы (в жестких условиях) 3Ca + 2P =Ca3P2

Взаимодействие со сложными веществами С растворами кислот (металлы, стоящие в ряду напряжений до «Н») Zn + H2SO4 = Zn S O4 + H2↑ C растворами солей металлов, стоящих в ряду напряжений правее Zn + Pb(NO3)2 = Zn(NO3)2 + Pb C водой (активные) 2Na + 2H2O =2Na OH + H2↑ Реакция идет в том случае, если образуется растворимое основание.