Презентация на тему: «Альдегиды» 10 класс

5klass.net

Контрольные вопросы: Сформулируйте определение фенолов. Опишите физические свойства фенола. Какова растворимость фенола в холодной и горячей воде? Как по строению отличаются фенолы от предельных спиртов? Что общего в химических свойствах предельных спиртов и фенолов? Чем отличаются химические свойства фенола от свойств предельных спиртов? Какие типы химических реакций характерны для фенола? Составьте уравнения реакций: а) замещения атома водорода в гидроксильной группе б) замещения атомов водорода в бензольном кольце в) присоединения Назовите полученные соединения. Какие качественные реакции на фенол вам известны? Назовите основные области применения фенола.

К. Шееле И.В. Дёберейнер, 1821 год Л.Воклен Ю. Либих, 1835 год А.Фуркруа «кислородный эфир» А.В. Гофман, 1868 год
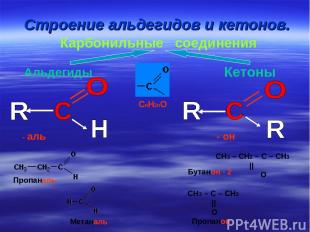
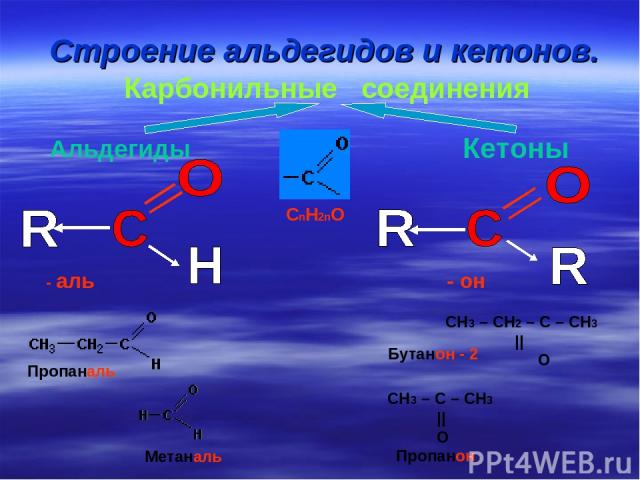
Строение альдегидов и кетонов. Карбонильные соединения Альдегиды Кетоны CnH2nO - аль - он СН3 – СН2 – С – СН3 || O СН3 – С – СН3 || O Пропаналь Метаналь Пропанон Бутанон - 2
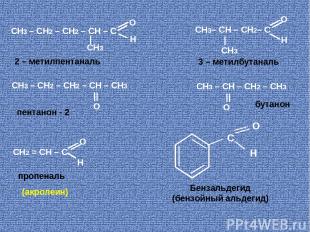
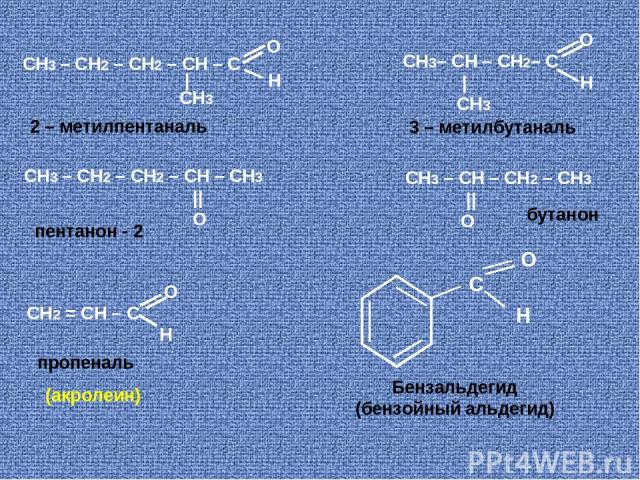
О СН3 – СН2 – СН2 – СН – С | Н CH3 СН3 – СН2 – СН2 – СН – CH3 || O О СН3– СН – СН2– С | Н CH3 О СН2 = СН – С Н СН3 – СН – СН2 – CH3 || O С O H Бензальдегид (бензойный альдегид) пропеналь пентанон - 2 бутанон 2 – метилпентаналь 3 – метилбутаналь (акролеин)

О СН3 – СН2 – СН2 – СН = СН – С Н O || СН3 – СН2 – С – СН – СН2 – СН3 | CH3 гексен - 2 - аль 4-метил гексанон - 3
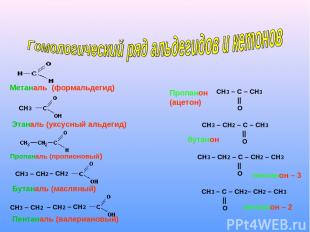
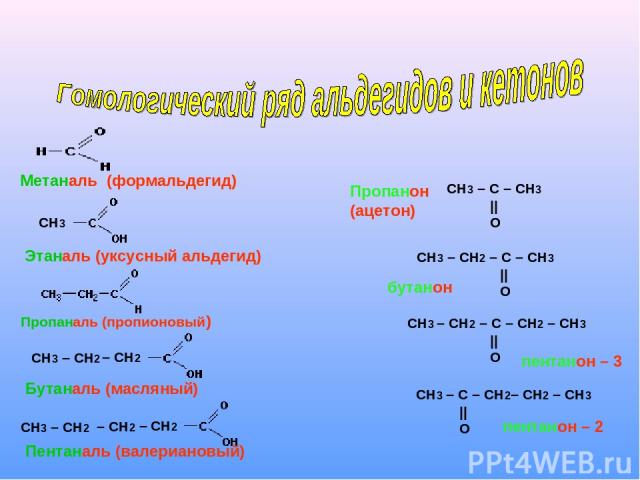
СН3 СН3 – СН2 – СН2 – СН2 СН3 – СН2 – СН2 Метаналь (формальдегид) Этаналь (уксусный альдегид) Пропаналь (пропионовый) Пентаналь (валериановый) Бутаналь (масляный) Пропанон (ацетон) СН3 – С – СН3 || O СН3 – СН2 – С – СН3 || O СН3 – СН2 – С – СН2 – СН3 || O СН3 – С – СН2– СН2 – СН3 || O бутанон пентанон – 3 пентанон – 2
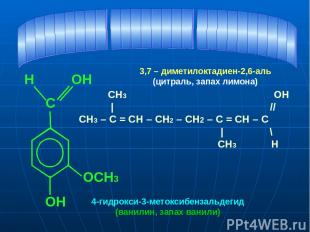
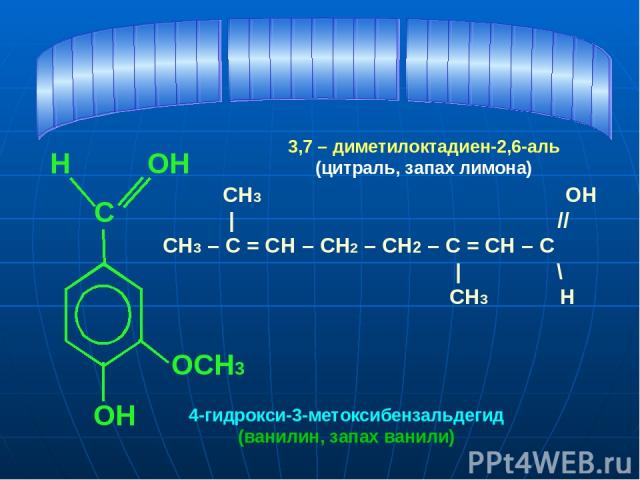
С ОСН3 ОН ОН Н CH3 ОН | // СН3 – С = СH – СН2 – СН2 – С = СН – С | \ СН3 Н 4-гидрокси-3-метоксибензальдегид (ванилин, запах ванили) 3,7 – диметилоктадиен-2,6-аль (цитраль, запах лимона)
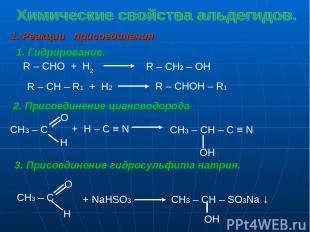
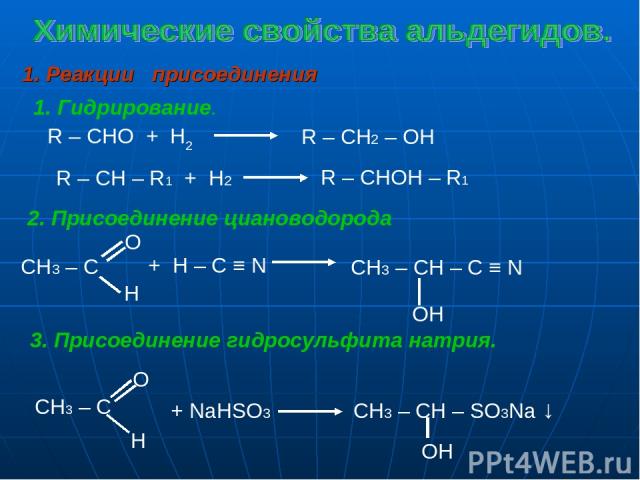
1. Реакции присоединения 1. Гидрирование. R – CHO + H2 R – CH2 – OH R – CH – R1 + H2 R – CHOH – R1 2. Присоединение циановодорода + H – C ≡ N CH3 – CH – C ≡ N ОH 3. Присоединение гидросульфита натрия. + NaHSO3 CH3 – CH – SO3Na ↓ OH CH3 – C O H CH3 – C O H
![– C OH 2. Реакции окисления. R – C O O H [О] R CH3 – C O H + Ag2O O H CH3 – C O – C OH 2. Реакции окисления. R – C O O H [О] R CH3 – C O H + Ag2O O H CH3 – C O](https://fs3.ppt4web.ru/images/132073/183328/310/img9.jpg)
– C OH 2. Реакции окисления. R – C O O H [О] R CH3 – C O H + Ag2O O H CH3 – C O OH CH3 – C CH3 – C + 2Cu(OH)2 O OH + Cu2O + 2H2O

Реакция c гидроксидом меди (II). Реакция серебряного зеркала Сu(OH)2, t Cu2O, - H2O Ag2O в аммиаке - Ag↓ Получение гидроксида меди (II) Сu + 2ОН = Сu(ОН)2↓ Признак реакции – изменение цвета осадка с голубого на кирпично-красный. Получение аммиачного раствора оксида серебра. Ag2O + 4NH3 + H2O = 2[Ag(NH3)2]OH Признак реакции – образование серебра на стенках колбы или выпадение чёрно-бурого осадка.

Юстус Либих. (1803 – 1873) Выдающийся немецкий химик. В 1824—52 профессор университета в Гисене. С 1830 — иностранный член-коррес-пондент Петер бургской академии наук. С 1852 - профессор университета в Мюнхене, с 1860— президент Баварской академии наук. Изучил процесс образования серебряного зеркала, впервые получил хлороформ (1831) и уксусный альдегид. Усовершенствовал методику определения в органических соедине-ниях углерода и водорода и, пользуясь этим методом, сохранившемся в основ-ном до настоящего времени, установил точный состав органических соединений.
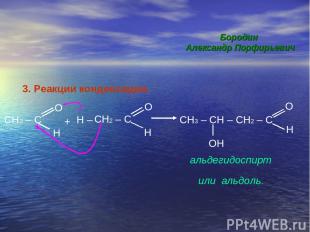
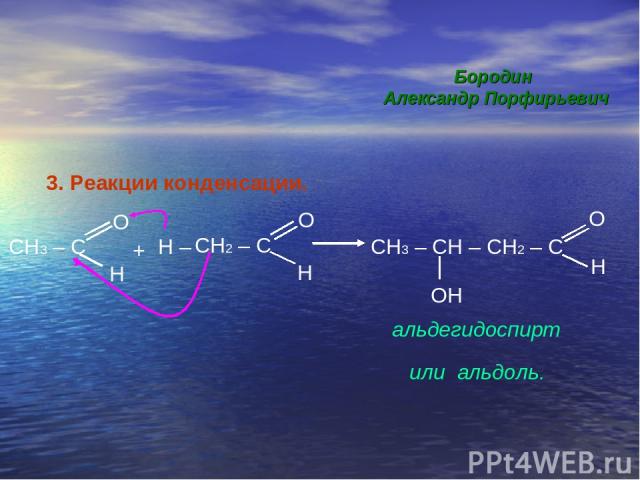
3. Реакции конденсации. CH3 – C O H + CH2 – C H – O H CH3 – CH – CH2 – C O H OH или альдоль. альдегидоспирт Бородин Александр Порфирьевич

Бородин Александр Порфирьевич 12.09.1883 – 27.02. 1887. Основные научные достижения 1852 — Вышла в свет монография "Солигаличские солено-минеральные воды". 1861 - Синтезировал первое фторорганическое сое-динение — фтористый бензоил. 1861 — Предложил способ получения алкилгалогенидов, действуя галогенами на соли жирных кислот. Реакция получила название реакции Бородина: 1872 — Одновременно с Вюрцем и независимо от него осуществил реакцию альдольной концентрации. 1876 — Создал прибор для определения азота в продуктах обмена человеческого организма и с его помощью разработал метод определения этого элемента, которым пользуются до сих пор ("способ Бородина"). Музыкальные достижения К 1867 г. относится сочинение Бородиным Первой симфонии. К концу 1860-х гг. им был написан цикл романсов на собственные тексты, начата работа над Второй (Богатырской) симфонией и оперой "Князь Игорь". Умер Бородин в 1887 г. В 1890 г. опера "Князь Игорь" была поставлена на сцене Мариинского театра.
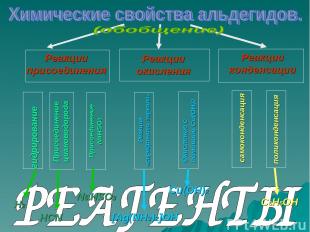
Реакции присоединения Реакции окисления Реакции конденсации гидрирование Присоединение циановодорода Присоединение NaHSO3 Реакция «серебряного зеркала» Окисление с помощью Сu(OH)2 самоконденсация поликонденсация H2 HCN NaHSO3 [Ag(NH3)2]OH Сu(OH)2 С6H5OH
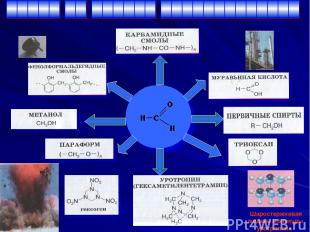
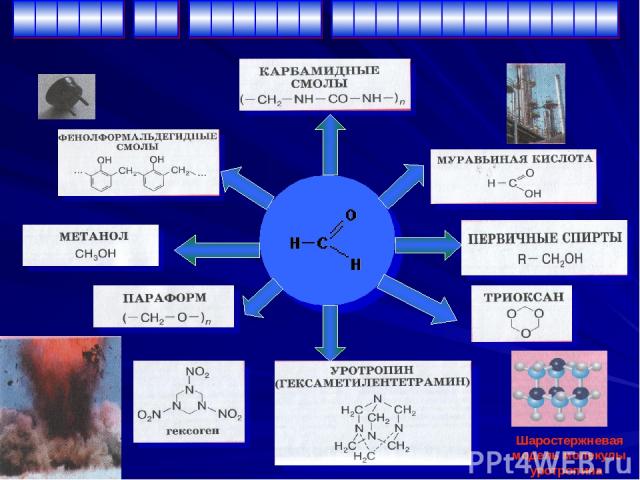
Шаростержневая модель молекулы уротропина

1 2 3 4 5 6 7 8 9 10 11 А А А А А А А А К К А К К Р Р Р Р О О О О О Л Л Л Л Л Л Л Е Е Е Е Е Е И И И И И Н Н Н Н Н Н Н Н Н Н Т Т Т Т Т Б Ь Ь Ь Т Я Я Д Д Д Ь С Г Ф Г М М П Э Ц

Используемая литература О.С.Габриелян «Химия-10». О.С.Габриелян, И.Г.Остроумова. «Настольная книга учителя химии. 10 класс». А.А.Карцова, А.Н.Лёвкин «Органическая химия. Иллюстрированный курс».





![– C OH 2. Реакции окисления. R – C O O H [О] R CH3 – C O H + Ag2O O H CH3 – C O OH CH3 – C CH3 – C + 2Cu(OH)2 O OH + Cu2O + 2H2O – C OH 2. Реакции окисления. R – C O O H [О] R CH3 – C O H + Ag2O O H CH3 – C O OH CH3 – C CH3 – C + 2Cu(OH)2 O OH + Cu2O + 2H2O](https://fs3.ppt4web.ru/images/132073/183328/640/img9.jpg)



![Реакции присоединения Реакции окисления Реакции конденсации гидрирование Присоединение циановодорода Присоединение NaHSO3 Реакция «серебряного зеркала» Окисление с помощью Сu(OH)2 самоконденсация поликонденсация H2 HCN NaHSO3 [Ag(NH3)2]OH Сu(OH)2 С6H5OH Реакции присоединения Реакции окисления Реакции конденсации гидрирование Присоединение циановодорода Присоединение NaHSO3 Реакция «серебряного зеркала» Окисление с помощью Сu(OH)2 самоконденсация поликонденсация H2 HCN NaHSO3 [Ag(NH3)2]OH Сu(OH)2 С6H5OH](https://fs3.ppt4web.ru/images/132073/183328/640/img14.jpg)