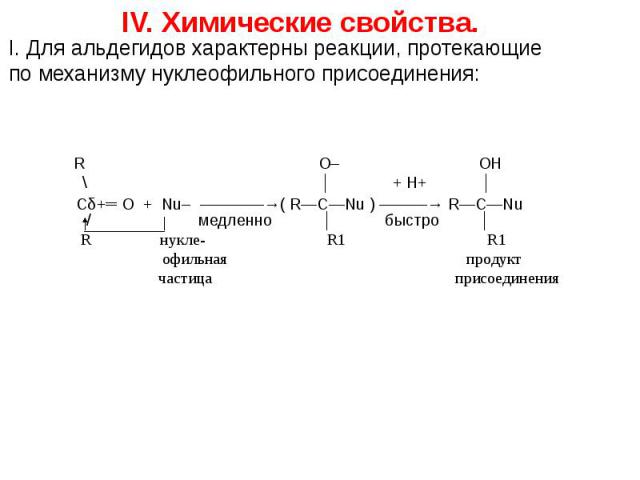
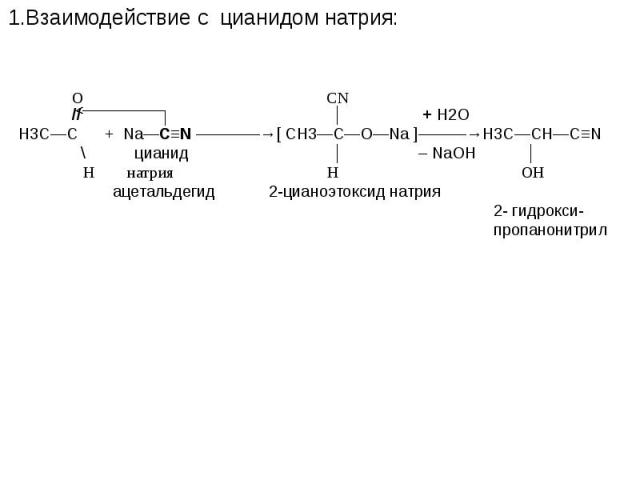
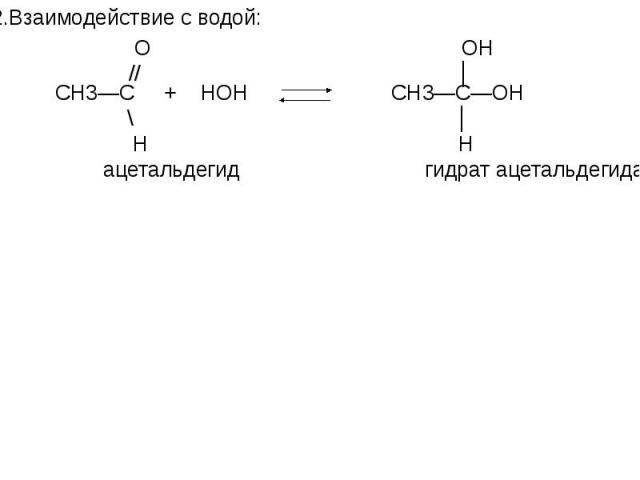
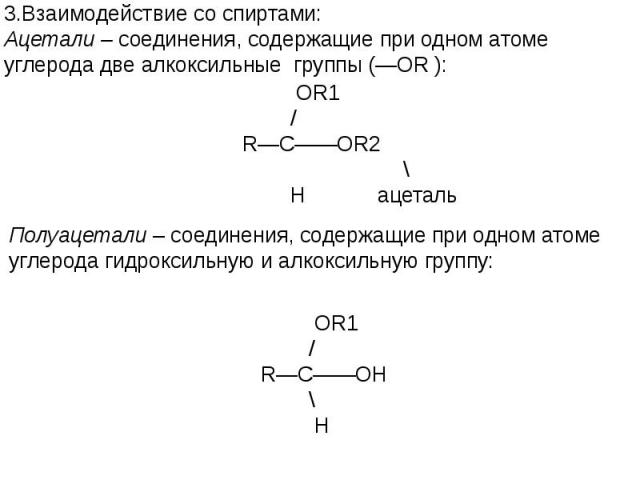
Презентация на тему: АЛЬДЕГИДЫ, КЕТОНЫ

Лекция №11. ТЕМА: АЛЬДЕГИДЫ, КЕТОНЫ.

I. Общая характеристика альдегидов и кетонов. Карбонильные соединения (оксосоединения) – это соединения, содержащие карбонильную \ группу С═О. /

Оксосоединения делятся на две группы: O // 1.Альдегиды – соединения, содержащие альдегидную групп—С . \ H Им можно дать и такое определение: « Это соединения, содержащие карбонильную группу, связанную с атомом водорода и углеводородным радикалом». O // R—C общая формула альдегидов. \ H

2. Кетоны – соединения, содержащие карбонильную \ группу С═О, связанную с двумя / углеводородными радикалами. \ Группу С ═ О называют также кетонной группой /
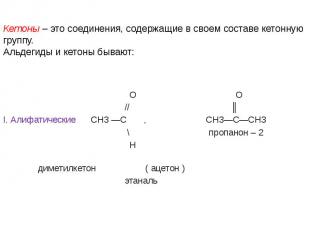
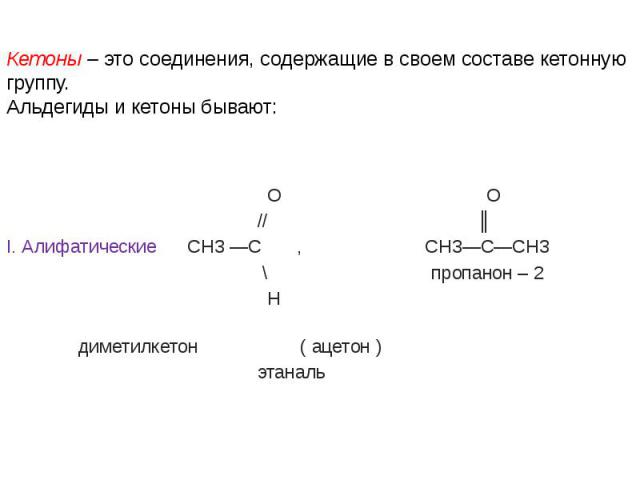
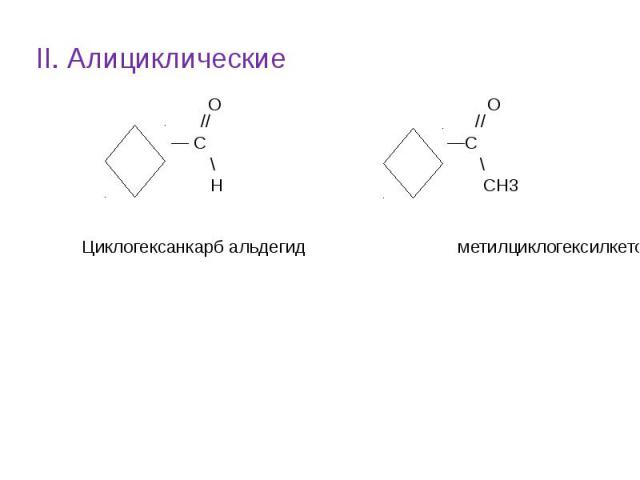
Кетоны – это соединения, содержащие в своем составе кетонную группу. Альдегиды и кетоны бывают: О О // ║ I. Алифатические СН3 —С , СН3—С—СН3 \ пропанон – 2 Н диметилкетон ( ацетон ) этаналь
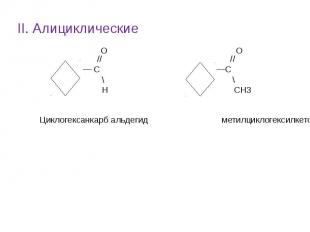
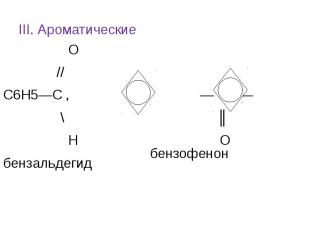
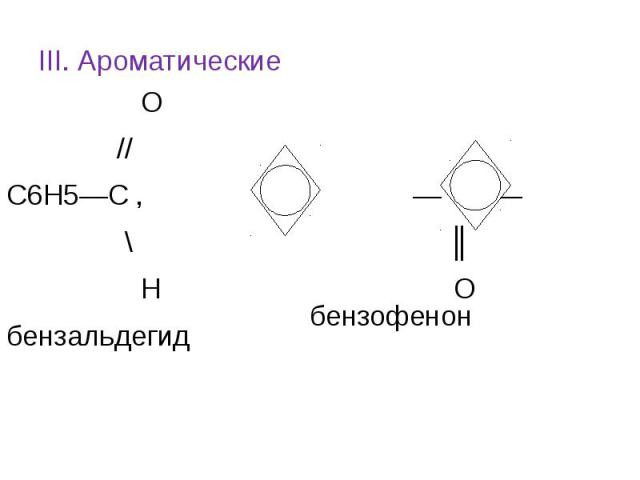
III. Ароматические О // С6Н5—С , — С — \ ║ Н О бензальдегид
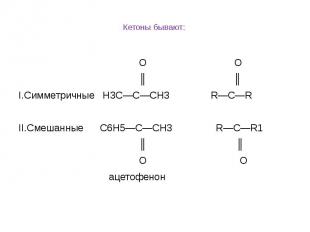
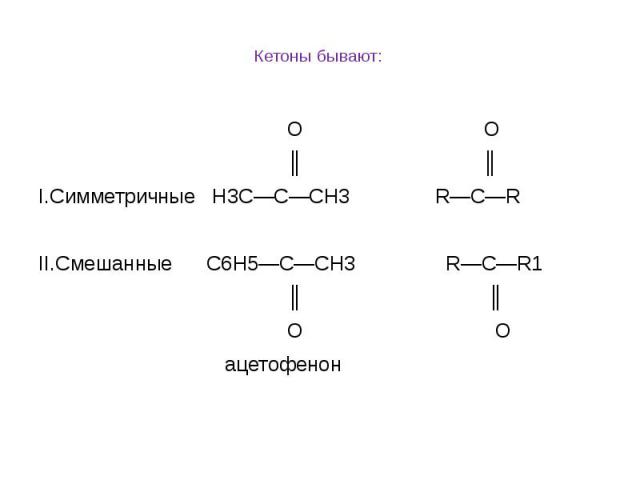
Кетоны бывают: O О ║ ║ I.Симметричные Н3С—С—СН3 R—C—R II.Смешанные С6Н5—С—СН3 R—C—R1 ║ ║ О O ацетофенон

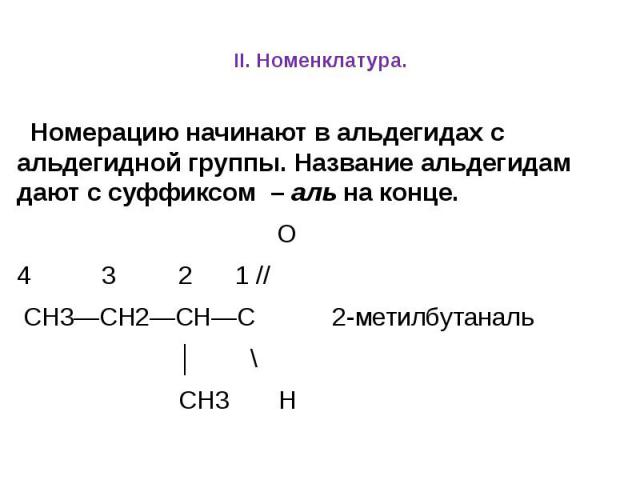
II. Номенклатура. Номерацию начинают в альдегидах с альдегидной группы. Название альдегидам дают с суффиксом – аль на конце. О 4 3 2 1 // СН3—СН2—СН—С 2-метилбутаналь │ \ СН3 Н
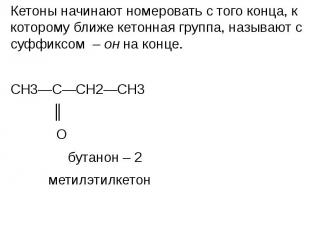
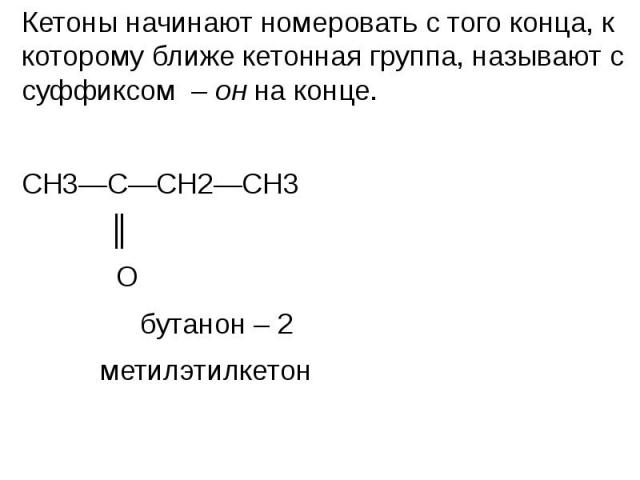
Кетоны начинают номеровать с того конца, к которому ближе кетонная группа, называют с суффиксом – он на конце. Кетоны начинают номеровать с того конца, к которому ближе кетонная группа, называют с суффиксом – он на конце. СН3—С—СН2—СН3 ║ О бутанон – 2 метилэтилкетон

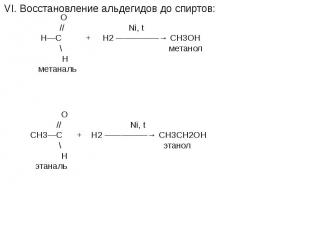
Гомологический ряд альдегидов: О // 1.Н—С метаналь ( формальдегид, муравьиный альдегид, \ 40% р-р называют – формалин ). Н О // 2.СН3—С этаналь ( уксусный альдегид ). \ Н

О О // 3.СН3—СН2—С пропаналь ( пропионовый альдегид ). \ Н О // 4. СН3—СН2—СН2—С бутаналь (масляный альдегид) \ Н О // 5. СН3—(СН2)3—С пентаналь ( валериановый альдегид ). \ Н

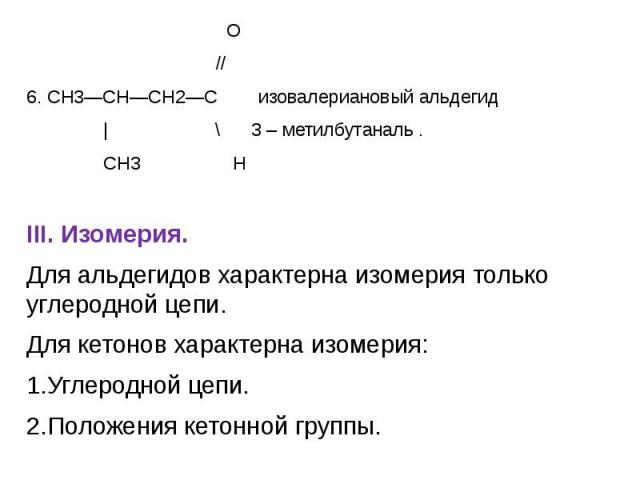
О О // 6. СН3—СН—СН2—С изовалериановый альдегид | \ 3 – метилбутаналь . CH3 Н III. Изомерия. Для альдегидов характерна изомерия только углеродной цепи. Для кетонов характерна изомерия: 1.Углеродной цепи. 2.Положения кетонной группы.
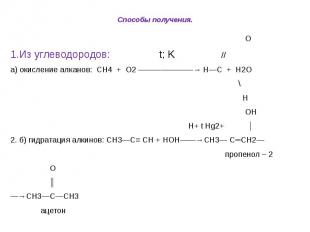
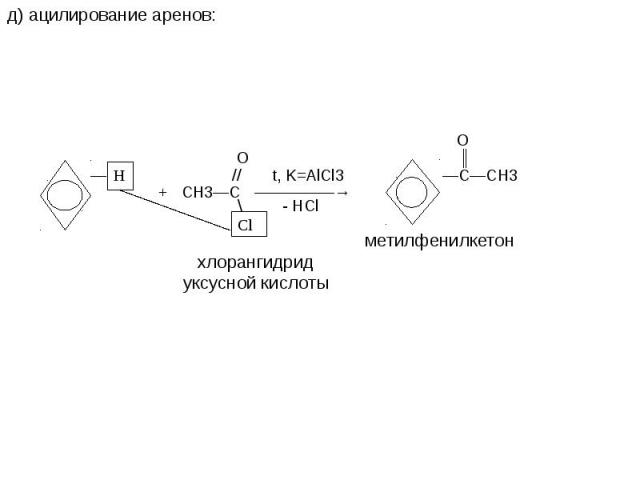
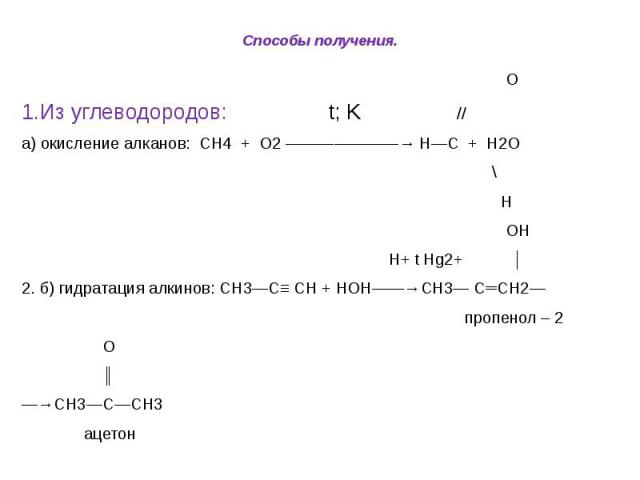
Способы получения. О 1.Из углеводородов: t; K // а) окисление алканов: СН4 + О2 ———————→ Н—С + Н2О \ Н ОН Н+ t Hg2+ │ 2. б) гидратация алкинов: СН3—С≡ СН + НОН——→СН3— С═СН2— пропенол – 2 О ║ —→СН3—С—СН3 ацетон
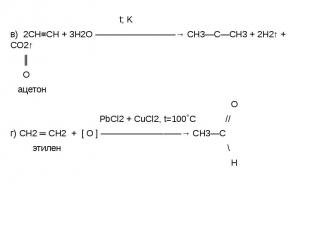
t; K t; K в) 2СН≡СН + 3Н2О —————————→ СН3—С—СН3 + 2Н2↑ + СО2↑ ║ О ацетон О PbCl2 + CuCl2, t=100˚C // г) СН2 ═ СН2 + [ О ] —————————→ СН3—С этилен \ Н
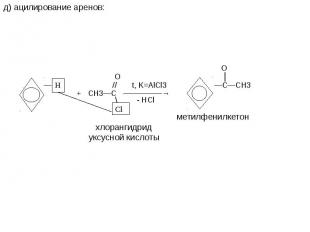
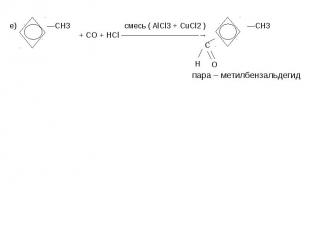
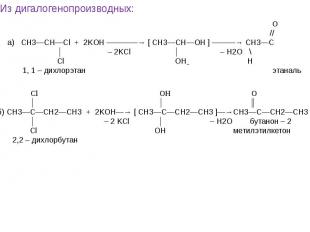
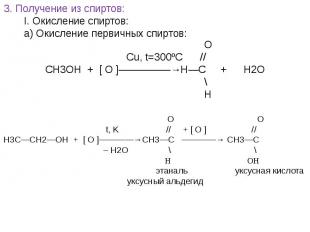
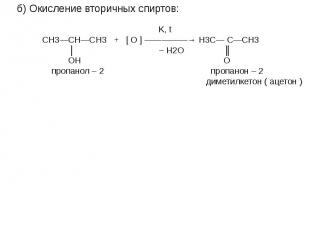
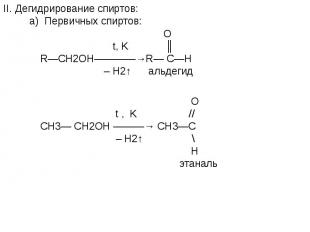
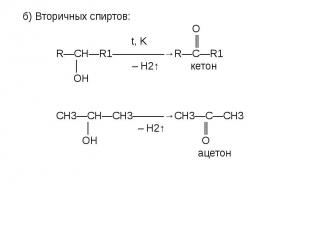
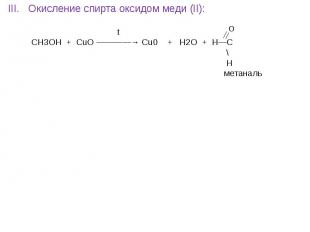
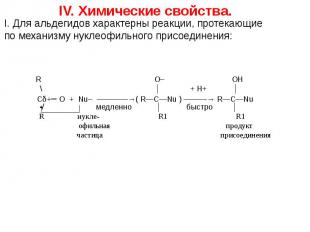
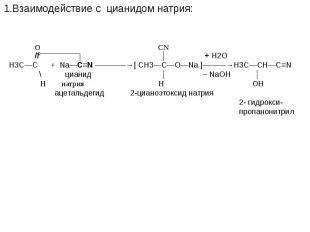
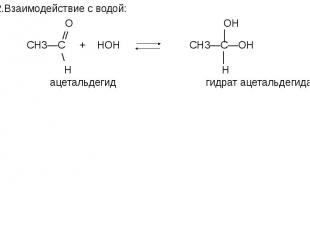
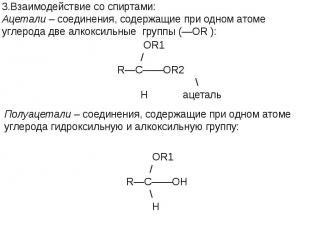
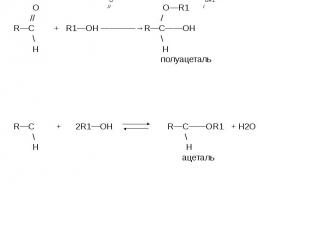
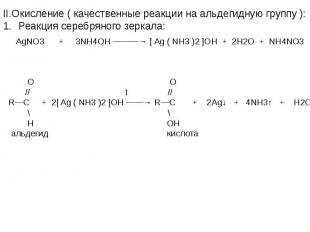
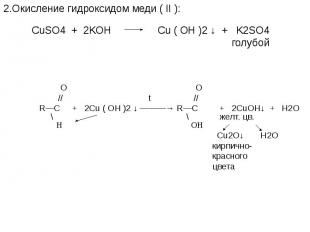
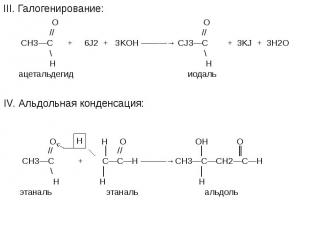
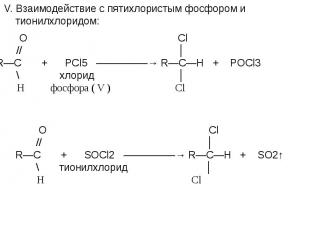









![t; K t; K в) 2СН≡СН + 3Н2О —————————→ СН3—С—СН3 + 2Н2↑ + СО2↑ ║ О ацетон О PbCl2 + CuCl2, t=100˚C // г) СН2 ═ СН2 + [ О ] —————————→ СН3—С этилен \ Н t; K t; K в) 2СН≡СН + 3Н2О —————————→ СН3—С—СН3 + 2Н2↑ + СО2↑ ║ О ацетон О PbCl2 + CuCl2, t=100˚C // г) СН2 ═ СН2 + [ О ] —————————→ СН3—С этилен \ Н](https://fs1.ppt4web.ru/images/95289/117436/640/img14.jpg)