Презентация на тему: «Окислительно-восстановительные реакции» химия

Министерство Здравоохранения Республики Казахстан Южно-Казахстанская Фармацевтическая Академия Кафедра ФГЗ и химии Выполнил: Сейдуали Е. Проверила: Рустемова Г. С. Группа: 202 ФТ Роль ОВР в анализе лекарственных препаратов, применение в клинических исследованиях и метоболизме лекарственных веществ. Шымкент 2013 900igr.net

Окислительно-восстановительные реакции - (реакции окисления-восстановления), химические реакции, сопровождающиеся изменением степени окисления атомов, входящих в состав реагирующих веществ. Первоначально окислением назывались только реакции веществ с O2, а восстановлением — реакции, в результате которых вещество теряло атом кислорода. С введением в химию электронных представлений понятие окислительно-восстановительных реакций распространилось и на реакции без участия кислорода. Окислитель, как отъявленный злодей, Как пират, бандит, агрессор, Бармалей, Отнимает электроны - и OK! Потерпев урон, восстановитель Восклицает: "Вот я! Помогите! Электроны мне мои верните!" Но никто ему не помогает И тем более ущерб не возмещает. Что такое ОВР?

Окислением называется процесс отдачи атомом, молекулой или ионом электронов. Степень окисления при этом повышается. Восстановлением называется процесс присоединения электронов атомом, молекулой или ионом. Степень окисления при этом понижается.

В любой окислительно-восстановительной реакции участвуют не менее двух редокс-пар не менее одного окислителя и одного восстановителя. Возможность прохождения окислительно-восстановительной реакции определяется химической активностью редокс-пар, участвующих в ней.

Химическую активность редокс-пары характеризуют величиной стандартного (нормального) окислительно-восстановительного потенциала (редокс-потенциала) Е°. Потенциал измеряют в электрохимической ячейке типа гальванического элемента, состоящей из стандартного и индикаторного электрода, на котором проходит электрохимическая реакция восстановления или окисления компонента редокс-пары. Измерение потенциала индикаторного (обычно платинового) электрода проводят относительно стандартного (нормального) водородного электрода.
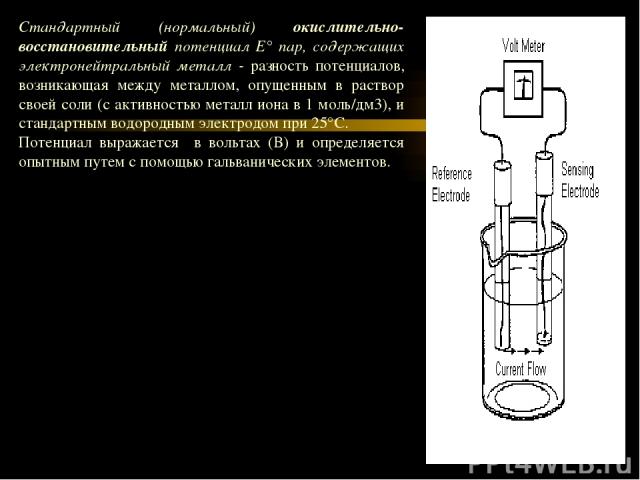
Стандартный (нормальный) окислительно-восстановительный потенциал Е° пар, содержащих электронейтральный металл - разность потенциалов, возникающая между металлом, опущенным в раствор своей соли (с активностью металл иона в 1 моль/дм3), и стандартным водородным электродом при 25°С. Потенциал выражается в вольтах (В) и определяется опытным путем с помощью гальванических элементов.
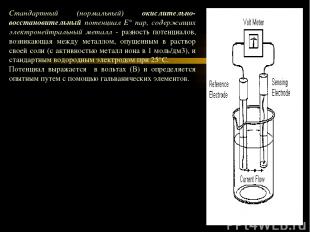
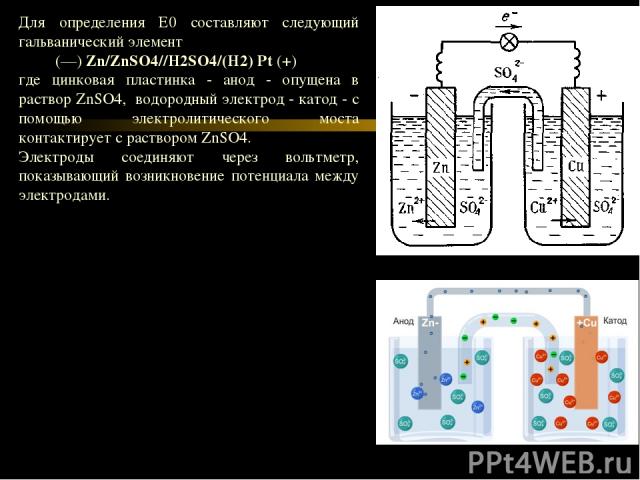
Для определения Е0 составляют следующий гальванический элемент (—) Zn/ZnSO4//H2SO4/(H2) Pt (+) где цинковая пластинка - анод - опущена в раствор ZnSO4, водородный электрод - катод - с помощью электролитического моста контактирует с раствором ZnSO4. Электроды соединяют через вольтметр, показывающий возникновение потенциала между электродами.
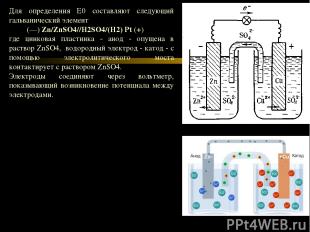
При увеличении величины Е0 увеличивается сила окислителя и соответственно уменьшается сила восстановителя. Направление протекания реакций Направление протекания реакции зависит от знака электродвижущей силы (ЭДС). ЭДС= Еок-Ефвос При ЭДС>0 протекает прямая реакция, При ЭДС
Потенциал системы определяют по уравнению Нернста-Петерса: E- Стандартный редокс потенциал R- Универсальная газовая постоянная Т- абсолютная температура (Т=273+t C) F – постоянная Фарадея n – число электронов, участвующих в процессах окисления или восстановления. Подставив в уравнение значения F, R и преобразовав ln в lg, получим:

Факторы, влияющие на окислительно-восстановительные реакции На механизм окислительно-восстановительных реакций оказывают влияние состояние окислителя и восстановителя, рН среды, растворитель, температура, катализатор, наличие побочных реакций. В зависимости от рН среды и состояния окислителей и восстановителей изменение степени окисления элемента на одну и ту же величину протекает при различных значениях потенциалов.

Повышение щелочности среды (возрастание рН) снижает величину потенциала (и окислительные свойства) окислителя и восстановителя, увеличивая его восстановительные свойства. Уменьшение значения рН (увеличение концентрации Н+ ионов) приводит, наоборот, к повышению значения Е°.

Изменение рН среды приводит не только к изменению величины потенциала, но и к образованию иных продуктов. Сильное влияние на окислительно-восстановительные реакции оказывает температура, повышение которой согласно уравнению увеличивает потенциал окислительно-восстановительной пары. Это явление используют для ускорения протекания некоторых окислительно-восстановительных реакций.

Важнейшие восстановители Металлы Соли, содержащие ионы: Fe2+, Sn2+, Mn2+, Cr2+ и др. Вещества, содержащие элементы в низшей СО: NH3, H2S, HCl, HBr, КI H2 C CO
Важнейшие окислители Вещества, содержащие элементы в высшей СО: KMnO4 K2Cr2O7 KBiO3 Галогены: F2, Cl2, Br2, I2 Оксиды: MnO2, PbO2, CuO, Ag2O O2, O3 Fe3+, Ce4+, ионы благородных металлов: Ag+, Au3+ и др. Кислоты: H2SO4 (конц.), HNO3, H2SeO4, «царская водка»
В качестве окислителей чаще в фармацевтических учреждениях применяются титрованные растворы перманганата калия, бихромата калия, йода, йодата калия и брамата калия. С восстановителей применяются растворы тиосульфата натрия (для определения йода), сульфата железа (2 +), мышьяковистой кислоты, хлорида (2 +) и т.д. Отсюда отражают отдельные названия методик - йодометрия, броматометрия, перманганатометрия (манганометрия) и т.д.

Методы окислительно-восстановительного титрования пригодны для определения многих органических лекарственных веществ, которые являются потенциальными восстановителями, поэтому могут быть окислены до веществ с целью восстановительной способностью, чем исходные вещества. Конечную точку титрования в окислительно-восстановительных методах определяют с помощью редокс-индикаторов - веществ, способных в среде с определенным окислительно-восстановительным потенциалом окисляться и менять свою окраску, а также специфических индикаторов (например метиловый красный в броматометрии, крахмал в йодометрии ).

Перманганатометрия базируется на использовании лекарственных веществ, определяемых перманганат-ионами. Чаще всего в титриметрическом анализ применяются реакции окисления перманганат-ионами в сильно-кислой среде. Методом перманганатометрии определяют количественное содержание раствора перекиси водорода, магния перекиси, натрия нитрита.