Презентация на тему: Окислительно-восстановительные реакции

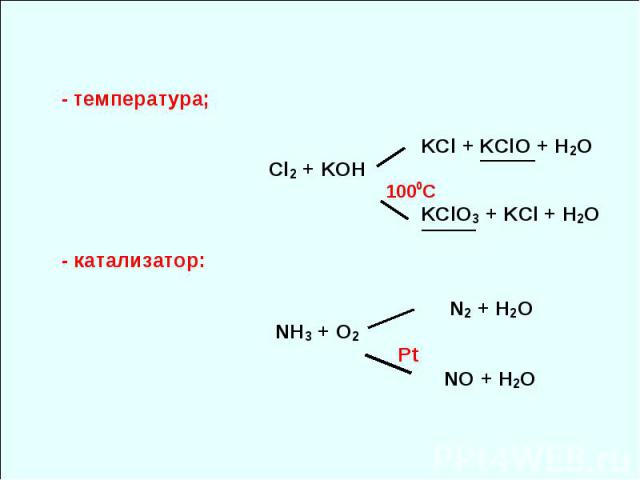
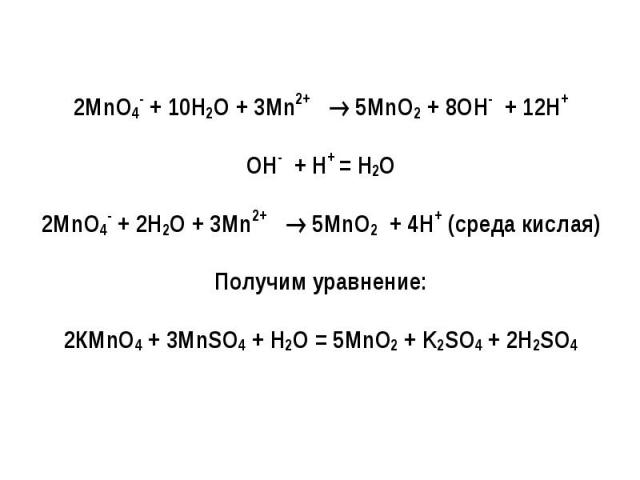
Окислительно-восстановительные реакции
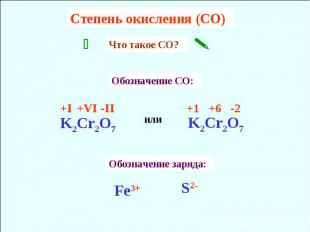
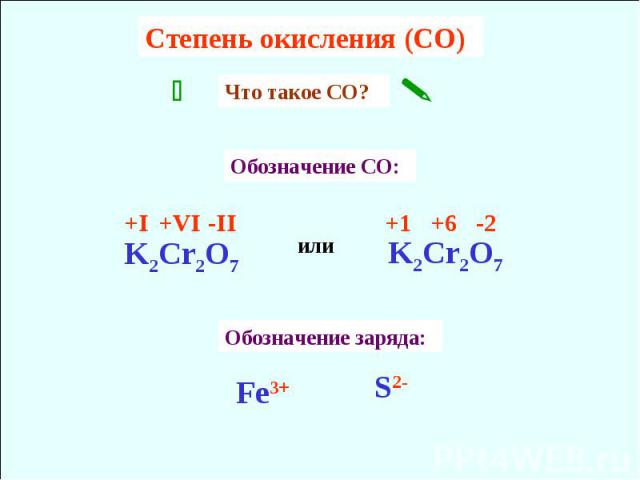
Cтепень окисления (CO) Что такое CО? Обозначение CO: Обозначение заряда:
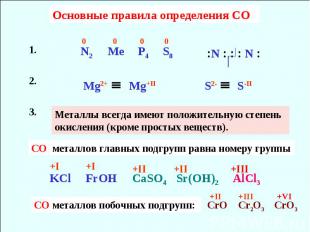
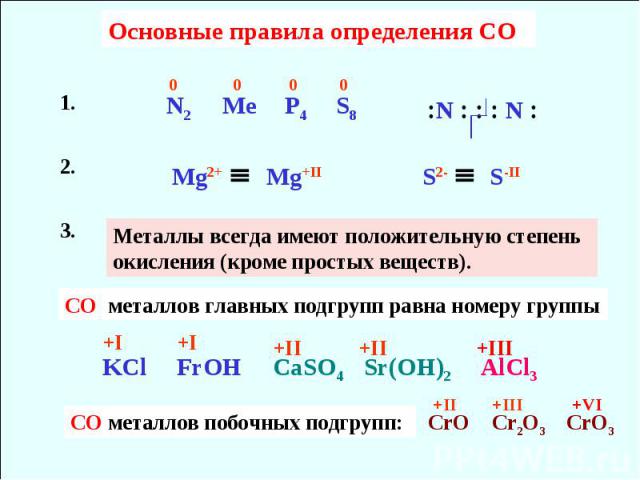
Основные правила определения CO Металлы всегда имеют положительную степень окисления (кроме простых веществ). СO металлов главных подгрупп равна номеру группы СО металлов побочных подгрупп:
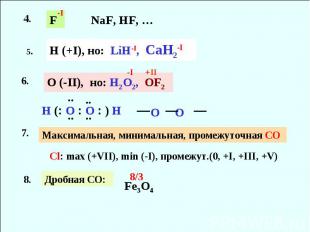
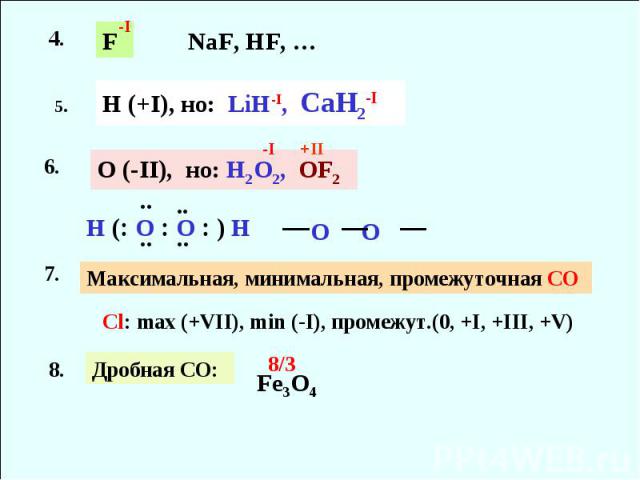
H (+I), но: LiH-I, CaH2-I NaF, HF, … O (-II), но: H2O2, OF2 H ( O O ) H Максимальная, минимальная, промежуточная СО Сl: max (+VII), min (-I), промежут.(0, +I, +III, +V) Дробная СО:

В сложных соединениях KNO3 CO азота: 1 + х - 6 = 0 х = +5 CO хрома: 2х - 14 = -2 х = + 6 LiNbO3 U2O72- углерод С -IV 0 +II +IV CO2H2CO3Na2CO3

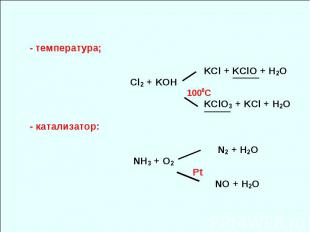
K2SO3 + H2O KHSO3 + KOH K2SO3 + H2O2 = K2SO4 + H2O Об окислителях и восстановителях Процессы окисления и восстановления На окислителе идет процесс восстановления Cl2 + 2 е = 2Сl- Fe3+ + 1 e = Fe2+ На восстановителе идет процесс окисления Fe2+ - 1 e = Fe3+ 2Cl- - 2 e = Cl2
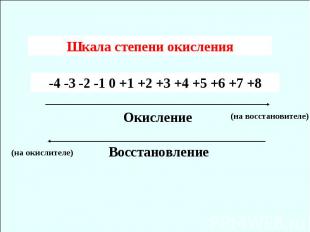
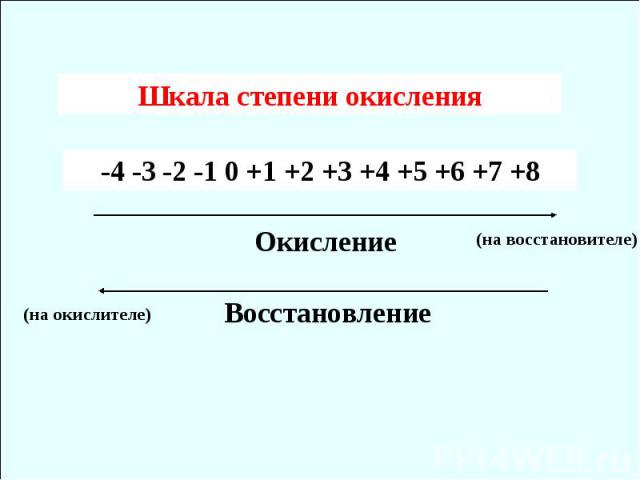
Шкала степени окисления -4 -3 -2 -1 0 +1 +2 +3 +4 +5 +6 +7 +8 Окисление Восстановление

K2SO3 - вещество-восстановитель K2SO3 + H2O2 = K2SO4 + H2O SO32- - ион-восстановитель SIV - атом-восстановитель H2O2 – вещество-окислитель О22- -ион-окислитель

Важнейшие окислители и восстановители F2, Cl2, Br2, О2 (при повышенных т-рах) KMnO4, K2Cr2O7, PbO2, HNO3, Катионы металлов более высокой CO: Fe3+, Au3+, Sn4+ Восстановители: Na, Ca, Zn, Al, H2, C, Na2S, KI, SnCl2, Fe(NO3)2, NH3, … Вещества с двойственной природой: H2O2, SO2, KNO2, H2O2 + KI+ H2SO4 = H2O + I2 + K2SO4 H2O2 + KMnO4 + H2SO4 = O2 + MnSO4 + K2SO4 + H2O

Составление уравнений ОВР Главное в металлургии: M+z M0 Метод электронного баланса PbS + O2 = PbO + SO2 (T ~ 1000C) O20 + 4 e = 2 O-II 3S-II - 6 e = SIV 2 3O20 + 2S-II =6O-II +2 SIV 2PbS + 3O2 = 2PbO + 2SO2

Метод полуреакций K2Cr2O7 + K2SO3 + H2SO4 = Cr2(SO4)3 + K2SO4 + H2O Cr2O72- + 14 H+ + 6 е 2Cr3+ + 7H2O 1SO32- + H2O - 2 е SO42- + 2H+ 3 Cr2O72- + 14H+ + 3SO32- + 3H2O 2Cr3+ + 7H2O + 3SO42- + 6H+ Cr2O72- + 8H+ + 3SO32- 2Cr3+ + 4H2O + 3SO42- K2Cr2O7 + 3K2SO3 + 4H2SO4 = Cr2(SO4)3 + 4K2SO4 + 4H2O

О том, как составляются полуреакции для уравнивания ОВР в щелочной и нейтральной средах, смотрите на сайте кафедры «Дополнительные материалы» Лекции № 8 «ОВР»





Окислительно-восстановительный эквивалент Что такое эквивалент ? ОВЭ = Мr/z Mr (KMnO4) = 158 OЭ(KMnO4) Закон эквивалентов Nок Vок = Nвосст Vвосст n окислителя = n восстановителя

Дополнительные материалы Лекции № 8 «ОВР» Составление полуреакций для уравнивания ОВР в щелочной и нейтральной средах

ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ

Метод полуреакций для ОВР, протекающих в щелочной среде
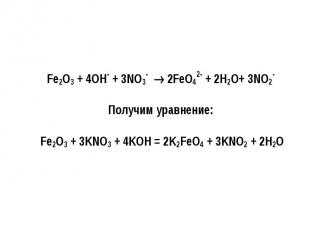

Метод полуреакций, протекающих в нейтральной среде
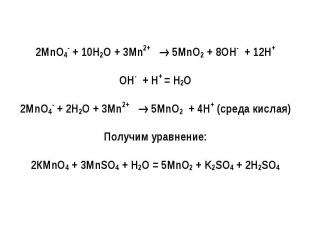

Электрохимический ряд напряжений металлов Li, Rb, K, Ba, Sr, Ca, Na, Mg, Al, Mn, Zn, Cr, Fe, Cd, Co, Ni, Sn, Pb, H, Sb, Bi, Cu, Hg, Ag, Pd, Pt, Au Металлы расположены в порядке возрастания их стандартных электродных потенциалов

Ряд напряжений характеризует химические свойства металлов: 1. Чем более отрицателен электродный потенциал металла, тем больше его восстановительная способность Например: железо (φ° = - 0,44) более сильный восстановитель, чем медь (φ° = + 0,34) Но, катионы Cu2+ в водном растворе более сильный окислитель, чем Fe2+

2. Каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые стоят в ряду напряжений металлов после него Fe + CuSO4 → FeSO4 + Cu ↓ Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓ Исключение – щелочные и щелочно-земельные металлы 3. Все металлы, имеющие отрицательный электродный потенциал, т.е. находящиеся в ряду напряжений металлов левее водорода, способны вытеснять его из растворов кислот (HCl, HBr, HI, H3PO4, разбавленная H2SO4) Fe + H2SO4 → FeSO4 + H2 ↑; φ°Fe = -0,44
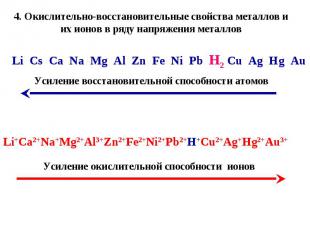
4. Окислительно-восстановительные свойства металлов и их ионов в ряду напряжения металлов Li Cs Ca Na Mg Al Zn Fe Ni Pb H2 Cu Ag Hg Au Усиление восстановительной способности атомов Li+Ca2+Na+Mg2+Al3+Zn2+Fe2+Ni2+Pb2+H+Cu2+Ag+Hg2+Au3+ Усиление окислительной способности ионов