Презентация на тему: окислительно- восстановительные реакции

окислительно-восстановительные реакции8 класс

Сумма степеней окисления химических элементов в соединении равна 0 Al2O3

В этой химической реакции степени окисления химических элементов в исходных веществах и в продуктах реакции не изменяютсяСu О + 2 HCl → CuCl2 + H2O Химические реакции, протекающие без изменения степеней окисления химических элементов, относятся к неокислительно-восстановительным реакциям.

CuO + CO → Cu + CO2 Химические реакции, протекающие c изменением степеней окисления химических элементов, относятся кокислительно-восстановительным реакциям.

По изменению степеней окисления химических элементов химические реакции делят на две группы:

Составление уравнений окислительно - восстановительных реакций методом электронного баланса

восстановитель,процесс окисленияокислитель,процесс восстанов-ления

Восстановитель – элемент, который отдает электроны.Окислитель – элемент, которыйпринимает электроны.

Процесс окисления – это процесс отдачи электронов.Процесс восстановления – это процесс присоединенияэлектронов.

Значение окислительно- восстановительных реакций

Лесные пожары

фотосинтез

Коррозия металлов

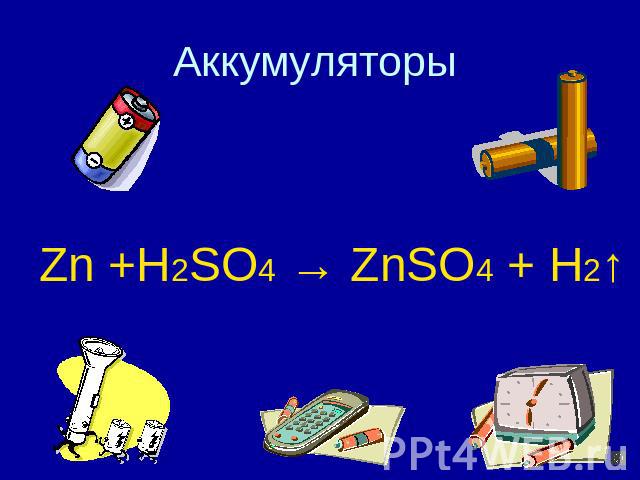
Аккумуляторы

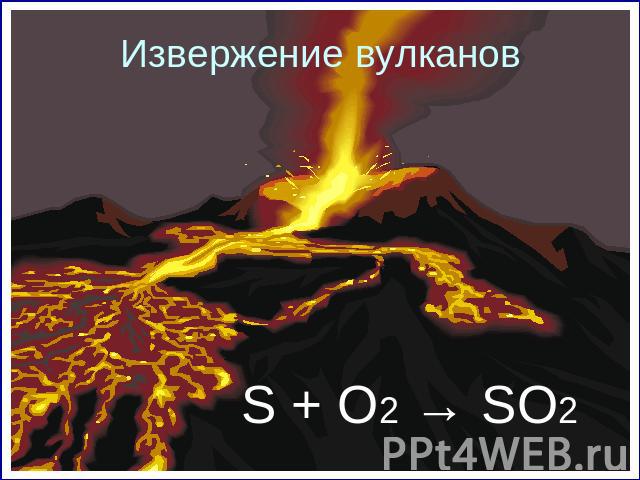
Извержение вулканов

Сгорание топлива

Брожение глюкозы

Взрывчатые вещества

Салют

Молния