Презентация на тему: Окислительно-восстановительные реакции

Готовимся к ЕГЭ Окислительно-восстановительные реакцииИз опыта работы учителя химии «МОУ СОШ № 73» г. Оренбурга Кочулевой Л. Р.

Окислительно-восстановительные реакции (ОВР) - – химические реакции, в которых происходит изменение степеней окисления атомов, входящих в состав реагирующих веществ.

Степень окисления Степень окисления атомов элементов простых веществ равна нулюСтепень окисления водорода в соединениях +1, кроме гидридовСтепень окисления кислорода в соединениях -2, кроме пероксидов и соединений с фторомСумма всех степеней окисления атомов в соединении равна нулюСумма всех степеней окисления атомов в ионе равна значению заряда иона

Распознавание уравнений ОВР Запишите значения степеней окисления атомов всех элементов в уравнении реакции Определите изменяется ли степень окисления атомов элементов. +2 -2 +1 -1 +2 -1 +1 -2 PbO + 2HCl → PbCl2 + H2O Степень окисления не изменяется => реакция не окислительно-восстановительная +4 -2 +1 -1 +2 -1 0 +1 -2 PbO2 + 2HCl → PbCl2 + Cl2 + 2H2O Степень окисления изменяется => реакция окислительно-восстановительная
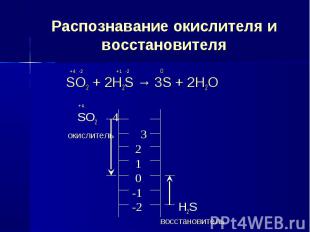
Распознавание окислителя и восстановителя

Метод электронного баланса
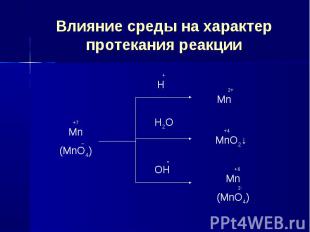
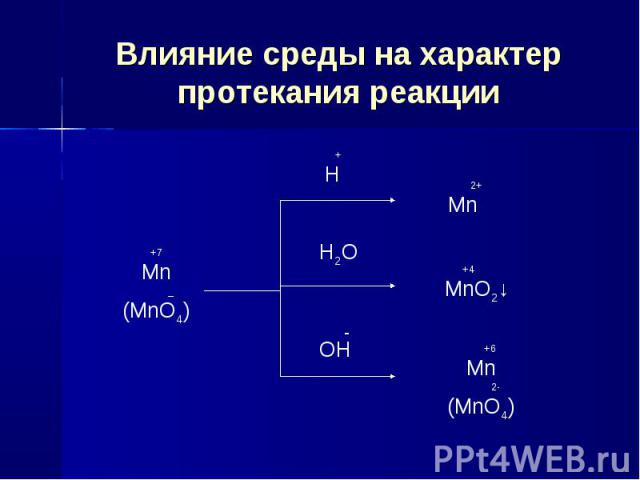
Влияние среды на характер протекания реакции

Используя метод электронного баланса, составьте уравнение реакции:FeSO4+KMnO4+…→…+K2SO4+K2MnO4 Степень окисления Mn изменяется от +7 до +6 в щелочной среде!FeSO4 окисляется в щелочной среде до Fe(OH)3FeSO4+KMnO4+3KOH→ Fe(OH)3 +K2SO4+K2MnO4FeSO4 – восстановитель, KMnO4 – окислитель

Используя метод электронного баланса, составьте уравнение pеакции:Zn+KMnO4+…→…+K2SO4+MnSO4 +Н2О Степень окисления Mn изменяется от +7 до +2 в кислой среде!Электронный баланс: Mn+7 + 5e- → Mn+2 2 Zn0 – 2e- → Zn+2 55Zn+2KMnO4+8H2SO4→5ZnSO4 ++K2SO4+2MnSO4 +8Н2О

Используя метод электронного баланса, составьте уравнение реакции: K2SO3+KMnO4+…→…+MnO2 +… Степень окисления Mn изменяется от +7 до +4 в нейтральной среде!Электронный баланс: Mn+7 + 3e- → Mn+4 2 S+4 – 2e- → S+6 33K2SO3+2KMnO4+H2O→3K2SO4+2MnO2 +2KОH
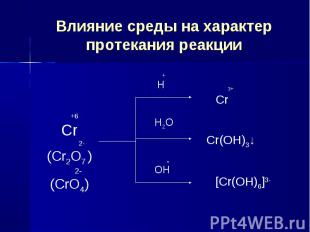
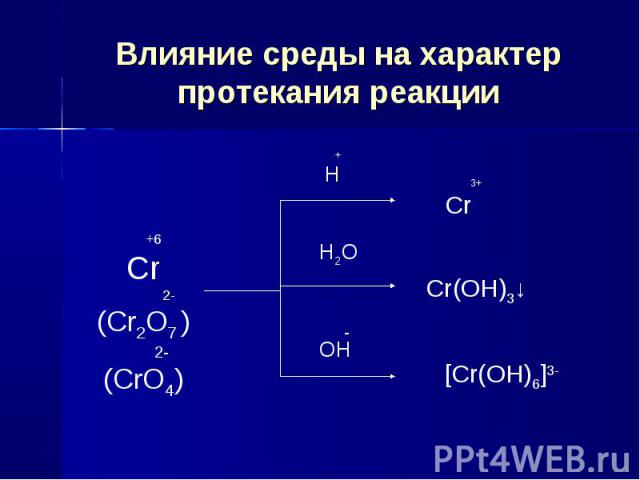
Влияние среды на характер протекания реакции
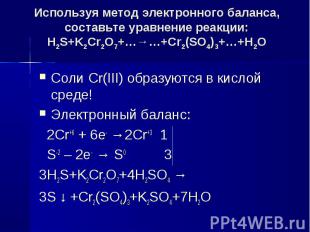
Используя метод электронного баланса, составьте уравнение pеакции: H2S+K2Cr2O7+…→…+Cr2(SO4)3+…+H2O Соли Cr(III) образуются в кислой среде!Электронный баланс: 2Cr+6 + 6e- →2Cr+3 1 S-2 – 2e- → S0 33H2S+K2Cr2O7+4H2SO4 →3S ↓ +Cr2(SO4)3+K2SO4+7H2O

Используя метод электронного баланса, составьте уравнение pеакции: H2S+K2CrO4+…→…+Cr(OH)3 ↓ +KOH Гидроксид хрома(III) образуется в нейтральной среде.Электронный баланс: Cr+6 +3e- →Cr+3 2 S-2 – 2e- → S0 33H2S+2K2CrO4+2H2O →3S↓ +2Cr(OH)3 ↓ +4KOH

Используя метод электронного баланса, составьте уравнение pеакции: K2CrO4+H2O2+…→K3[Cr(OH)6]+O2↑+… Комплексный анион [Cr(OH)6]3- образуется в щелочной среде.Электронный баланс: Cr+6 +3e- →Cr+3 2 2O-1 – 2e- → O2 32K2CrO4+3H2O2+2KOH+2H2O →2K3[Cr(OH)6]+3O2↑Т.к. в правой части уравнения в составе гидроксокомплекса содержится уже 6 атомов водорода, вода переносится в левую часть уравнения.

Используя метод электронного баланса, составьте уравнение pеакции: NaCrO2+…+NaOH→…+NaBr +H2O Соединения хрома(III) при окислении в щелочной среде образуют хроматы (CrO42-). Степень окисления хрома увеличивается от +3 до +6, следовательно NaCrO2 является восстановителем, а окислителем будет служить Br2, степень окисления которого снижается от 0 до -1.Электронный баланс: Cr+3-3e-→ Cr+6 2 Br2+2e-→2Br- 32NaCrO2+3Br2+8NaOH→2 Na2 CrO4+6NaBr +4H2O

ОВР азотной кислоты

ОВР азотной кислоты 0 +5 +2 +14Ca + 10HNO3(конц.) → 4Ca(NO3)2 + N2O + 5H2O 0 _ +2Ca – 2 e → Ca 4 +5 _ +12N + 8 e → 2N 1Ca – восстановительHNO3 – окислитель 0 +5 +2 +4Cu + 4HNO3(конц.)→Cu(NO3)2 +2NO2 + 2H2O

ОВР азотной кислоты S0 + 6HNO3(конц) = H2S+6O4 + 6NO2 + 2H2OB0 + 3HNO3 (конц)= H3B+3O3 + 3NO23P0 + 5HNO3 + 2H2O = 5NO + 3H3P+5O4P0 + 5HNO3 (конц) = 5NO2 + H3P+5O4+H2O

ОВР азотной кислоты +2 -1 +5 +3 +6 +4FeS2 + 18HNO3(конц.)→Fe(NO3)3+2H2SO4+15NO2+7H2O +2 _ +3Fe – 1 e → Fe _ – 15 e 1 -1 _ +62S – 14 e → 2S +5 _ +4 N + e → N 15FeS2 – восстановительHNO3 – окислитель

ОВР с участием органических соединений Окисление алкенов в нейтральной среде: C2H4 + 2KMnO4 + 2H2O→ CH2OH–CH2OH + 2MnO2 + 2KOH Окисление алкенов в кислой среде: CH3CH=CH2 +2KMnO4 +3H2SO4 →CH3COOH +CO2 +2MnSO4 +K2SO4 +4H2O Окисление алкенов в щелочной среде:CH3CH=CH2 + 10KMnO4 + 13KOH→ CH3COOK + K2CO3 + 8H2O + 10K2MnO4

Окисление алкинов в нейтральной среде:3CH≡CH +8KMnO4→3KOOC – COOK +8MnO2 +2КОН +2Н2О 2C-1 – 8e- → 2C+3 3 Mn+7 +3e- →Mn+4 8 в кислой среде:5CH≡CH +8KMnO4 +12H2SO4 →5HOOC– COOH +8MnSO4 +4К2SO4 +12Н2ОCH≡CH + 2KMnO4 +3H2SO4 =2CO2 + 2MnSO4 + 4H2O + K2SO4
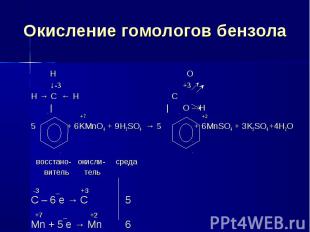
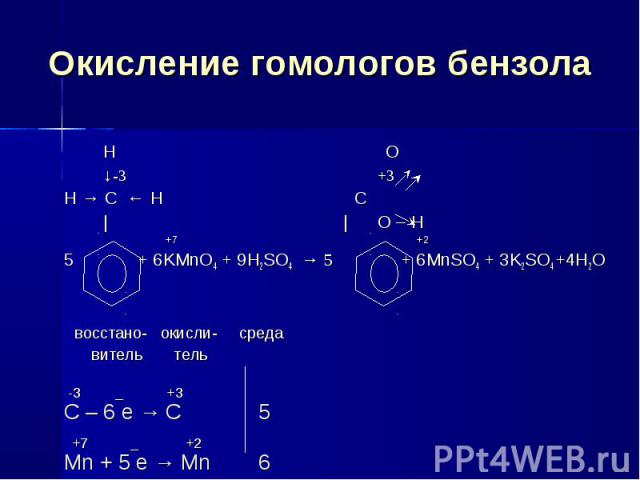
Окисление гомологов бензола H O ↓-3 +3H → C ← H C | | O – H +7 +25 + 6KMnO4 + 9H2SO4 → 5 + 6MnSO4 + 3K2SO4 +4H2O восстано- окисли- среда витель тель -3 _ +3С – 6 e → C 5 +7 _ +2Mn + 5 e → Mn 6

Окисление гомологов бензола Обратите внимание, что только α-углеродные атомы (непосредственно связанные с бензольным кольцом) окисляются до карбоксильных групп, остальные атомы углерода – до углекислого газа.5C6H5-CH2CH3 + 12KMnO4+18H2SO4→→5С6Н5СООН+CO2+12MnSO4 +6K2SO4 +28H2O C-2 -5e- →C+3 5 C-3 -7e- →C+4 Mn+7 +5e-→Mn+2 12

Окисление стирола В нейтральной среде:3C6H5-CH =CH2+2 KMnO4+ H2O→3C6H5-CH(OH) -CH2(OH)+2MnO2+2KOHВ кислой среде:C6H5-CH=CH2 +2KMnO4+3H2SO4→С6Н5СООН+CO2+2MnSO4 +K2SO4 +H2O

Окисление спиртов 3C2H5OH + K2Cr2O7 + 4H2SO4 = 3CH3CHO + K2SO4 + Cr2(SO4)3 + 7H2O 3СН2(ОН) – СН2(ОН) + 8КMnO4→3KOOC – COOK +8MnO2 +2КОН +8Н2О 5СН2(ОН) – СН2(ОН) + 8КMnO4-+12H2SO4→→5HOOC – COOH +8MnSO4 +4К2SO4 +22Н2О

Окисление альдегидов 3CH3CH=O + 2KMnO4 = CH3COOH ++ 2CH3COOK + 2MnO2 + H2O3CH3CH=O + K2Cr2O7 + 4H2SO4 == 3CH3COOH + Cr2(SO4)3 + 7H2O3СН2О + 2K2Cr2O7 + 8H2SO4 = = 3CO2 +2K2SO4 + 2Cr2(SO4)3 + 11H2O

Окисление карбоновых кислот НСООН + HgCl2 =CO2 + Hg + 2HClHCOOH+ Cl2 = CO2 +2HClHOOC-COOH+ Cl2 =2CO2 +2HCl

Список источников и литературы 1. Ахлебинин А.К., Нифантьев Э.Е., Анфилов К.Л. Органическая химия. Решение качественных задач. – М.: Айрис-пресс, 20062. Габриелян О.С. Химия: пособие для школьников старших классов и поступающих в вузы. – М.: Дрофа, 20063. Слета Л.А. Химия: Справочник. – Харьков: Фолио; М.: ООО «Издательство АСТ», 20004. Новошинский И.И., Новошинская Н.С. Переходные металлы. – Краснодар: «Советская Кубань», 20064.http://www1.ege.edu.ru/5. http://www.it-n.ru (сообщества «Химоза» и «Подготовка к ЕГЭ по химии»)












![Используя метод электронного баланса, составьте уравнение pеакции: K2CrO4+H2O2+…→K3[Cr(OH)6]+O2↑+… Комплексный анион [Cr(OH)6]3- образуется в щелочной среде.Электронный баланс: Cr+6 +3e- →Cr+3 2 2O-1 – 2e- → O2 32K2CrO4+3H2O2+2KOH+2H2O →2K3[Cr(OH)6]… Используя метод электронного баланса, составьте уравнение pеакции: K2CrO4+H2O2+…→K3[Cr(OH)6]+O2↑+… Комплексный анион [Cr(OH)6]3- образуется в щелочной среде.Электронный баланс: Cr+6 +3e- →Cr+3 2 2O-1 – 2e- → O2 32K2CrO4+3H2O2+2KOH+2H2O →2K3[Cr(OH)6]…](https://fs1.ppt4web.ru/images/5342/67870/640/img13.jpg)