Презентация на тему: Химические свойства оксидов

Химические свойства Способы получения 900igr.net
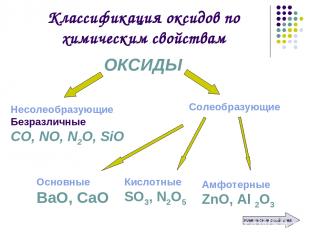
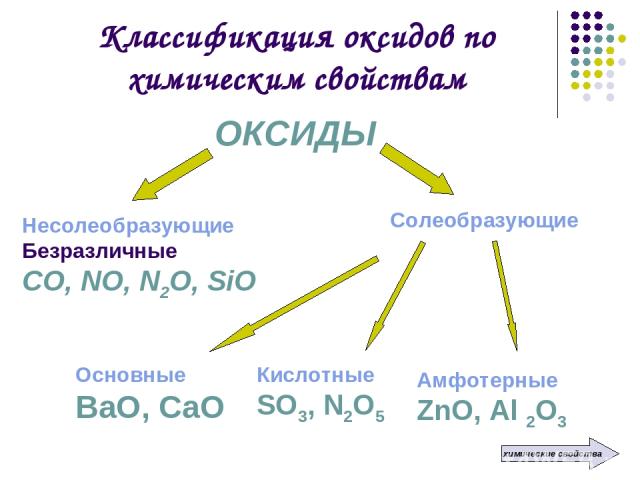
Классификация оксидов по химическим свойствам ОКСИДЫ Несолеобразующие Безразличные СО, NO, N2O, SiO Солеобразующие Основные ВаО, СаО Кислотные SO3, N2O5 Амфотерные ZnO, Al 2O3 химические свойства

Несолеобразующие оксиды – это оксиды, которые не взаимодействуют ни с кислотами, ни с основаниями и не образуют солей СО, NO, N2O, SiO

Солеобразующие оксиды – это оксиды, которые взаимодействуют с кислотами или со щелочами с образованием солей и воды

Основные оксиды – это оксиды, которым в качестве гидроксидов соответствуют основания Образованы металлами в степени окисления +1, +2 К2О → КОН MgO → Mg(OH)2

Кислотные оксиды – это оксиды, которым в качестве гидроксидов соответствуют кислоты Образованы неметаллами и металлами в степени окисления +5 и выше SО3 → Н2SО4

Амфотерные оксиды – это оксиды, которым соответствуют гидроксиды, проявляющие свойства как оснований, так и кислот Образованы металлами в степени окисления +3, +4, а также оксиды ВеО, ZnO, SnO, PbO ZnO → Zn(OH)2 или Н2ZnО2
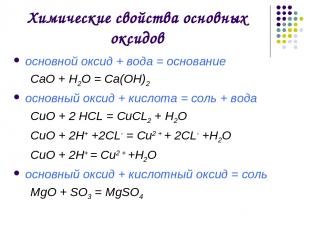
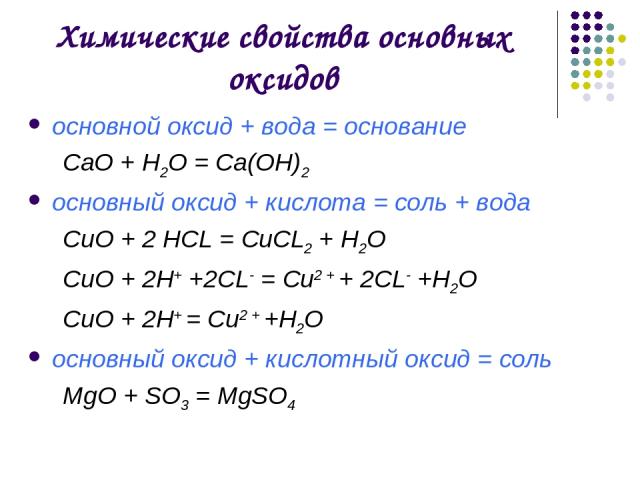
Химические свойства основных оксидов основной оксид + вода = основание СаO + H2O = Са(OН)2 основный оксид + кислота = соль + вода CuO + 2 HCL = CuCL2 + H2O CuO + 2H+ +2CL- = Cu2 + + 2CL- +Н2О CuO + 2H+ = Cu2 + +Н2О основный оксид + кислотный оксид = соль MgO + SO3 = MgSO4

Химические свойства кислотных оксидов кислотный оксид + вода = кислота Р2O5 + 3H2O = 2H3РO4 кислотный оксид + основание = соль + вода CO2 + Mg(OН)2= MgCO3 + H2O CO2 + Mg+ +2OН- = MgCO3 + Н2О кислотный оксид + основный оксид = соль SO3 + MgO = MgSO4

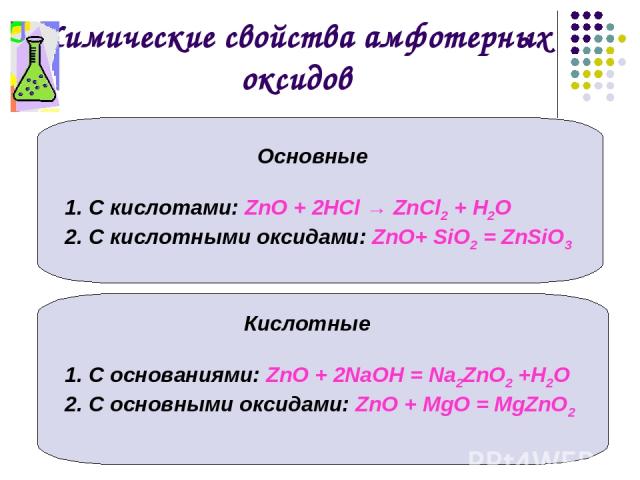
Химические свойства амфотерных оксидов Основные С кислотами: ZnO + 2НСl → ZnСl2 + Н2О С кислотными оксидами: ZnO+ SiO2 = ZnSiO3 Кислотные С основаниями: ZnO + 2NaОН = Na2ZnO2 +Н2О С основными оксидами: ZnO + MgО = MgZnO2
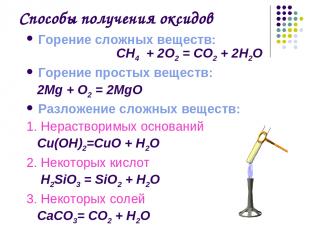
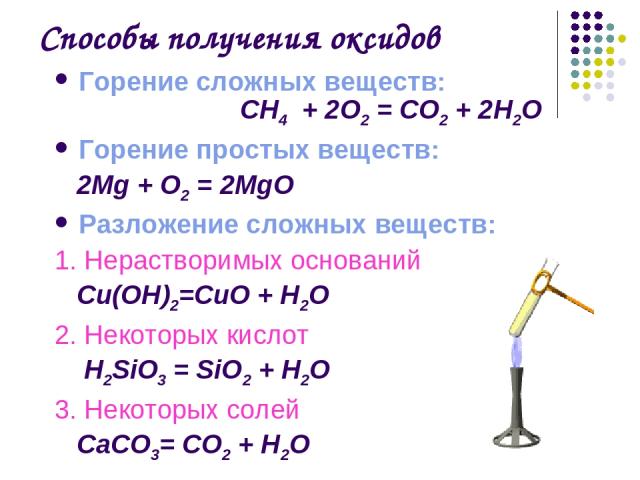
Способы получения оксидов Горение сложных веществ: СН4 + 2О2 = СО2 + 2Н2О Горение простых веществ: 2Mg + О2 = 2MgО Разложение сложных веществ: 1. Нерастворимых оснований Cu(OН)2=CuО + H2O 2. Некоторых кислот H2SiO3 = SiO2 + H2O 3. Некоторых солей СаСО3= СО2 + Н2О