Презентация на тему: 9 класс металлы

Что общего между этими предметами? 900igr.net

Учебное пособие для 9 класса
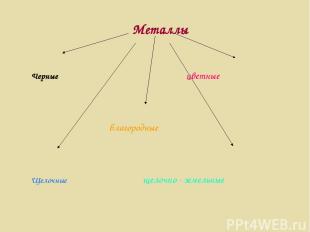
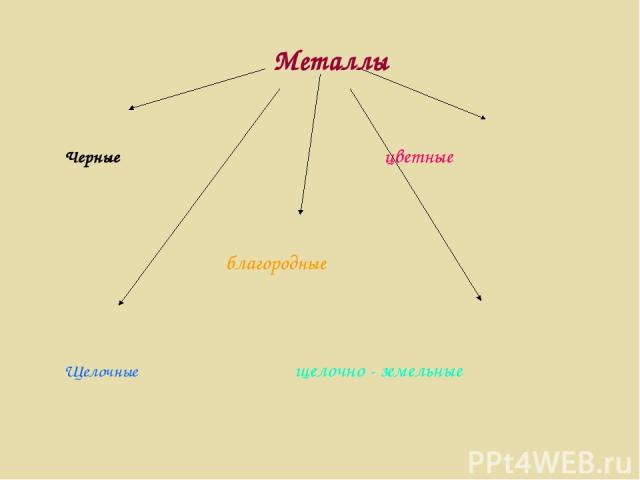
Металлы Черные цветные благородные Щелочные щелочно - земельные
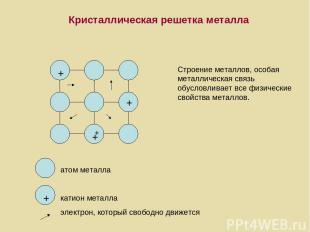
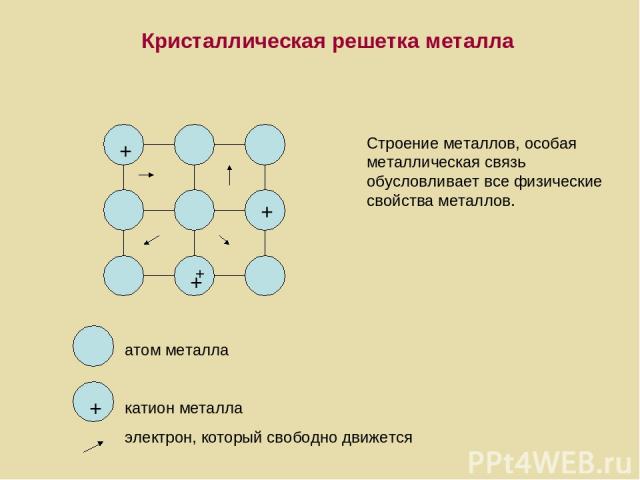
+ + + + + Кристаллическая решетка металла Строение металлов, особая металлическая связь обусловливает все физические свойства металлов. атом металла катион металла электрон, который свободно движется

Физические свойства металлов Металлический блеск Ковкость Пластичность Постоянная температура плавления Электропроводность Теплопроводность

САМЫЙ, САМЫЙ, САМЫЙ. . . Самый блестящий металл … ? Самый твердый металл… ? Самый тугоплавкий металл… ? Самый легкоплавкий металл… ? Самый пластичный металл… ? Самый электропроводный металл… ? Самый тяжелый металл… ? Самый легкий металл…? Жидкий металл… ? Благородный металл… ? Один из главных металлов…? Ag Fe Cu W Au Os Hg Li Cr

Особенности в строении атомов металлов: На внешней оболочке 1-3 электрона, редко 4. Имеют относительно большие радиусы. В химических реакциях электроны отдают, Металлы являются восстановителями, а сами при этом окисляются. Na – 1e- = Na+ Ca – 2e- = Ca2+ Al – 3 e- = Al3+

МЕТАЛЛЫ ВЗАИМОДЕЙСТВУЮТ: С КИСЛОТАМИ Zn + H2SO4 = ZnSO4 + H2 С НЕМЕТАЛЛАМИ 2Cu + O2 = 2CuO 2Al + 3S = Al2S3 6Na + N2 = 2Na3N С ВОДОЙ И С СОЛЯМИ, НО ПРИ ЭТОМ НАДО УЧИТЫВАТЬ МЕСТО НУЖНОГО ВАМ МЕТАЛЛА В РЯДУ НАПРЯЖЕНИЙ МЕТАЛЛОВ (БЕКЕТОВ Н.Н.)