Презентация на тему: Гидролиз. Гидролиз органических и неорганических веществ

Гидролиз. Гидролиз органических и неорганических веществ УЧИТЕЛЬ ХИМИИ: МАКАРКИНА М.А.

Гидролиз ( от древне греческого «ὕδωρ»— вода и «λύσις» — разложение) — один из видов химических реакций, где при взаимодействии веществ с водой происходит разложение исходного вещества с образованием новых соединений. Механизм гидролиза соединений различных классов: - соли, углеводы, жиры, сложные эфиры и др. имеет существенные различия

Гидролиз органических веществЖивые организмы осуществляют гидролиз различных органических веществ в ходе реакций при участии ФЕРМЕНТОВ.Например, в ходе гидролиза при участии пищеварительных ферментов БЕЛКИ расщепляются на АМИНОКИСЛОТЫ, ЖИРЫ — на ГЛИЦЕРИН и ЖИРНЫЕ КИСЛОТЫ, ПОЛИСАХАРИДЫ ( например, крахмал и целлюлоза) — на МОНОСАХАРИДЫ (например, на ГЛЮКОЗУ ),НУКЛЕИНОВЫЕ КИСЛОТЫ — на свободные НУКЛЕОТИДЫ. При гидролизе жиров в присутствии щёлочей получают мыло; гидролиз жиров в присутствии катализаторов применяется для получения глицерина и жирных кислот. Гидролизом древесины получают этанол, а продукты гидролиза торфа находят применение в производстве кормовых дрожжей, воска, удобрений и др.

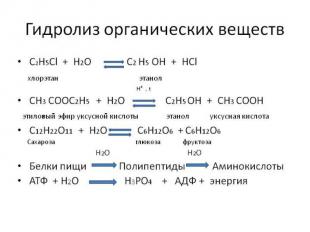
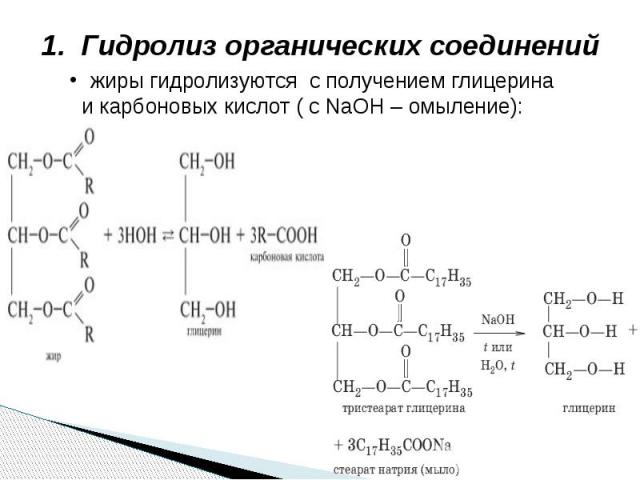
1. Гидролиз органических соединений жиры гидролизуются с получением глицерина и карбоновых кислот ( с NaOH – омыление):

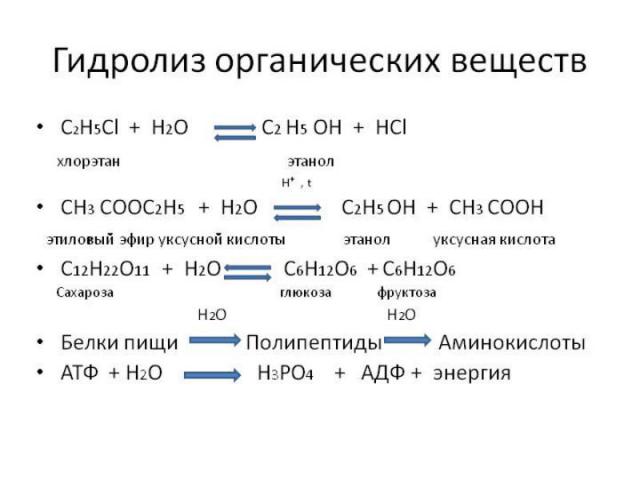
крахмал и целлюлоза гидролизуются до глюкозы:

ТЕСТ 1. При гидролизе жиров образуются 1) спирты и минеральные кислоты 2) альдегиды и карбоновые кислоты3) одноатомные спирты и карбоновые кислоты 4) глицерин и карбоновые кислоты 2. Гидролизу подвергается:Ацетилен 2) Целлюлоза 3) Этанол 4) Метан 3. Гидролизу подвергается:Глюкоза 2) Глицерин 3) Жир 4) Уксусная кислота

4. При гидролизе сложных эфиров образуются: 1) Спирты и альдегиды 2) Карбоновые кислоты и глюкоза 3) Крахмал и глюкоза 4) Спирты и карбоновые кислоты 5. При гидролизе крахмала получается: 1) Сахароза 2) Фруктоза 3) Мальтоза 4) Глюкоза

2. Обратимый и необратимый гидролиз Почти все рассмотренные реакции гидролиза органических веществобратимы. Но есть и необратимый гидролиз. Общее свойство необратимого гидролиза - один ( лучше оба) изпродуктов гидролиза должен быть удален из сферы реакции в виде: - ОСАДКА , - ГАЗА. СаС₂ + 2Н₂О = Са(ОН)₂↓ + С₂Н₂↑ При гидролизе солей: Al₄C₃ + 12 H₂O = 4 Al(OH)₃↓ + 3CH₄↑ Al₂S₃ + 6 H₂O = 2 Al(OH)₃↓ + 3 H₂S↑ CaH₂ + 2 H₂O = 2Ca(OH)₂↓ + H₂↑

Г И Д Р О Л И З С О Л Е Й Гидролиз солей — разновидность реакций гидролиза, обусловленного протеканием реакций ионного обмена в растворах (водных) растворимых солей-электролитов. Движущей силой процесса является взаимодействие ионов с водой, приводящее к образованию слабого электролита в ионном или молекулярном виде («связывание ионов»).Различают обратимый и необратимый гидролиз солей. 1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону). 2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону). 3. Гидролиз соли слабой кислоты и слабого основания (необратимый) Соль сильной кислоты и сильного основания не подвергается гидролизу

1. Гидролиз соли слабой кислоты и сильного основания (гидролиз по аниону): (раствор имеет щелочную среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени) 2. Гидролиз соли сильной кислоты и слабого основания (гидролиз по катиону): (раствор имеет кислую среду, реакция протекает обратимо, гидролиз по второй ступени протекает в ничтожной степени)

3. Гидролиз соли слабой кислоты и слабого основания: (равновесие смещено в сторону продуктов, гидролиз протекает практически полностью, так как оба продукта реакции уходят из зоны реакции в виде осадка или газа).Соль сильной кислоты и сильного основания не подвергает-ся гидролизу, и раствор нейтрален.

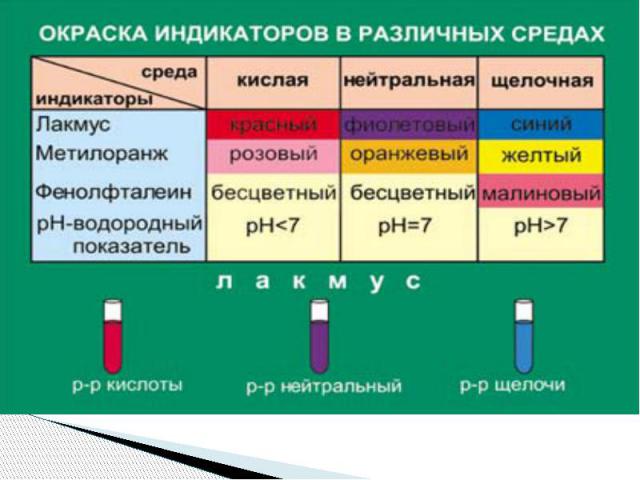
СХЕМА ГИДРОЛИЗА КАРБОНАТА НАТРИЯ Na₂CO₃ ↙ ↘ NaOH H₂CO₃ сильное основание слабая кислота [OH]⁻ > [H]⁺ ЩЕЛОЧНАЯ СРЕДА СОЛЬ КИСЛАЯ, гидролиз по АНИОНУ
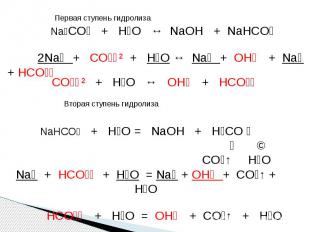
Na₂CO₃ + H₂O ↔ NaOH + NaHCO₃ 2Na⁺ + CO₃⁻² + H₂O ↔ Na⁺ + OH⁻ + Na⁺ + HCO₃⁻ CO₃⁻² + H₂O ↔ OH⁻ + HCO₃⁻ Вторая ступень гидролиза NaHCO₃ + H₂O = NaOH + H₂CO ₃ ↙ ↘ CO₂↑ H₂ONa⁺ + HCO₃⁻ + H₂O = Na⁺ + OH⁻ + CO₂↑ + H₂O HCO₃⁻ + H₂O = OH⁻ + CO₂↑ + H₂O
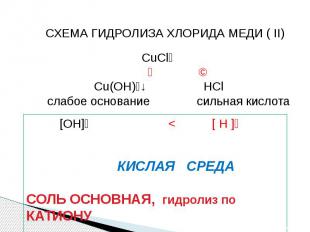
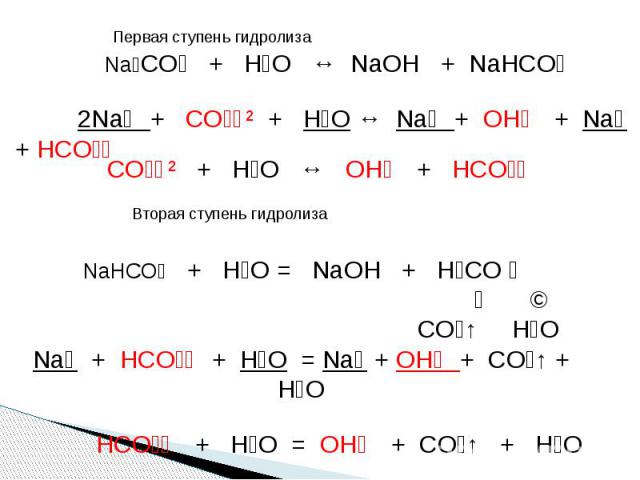
СХЕМА ГИДРОЛИЗА ХЛОРИДА МЕДИ ( II) CuCl₂ ↙ ↘ Cu(OH)₂↓ HCl слабое основание сильная кислота [OH]⁻ < [ H ]⁺ КИСЛАЯ СРЕДАСОЛЬ ОСНОВНАЯ, гидролиз по КАТИОНУ
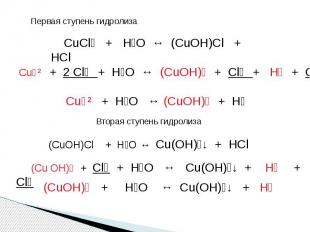
Первая ступень гидролиза CuCl₂ + H₂O ↔ (CuOH)Cl + HCl Cu⁺² + 2 Cl⁻ + H₂O ↔ (CuOH)⁺ + Cl⁻ + H⁺ + Cl⁻ Cu⁺² + H₂O ↔ (CuOH)⁺ + H⁺ Вторая ступень гидролиза (СuOH)Cl + H₂O ↔ Cu(OH)₂↓ + HCl (Cu OH)⁺ + Cl⁻ + H₂O ↔ Cu(OH)₂↓ + H⁺ + Cl⁻ (CuOH)⁺ + H₂O ↔ Cu(OH)₂↓ + H⁺

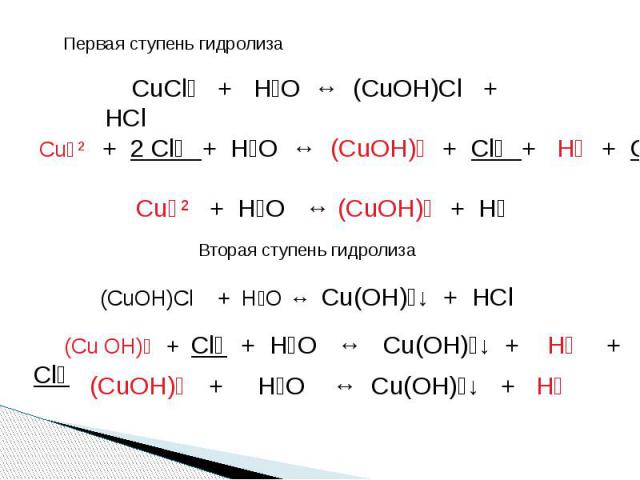
СХЕМА ГИДРОЛИЗА СУЛЬФИДА АЛЮМИНИЯ Al₂S₃ ↙ ↘ Al(OH)₃↓ H₂S↑ слабое основание слабая кислота [OH]⁻ = [H]⁺НЕЙТРАЛЬНАЯ РЕАКЦИЯ СРЕДЫ гидролиз необратимый
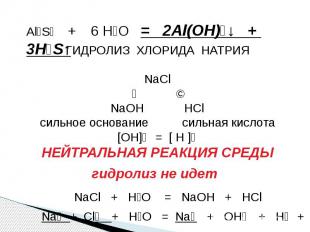
Al₂S₃ + 6 H₂O = 2Al(OH)₃↓ + 3H₂S↑ ГИДРОЛИЗ ХЛОРИДА НАТРИЯNaCl↙ ↘NaOH HClсильное основание сильная кислота[OH]⁻ = [ H ]⁺НЕЙТРАЛЬНАЯ РЕАКЦИЯ СРЕДЫ гидролиз не идет NaCl + H₂O = NaOH + HCl Na⁺ + Cl⁻ + H₂O = Na⁺ + OH⁻ + H⁺ + Cl⁻

РОЛЬ ГИДРОЛИЗА В ПРИРОДЕ Преобразование земной корыОбеспечение слабощелочной среды морской воды РОЛЬ ГИДРОЛИЗА В ЖИЗНИ ЧЕЛОВЕКАСтирка Умывание с мыломМытье посуды Процессы пищеварения
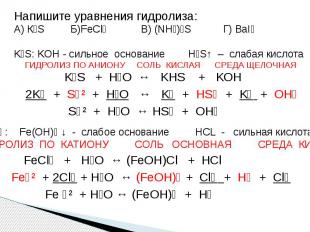
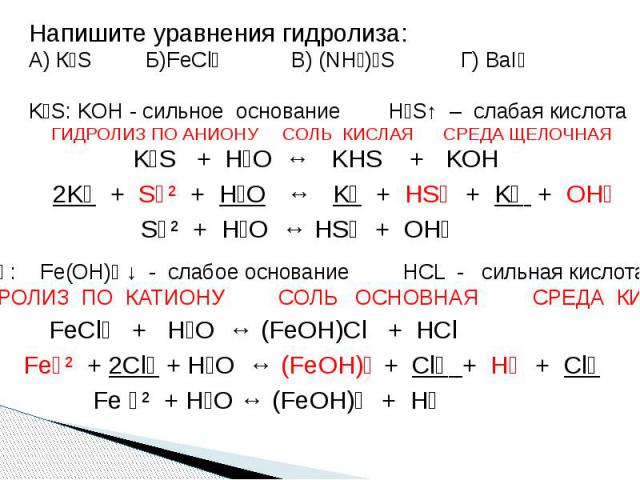
Напишите уравнения гидролиза:А) К₂S Б)FeCl₂ В) (NH₄)₂S Г) BaI₂ K₂S: KOH - сильное основание H₂S↑ – слабая кислота ГИДРОЛИЗ ПО АНИОНУ СОЛЬ КИСЛАЯ СРЕДА ЩЕЛОЧНАЯ K₂S + H₂O ↔ KHS + KOH 2K⁺ + S⁻² + H₂O ↔ K⁺ + HS⁻ + K⁺ + OH⁻ S⁻² + H₂O ↔ HS⁻ + OH⁻ FeCl₂ : Fe(OH)₂ ↓ - слабое основание HCL - сильная кислота ГИДРОЛИЗ ПО КАТИОНУ СОЛЬ ОСНОВНАЯ СРЕДА КИСЛАЯ FeCl₂ + H₂O ↔ (FeOH)Cl + HCl Fe⁺² + 2Cl⁻ + H₂O ↔ (FeOH)⁺ + Cl⁻ + H⁺ + Cl⁻ Fe ⁺² + H₂O ↔ (FeOH)⁺ + H⁺
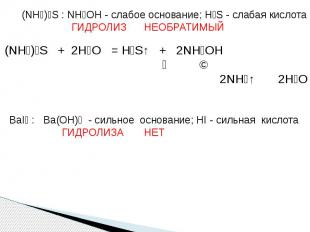
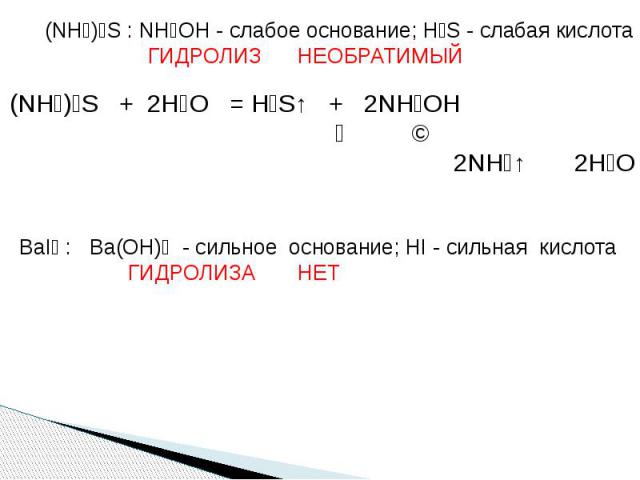
(NH₄)₂S : NH₄OH - слабое основание; H₂S - слабая кислота ГИДРОЛИЗ НЕОБРАТИМЫЙ (NH₄)₂S + 2H₂O = H₂S↑ + 2NH₄OH ↙ ↘ 2NH₃↑ 2H₂O BaI₂ : Ba(OH)₂ - сильное основание; HI - сильная кислота ГИДРОЛИЗА НЕТ



7. Водный раствор какой из солей имеет нейтральную среду? а) Al(NO₃)₃ б) ZnCl₂ в) BaCl₂ г) Fe(NO₃)₂ 8. В каком растворе цвет лакмуса будет синим? а) Fe₂(SO₄)₃ б) K₂S в) CuCl₂ г) (NH₄)₂SO₄

9. Гидролизу не подвергаются 1) карбонат калия 2) этан 3) хлорид цинка 4) жир 10. При гидролизе клетчатки ( крахмала ) могут образовываться:1) глюкоза 2) только сахароза 3) только фруктоза 4) углекислый газ и вода 11. Среда раствора в результате гидролиза карбоната натрия1) щёлочная 2) сильно кислая 3) кислая 4) нейтральная 12. Гидролизу подвергается 1) CH3COOK 2) KCI 3) CaCO3 4)Na2SO4 ОТВЕТ: 9 - 2; 10 - 1; 11 - 1; 12 - 1

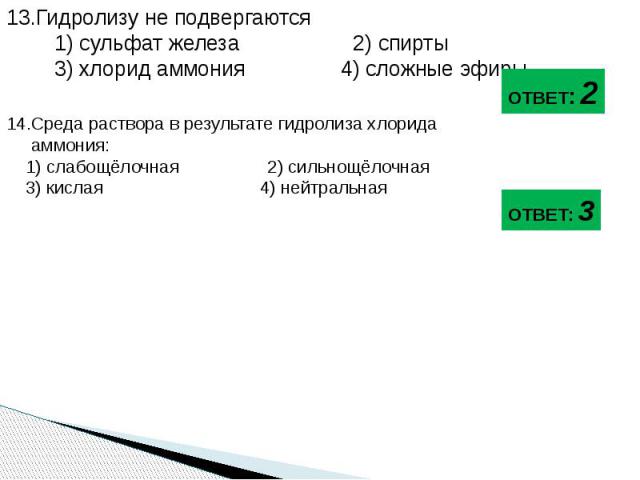
13.Гидролизу не подвергаются 1) сульфат железа 2) спирты 3) хлорид аммония 4) сложные эфиры 14.Среда раствора в результате гидролиза хлорида аммония: 1) слабощёлочная 2) сильнощёлочная 3) кислая 4) нейтральная

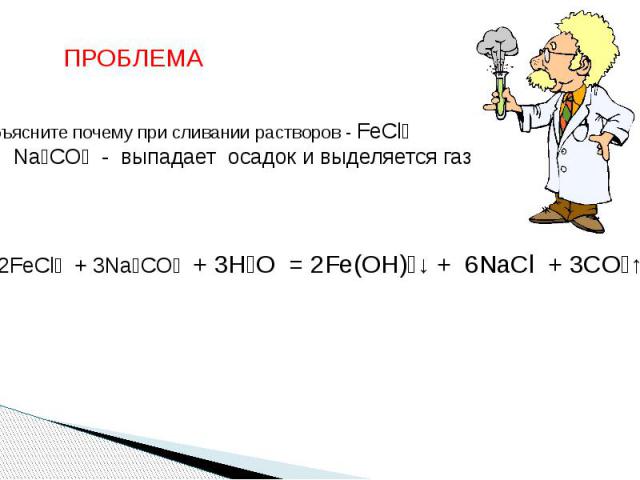
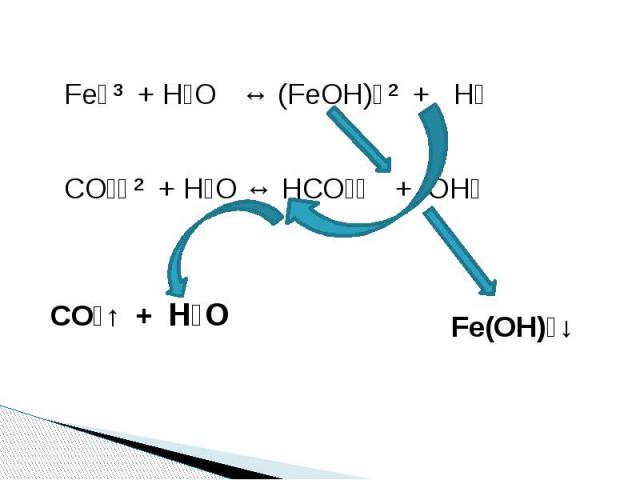
ПРОБЛЕМА Объясните почему при сливании растворов - FeCl₃ и Na₂CO₃ - выпадает осадок и выделяется газ? 2FeCl₃ + 3Na₂CO₃ + 3H₂O = 2Fe(OH)₃↓ + 6NaCl + 3CO₂↑
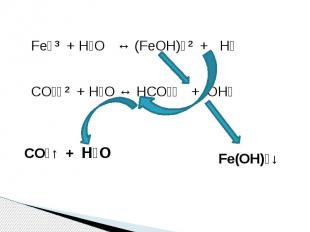
Fe⁺³ + H₂O ↔ (FeOH)⁺² + H⁺CO₃⁻² + H₂O ↔ HCO₃⁻ + OH⁻ CO₂↑ + H₂O Fe(OH)₃↓











![СХЕМА ГИДРОЛИЗА КАРБОНАТА НАТРИЯ Na₂CO₃ ↙ ↘ NaOH H₂CO₃ сильное основание слабая кислота [OH]⁻ > [H]⁺ ЩЕЛОЧНАЯ СРЕДА СОЛЬ КИСЛАЯ, гидролиз по АНИОНУ СХЕМА ГИДРОЛИЗА КАРБОНАТА НАТРИЯ Na₂CO₃ ↙ ↘ NaOH H₂CO₃ сильное основание слабая кислота [OH]⁻ > [H]⁺ ЩЕЛОЧНАЯ СРЕДА СОЛЬ КИСЛАЯ, гидролиз по АНИОНУ](https://fs1.ppt4web.ru/images/5418/71238/640/img13.jpg)
![СХЕМА ГИДРОЛИЗА ХЛОРИДА МЕДИ ( II) CuCl₂ ↙ ↘ Cu(OH)₂↓ HCl слабое основание сильная кислота [OH]⁻ < [ H ]⁺ КИСЛАЯ СРЕДАСОЛЬ ОСНОВНАЯ, гидролиз по КАТИОНУ СХЕМА ГИДРОЛИЗА ХЛОРИДА МЕДИ ( II) CuCl₂ ↙ ↘ Cu(OH)₂↓ HCl слабое основание сильная кислота [OH]⁻ < [ H ]⁺ КИСЛАЯ СРЕДАСОЛЬ ОСНОВНАЯ, гидролиз по КАТИОНУ](https://fs1.ppt4web.ru/images/5418/71238/640/img15.jpg)
![СХЕМА ГИДРОЛИЗА СУЛЬФИДА АЛЮМИНИЯ Al₂S₃ ↙ ↘ Al(OH)₃↓ H₂S↑ слабое основание слабая кислота [OH]⁻ = [H]⁺НЕЙТРАЛЬНАЯ РЕАКЦИЯ СРЕДЫ гидролиз необратимый СХЕМА ГИДРОЛИЗА СУЛЬФИДА АЛЮМИНИЯ Al₂S₃ ↙ ↘ Al(OH)₃↓ H₂S↑ слабое основание слабая кислота [OH]⁻ = [H]⁺НЕЙТРАЛЬНАЯ РЕАКЦИЯ СРЕДЫ гидролиз необратимый](https://fs1.ppt4web.ru/images/5418/71238/640/img17.jpg)
![Al₂S₃ + 6 H₂O = 2Al(OH)₃↓ + 3H₂S↑ ГИДРОЛИЗ ХЛОРИДА НАТРИЯNaCl↙ ↘NaOH HClсильное основание сильная кислота[OH]⁻ = [ H ]⁺НЕЙТРАЛЬНАЯ РЕАКЦИЯ СРЕДЫ гидролиз не идет NaCl + H₂O = NaOH + HCl Na⁺ + Cl⁻ + H₂O = Na⁺ + OH⁻ + H⁺ + Cl⁻ Al₂S₃ + 6 H₂O = 2Al(OH)₃↓ + 3H₂S↑ ГИДРОЛИЗ ХЛОРИДА НАТРИЯNaCl↙ ↘NaOH HClсильное основание сильная кислота[OH]⁻ = [ H ]⁺НЕЙТРАЛЬНАЯ РЕАКЦИЯ СРЕДЫ гидролиз не идет NaCl + H₂O = NaOH + HCl Na⁺ + Cl⁻ + H₂O = Na⁺ + OH⁻ + H⁺ + Cl⁻](https://fs1.ppt4web.ru/images/5418/71238/640/img18.jpg)