Презентация на тему: Свойства кислот

Тема: «Кислоты» 8 класс

H Cl = H+ + Cl – H2 SO 4 = 2 H+ + SO42- Кислоты – это электролиты, которые при диссоциации образуют катионы водорода и анионы кислотного остатка. Что такое кислоты? Кислотами называют сложные вещества, молекулы которых состоят из атомов водорода, способных замещаться на атомы металлов, и кислотных остатков.

Состав кислот H Cl H2SO4 H3PO4 1. Кислоты – это простые или сложные вещества? 2. Что общего в составе кислот? 3. Сформулируйте определение данного класса.
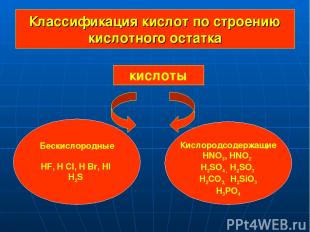
Классификация кислот по строению кислотного остатка кислоты Бескислородные HF, H Cl, H Br, HI H2S Кислородсодержащие HNO3, HNO2 H2SO4 , H2SO3 H2CO3, H2SiO3 H3PO4

Нахождение кислот в природе Лимонная кислота содержится в лимонах, яблочная кислота - в яблоках, щавелевая кислота - в листьях щавеля. В пчелином яде, в волосках крапивы, в иголках сосны и ели содержится муравьиная кислота. Муравьи, защищаясь от врагов, разбрызгивают капельки муравьиной кислоты. При скисании виноградного сока и молока, при квашении капусты образуется молочная кислота.

Физические свойства Жидкости, неограниченно смешивающиеся с водой: H2SO4, HNO3, HCI и др. Твёрдые вещества, растворимые в воде: H3PO4, HPO3 Нерастворимая в воде H2SiO3

Правила техники безопасности при работе с кислотами При растворении серной кислоты нужно вливать ее тонкой струей в воду и перемешивать !!! H2SO4 Н2О С растворами кислот надо обращаться осторожно, при попадании на кожу или одежду данных веществ - промыть большим количеством воды

Действие кислот на растворы индикаторов фиолетовый красный оранжевый розовый лакмус метилоранж обусловлено наличием в них ионов Н +

Взаимодействие кислот с металлами металл + кислота = соль + водород Zn HCl H 2
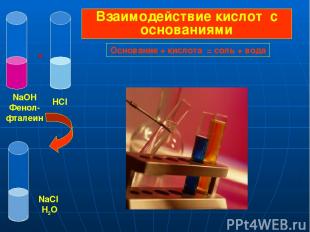
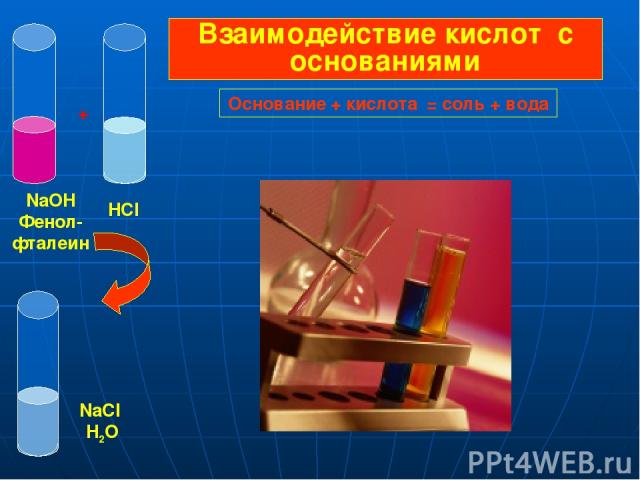
NaOH Фенол- фталеин HCl + NaCl H2O Взаимодействие кислот с основаниями Основание + кислота = соль + вода

основный оксид + кислота = соль + вода Взаимодействие кислот с основными и амфотерными оксидами Cu O H2SO4 Cu SO 4 H2O
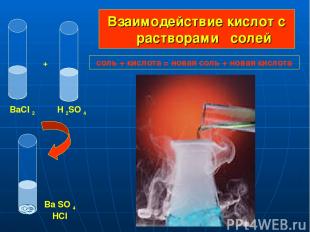
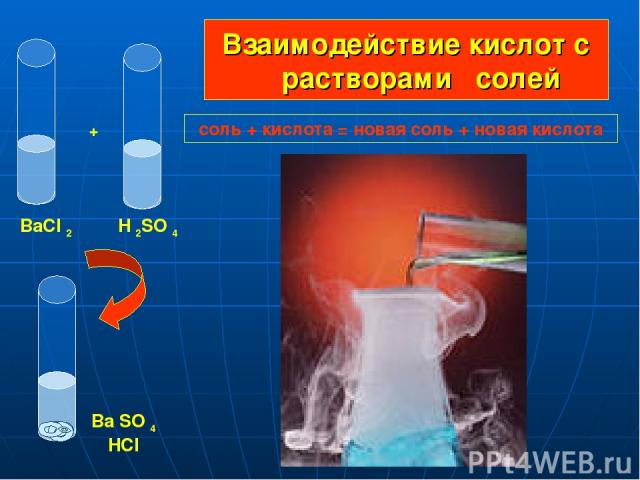
Взаимодействие кислот с растворами солей + BaCI 2 H 2SO 4 Ba SO 4 HCI соль + кислота = новая соль + новая кислота

H2CO3 = H2O + CO2 H2SO3 = H2O + SO2 H2SiO3 = H2O + SiO2 CO2 H 2CO 3 Разложение кислот Некоторые кислоты разлагаются при н.у. или при нагревании:

Способы получения кислот 1. Взаимодействие кислотных оксидов с водой: 2. Взаимодействие водорода с соответствующим неметаллом: