Презентация на тему: Свойства железа

Тема урока: Железо: строение атома, физические и химические свойства. Генетические ряды железа (II) и железа (III). Презентацию подготовила учитель l квалификационной категории МОУ Шуваевской ООШ Тропынёва Е.М. 900igr.net

"Третий лишний» Задание: Решите анаграммы и исключите лишнее. леруогд иксолодр ддрооов золеже

Проверь себя!

Положение железа в Периодической системе химических элементов Д.И. Менделеева. - Определите положение железа в Периодической системе химических элементов Д.И. Менделеева.

Запомни! Особенностью электронного строения элементов побочных подгрупп является заполнение электронами не последнего, а предпоследнего уровня.

Строение атома железа. Задание: Закончите электронно - буквенную формулу и нарисуйте графическую формулу строения атома железа:1s22s22p63s23p63d6….

Строение атома железа Нормальное состояние атома железа 3d6 4p0 4s2 1 возбужденное состояние атома железа 3d5 4p1 4s2 2 возбужденное состояние атома железа 3d5 4p2 4s2

Степени окисления железа Для железа характерны две основные степени окисления: +2, +3. Fe0 –2e – Fe+2 Fe0 –3e – Fe+3 Магнетит

Физические свойства: Задание: Рассмотрите образец выданного вам металла. Опишите его физические свойства, используя текст учебника 1. Цвет 2. Блеск 3. Пластичность 4. Магнитные свойства 5. Температура плавления 6. Твердость Гематит

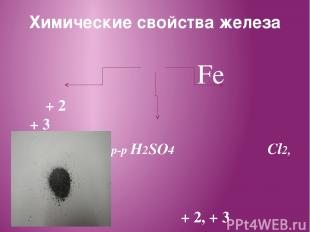
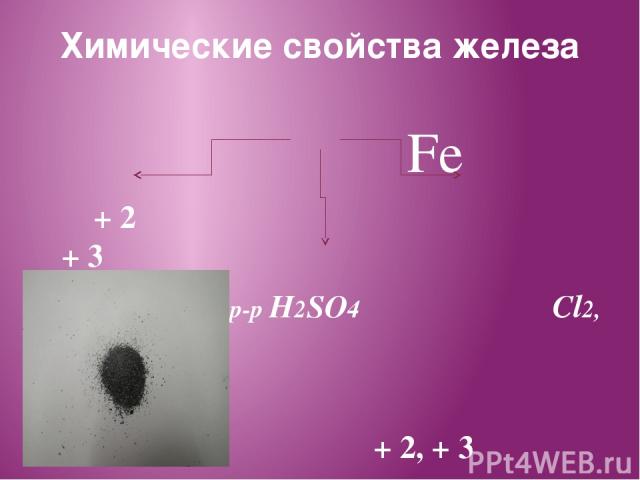
Химические свойства железа Fe + 2 + 3 S, Сu,р-р HCl, р-р H2SO4 Cl2, HNO3 + 2, + 3 O2, H2O

Химические свойства железа Степень окисления Fe зависит от окислительной способности реагирующего вещества. У сильных окислителей железо принимает степень окисления +3, у более слабых +2.

Химические свойства: Задание: Закончить уравнения химических реакций, демонстрирующих химические свойства железа 1) Fe + CI2 = 2) Fe + S = 3) Fe + HCI = Железный метеорит 4) Fe + O2 = 5) Fe + CuSO4 = 6) Fe + H2O = 7) Fe + O2 + H2O =

Какие из реакций соответствуют схеме: Fe+2 Fe+3 FeCI2 + CI2 = FeCI3 FeCI3 + NaOH =Fe(OH)3 + 3NaCI Fe(OH)2 + O2 + H2O = Fe(OH)3 «Лови ошибку!» - Что неправильно записано в уравнениях?

Верно только уравнение 2 Задание: Расставить коэффициенты в уравнениях 1 и 3 методом электронного баланса, определить окислитель и восстановитель в реакции.

Соединения железа: Fe3O4 – магнитный железняк Fe2O3 – красный железняк (гематит) 2Fe2O3 * 3H2O – бурый железняк FeS2 – железный колчедан Железо – второй по распространенности металл в земной коре. В природе встречается в виде оксидов и сульфидов

Лабораторная работа Задание: Рассмотреть образцы соединений железа, отметить основные их характеристики. Горение железа в кислороде

Выводы: Железо в природе находится в виде соединений: руд и минералов, а самородное железо встречается очень редко. Соединения железа (II) имеют ярко выраженный основный характер. Соединения железа (III) – проявляют амфотерные свойства.

«Конструирование текста» Задание: Из предложенных формул соединений составьте генетический ряд Fe+2 (для первого варианта) и генетический ряд Fe+3 (для второго варианта). Fe(OH)3 , Fe, Fe(OH)2 , FeCI3 , Fe2O3 , FeCI2 , FeO. Получение пирофорного железа из оксалата.

Проверим! Генетические ряды Fe+2, Fe+3. 1) Fe FeCI2 Fe(OH)2 FeO Fe FeCI3 Fe(OH)3 Fe2O3 Хлорид железа(l l ) (слева) Хлорид железа ( lll ) (справа).
![Качественная реакция на ион Fe+2 Реактив – красная кровяная сольK3[Fe(CN)6] Резу Качественная реакция на ион Fe+2 Реактив – красная кровяная сольK3[Fe(CN)6] Резу](https://fs3.ppt4web.ru/images/132073/183886/310/img20.jpg)
Качественная реакция на ион Fe+2 Реактив – красная кровяная сольK3[Fe(CN)6] Результат воздействия – синий осадок (турнбуленовой сини) K3[Fe(CN)6] + FeCI2 = 2KCI + KFe[Fe(CN)6] 3K+ + Fe2+ + 2CI- + [Fe(CN)6]3- → KFe[Fe(CN)6] + 2K+ + 2CI- K+ + Fe2+ + [Fe(CN)6]3- → KFe[Fe(CN)6] Красная кровяная соль
![Качественная реакция на ион Fe+3 1) Реактив – желтая кровяная сольK4[Fe(CN)6] Ре Качественная реакция на ион Fe+3 1) Реактив – желтая кровяная сольK4[Fe(CN)6] Ре](https://fs3.ppt4web.ru/images/132073/183886/310/img21.jpg)
Качественная реакция на ион Fe+3 1) Реактив – желтая кровяная сольK4[Fe(CN)6] Результат воздействия – синий осадок (берлинской лазури) K4[Fe(CN)6] + FeCI3 = 3KCI + KFe[Fe(CN)6] 4K+ + Fe3+ + 3CI- + [Fe(CN)6]4- → KFe[Fe(CN)6] + 3K+ + 3CI- K+ + Fe3+ + [Fe(CN)6]4-→ KFe[Fe(CN)6] 2) Реактив – роданиднатрия (аммония) NaNCS (NH4NCS) Результат воздействия – интенсивно- красный цвет. FeCI3 + NaNCS = [FeNCS]CI2 + NaCI Fe3+ + NCS- = FeNCS2+ Жёлтая кровяная соль

«Попс – формула»: Задание: Написать вывод урока по образцу, закончив предложения: Сегодня я понял (а), что… Главным на уроке для меня было… Больше всего мне запомнилось…

Спасибо за внимание ! Домашнее задание: §14, упражнение 4 на странице 82. Железный метеорит




















![Качественная реакция на ион Fe+2 Реактив – красная кровяная сольK3[Fe(CN)6] Результат воздействия – синий осадок (турнбуленовой сини) K3[Fe(CN)6] + FeCI2 = 2KCI + KFe[Fe(CN)6] 3K+ + Fe2+ + 2CI- + [Fe(CN)6]3- → KFe[Fe(CN)6] + 2K+ + 2CI- K+ + Fe2+ + [… Качественная реакция на ион Fe+2 Реактив – красная кровяная сольK3[Fe(CN)6] Результат воздействия – синий осадок (турнбуленовой сини) K3[Fe(CN)6] + FeCI2 = 2KCI + KFe[Fe(CN)6] 3K+ + Fe2+ + 2CI- + [Fe(CN)6]3- → KFe[Fe(CN)6] + 2K+ + 2CI- K+ + Fe2+ + […](https://fs3.ppt4web.ru/images/132073/183886/640/img20.jpg)
![Качественная реакция на ион Fe+3 1) Реактив – желтая кровяная сольK4[Fe(CN)6] Результат воздействия – синий осадок (берлинской лазури) K4[Fe(CN)6] + FeCI3 = 3KCI + KFe[Fe(CN)6] 4K+ + Fe3+ + 3CI- + [Fe(CN)6]4- → KFe[Fe(CN)6] + 3K+ + 3CI- K+ + Fe3+ + … Качественная реакция на ион Fe+3 1) Реактив – желтая кровяная сольK4[Fe(CN)6] Результат воздействия – синий осадок (берлинской лазури) K4[Fe(CN)6] + FeCI3 = 3KCI + KFe[Fe(CN)6] 4K+ + Fe3+ + 3CI- + [Fe(CN)6]4- → KFe[Fe(CN)6] + 3K+ + 3CI- K+ + Fe3+ + …](https://fs3.ppt4web.ru/images/132073/183886/640/img21.jpg)