Презентация на тему: обобщение по теме Металлы 9 класс

Обобщение по теме «Металлы» учитель: Лысоконь И.А

Эпиграф «Металлов много есть, но дело не в количестве В команде работящей металлической Такие мастера, такие личности! Преуменьшать нам вовсе не пристало Заслуги безусловные металлов.»

N, Hg, O, H, W, S, Li, Сr, F, Ag Hg, W, Сr, Li, Ag – самый легкий металл; – самый тугоплавкий металл; – жидкий металл; – самый электропроводный металл; – самый твердый металл. Li W Hg Ag Сr

Игра “Чудо – дерево” А у наших у ворот Чудо – дерево растет. Чудо, чудо, чудо, чудо Расчудесное. Не листочки на нем, Не цветочки на нём – Апельсинчики, лимоны, Чудо – яблоки. (К. И Чуковский)
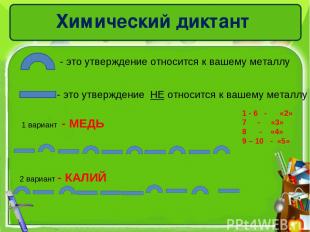
Химический диктант - это утверждение относится к вашему металлу - это утверждение НЕ относится к вашему металлу 1 вариант - МЕДЬ 2 вариант - КАЛИЙ 1 - 6 - «2» - «3» - «4» 9 – 10 - «5»

В ряду левее водорода Среди металлов нет урода: Все растворимы в кислоте, А те, что с краю, и в воде. Зато на правом фланге “знать” Кислот в упор не хочет знать…

Допишите уравнения возможных реакций Zn + H2O = Fe + HCl = Zn + H3PO4 = Cu + H2O = Al + HCl = Pb + H2SO4(разб.) = Ag + HCl = FeCl2 + H2 Zn3(PO4)2 + H2 AlCl3 + H2 PbSO4+ Н2 2 3 2 3 2 3 2 6
3 2 4 5 6 7 8

Варианты ответов: Вариант 1: Вариант 3: Вариант 2: Вариант 4: Вариант 5: в а б г в в а б г в в а б г в в а б г в в а б г в

ДОМАШНЕЕ ЗАДАНИЕ: 1. Написать уравнения раекций: а) Fe – FeO - FeSO4 – Fe б) Ba - BaO → Ba(OH)2 →BaCl2 2. Решить задачу Сколько литров углекислого газа выделится при взаимодействии соляной кислоты с 4г. карбоната кальция, если выход составит 90% от теоретически возможного