Презентация на тему: Химические свойства солей

Соли Химия 8 класс И. Жикина 5klass.net
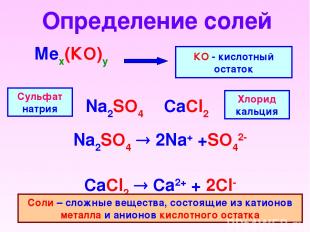
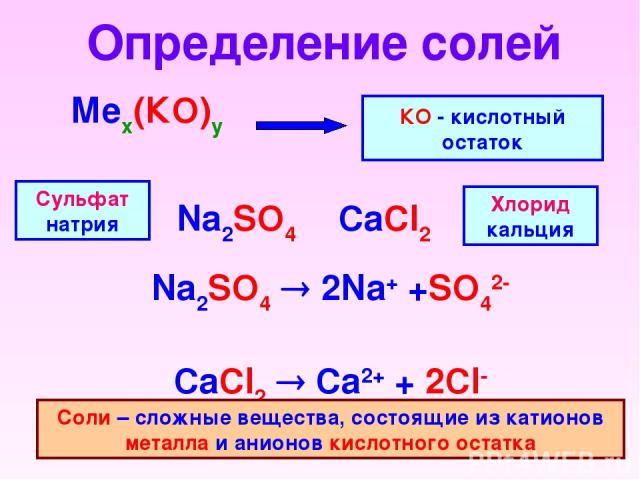
Определение солей Мех(КО)у КО - кислотный остаток Na2SO4 2Na+ +SO42- CaCl2 Ca2+ + 2Cl- Na2SO4 CaCl2 Сульфат натрия Хлорид кальция Соли – сложные вещества, состоящие из катионов металла и анионов кислотного остатка
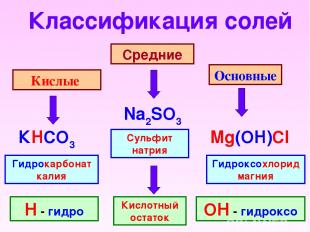
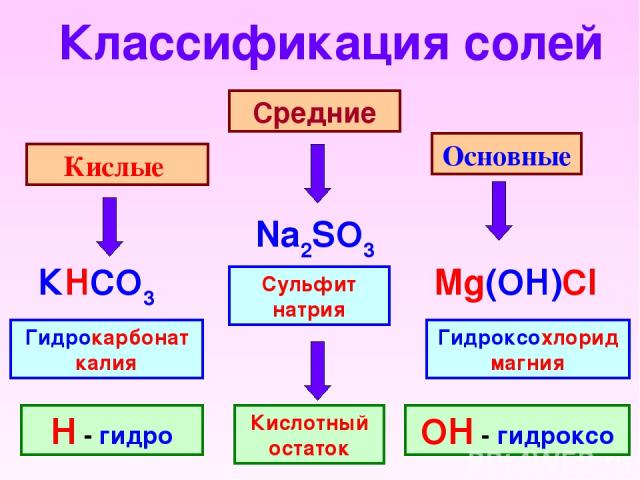
Классификация солей Кислые Средние Основные Na2SO3 КHCO3 Mg(OH)Cl Сульфит натрия Гидроксохлорид магния Гидрокарбонат калия Н - гидро ОН - гидроксо Кислотный остаток
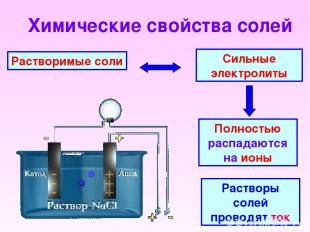
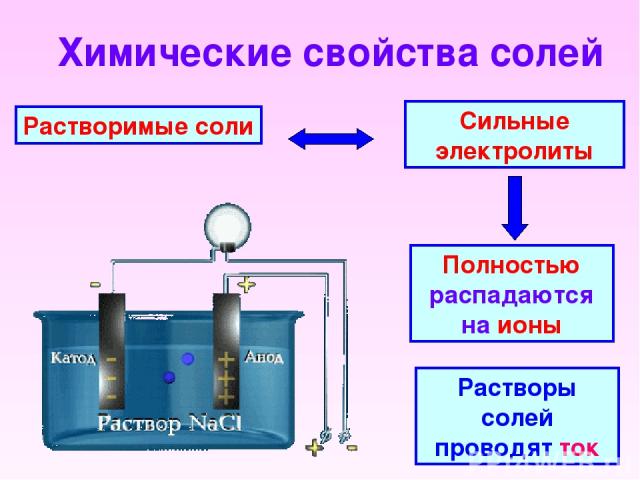
Химические свойства солей Растворимые соли Сильные электролиты Полностью распадаются на ионы Растворы солей проводят ток
Электролиты растворимые Основания Соли Кислоты Реакции в растворах электролитов протекают между ионами Признак реакции Осадок Газ Вода
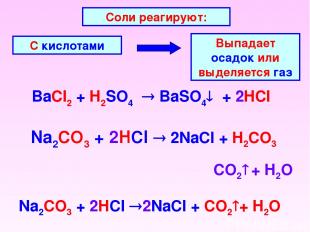
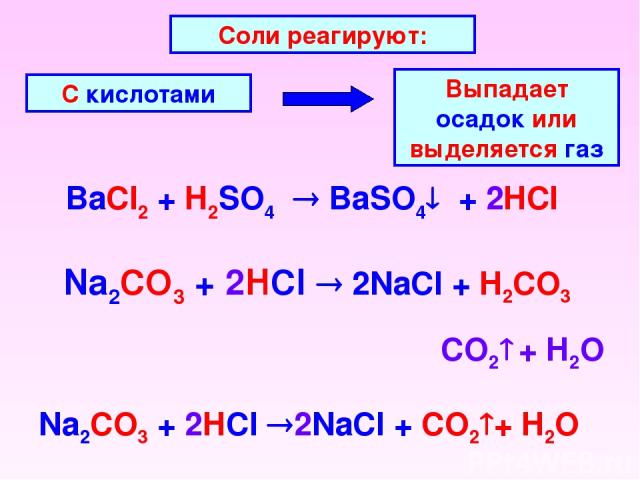
BaCl2 + H2SO4 BaSO4 + 2HCl Соли реагируют: С кислотами Выпадает осадок или выделяется газ Na2CO3 + 2HCl 2NaCl + H2CO3 CO2 + H2O Na2CO3 + 2HCl 2NaCl + CO2 + H2O
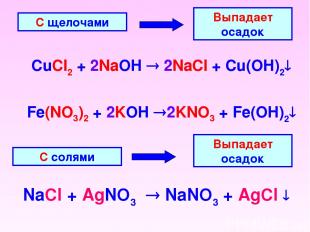
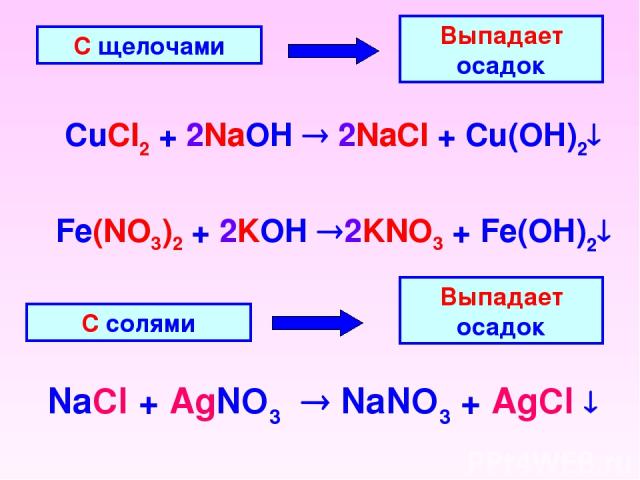
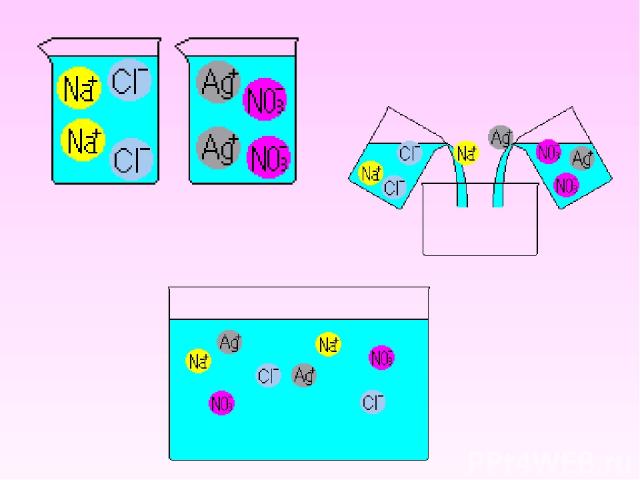
С щелочами Выпадает осадок CuCl2 + 2NaOH 2NaCl + Cu(OH)2 С солями Выпадает осадок NaCl + AgNO3 NaNO3 + AgCl Fe(NO3)2 + 2KOH 2KNO3 + Fe(OH)2
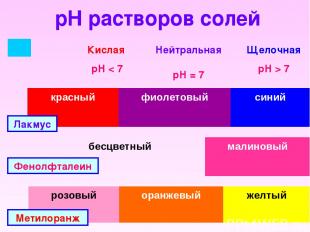
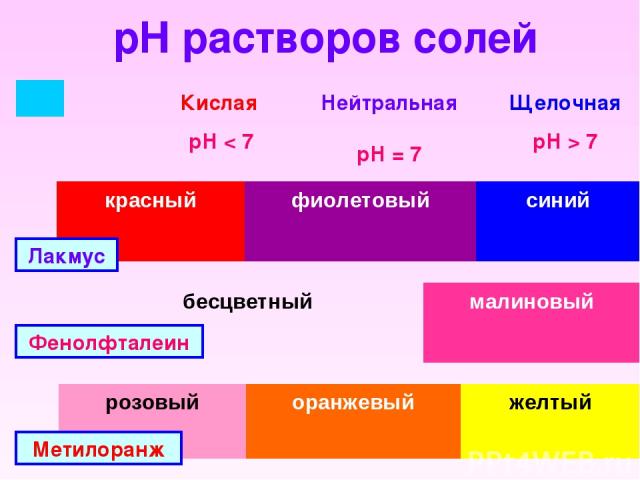
pH растворов солей Лакмус Фенолфталеин Метилоранж Кислая рН < 7 Нейтральная рН = 7 Щелочная рН > 7
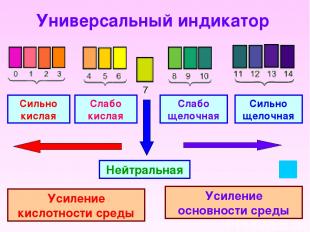
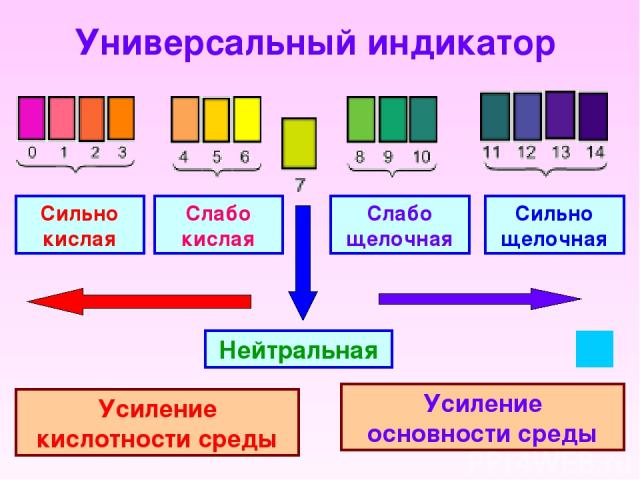
Универсальный индикатор Сильно кислая Слабо кислая Слабо щелочная Сильно щелочная Нейтральная Усиление кислотности среды Усиление основности среды

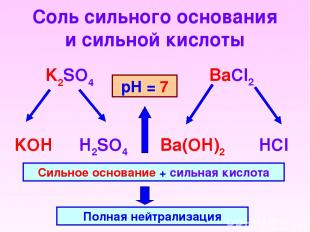
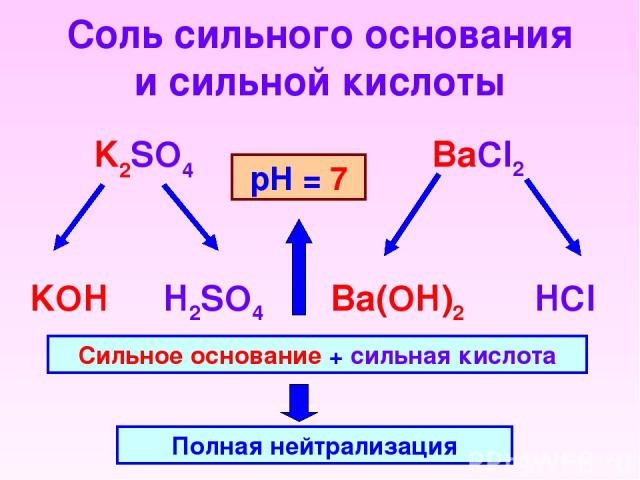
Соль сильного основания и сильной кислоты K2SO4 BaCl2 KOH H2SO4 HCl Ba(OH)2 Сильное основание + сильная кислота Полная нейтрализация рН = 7
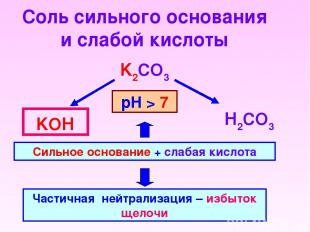
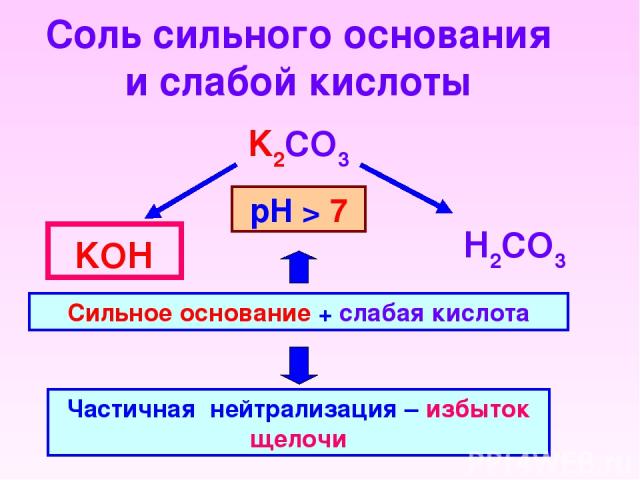
Соль сильного основания и слабой кислоты K2CO3 Н2CO3 KОН Сильное основание + слабая кислота Частичная нейтрализация – избыток щелочи рН > 7
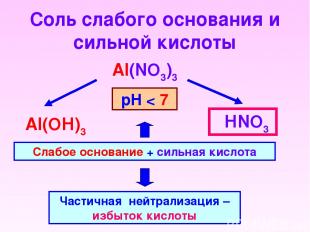
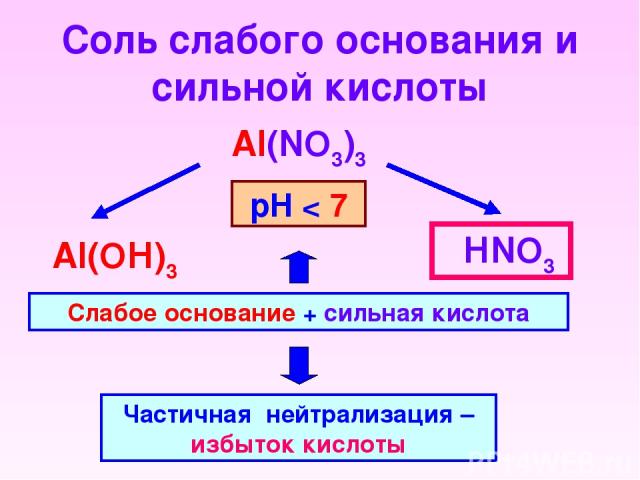
Соль слабого основания и сильной кислоты Al(NO3)3 НNO3 Al(OН)3 Слабое основание + сильная кислота Частичная нейтрализация – избыток кислоты рН < 7
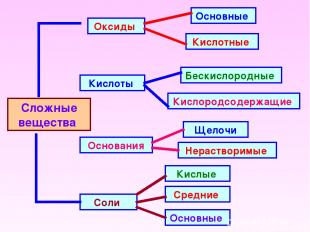
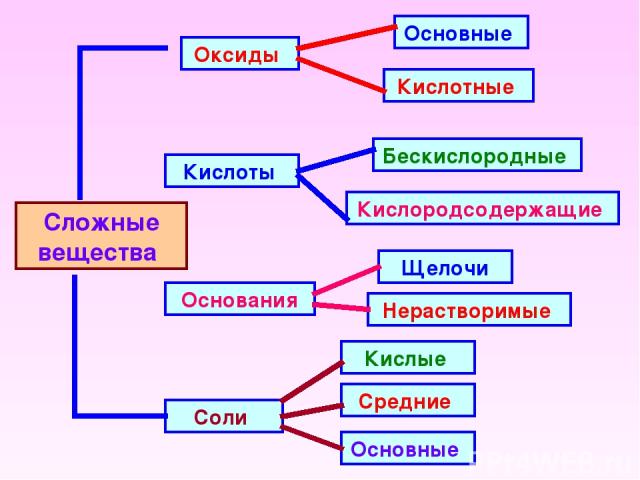
Сложные вещества Оксиды Кислоты Основания Соли Основные Кислотные Кислородсодержащие Бескислородные Щелочи Нерастворимые Основные Средние Кислые
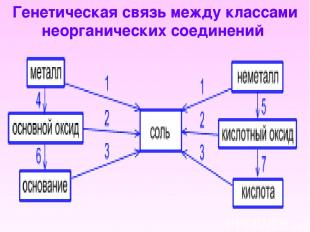
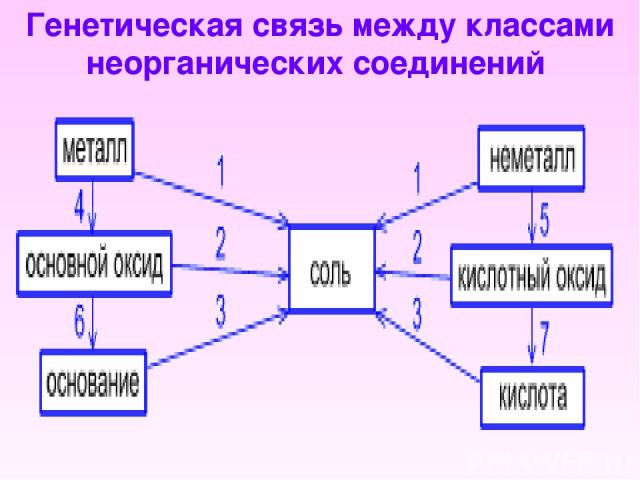
Генетическая связь между классами неорганических соединений

Примеры 1. Металл + неметалл соль Hg + S HgS 2Al + 3I2 2AlI3 2. Основной оксид + кислотный оксид соль Li2O + CO2 Li2CO3 CaO + SiO2 CaSiO3
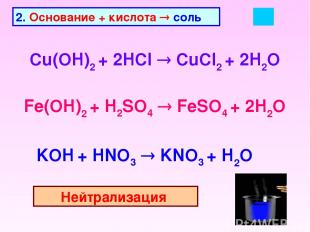
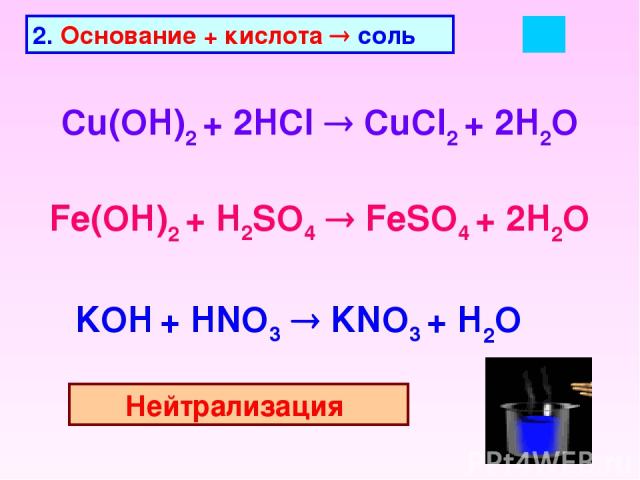
2. Основание + кислота соль Cu(OH)2 + 2HCl CuCl2 + 2H2O Fe(OH)2 + H2SO4 FeSO4 + 2H2O KOH + HNO3 KNO3 + H2O Нейтрализация
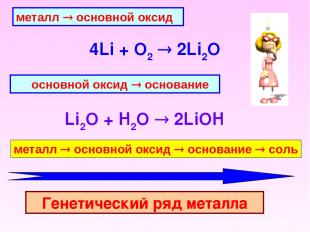
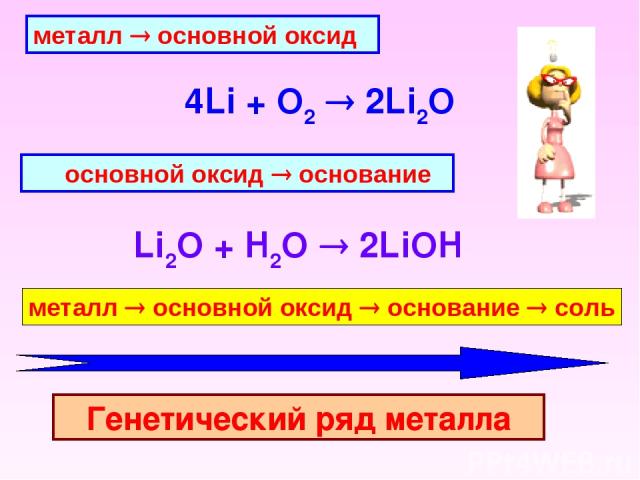
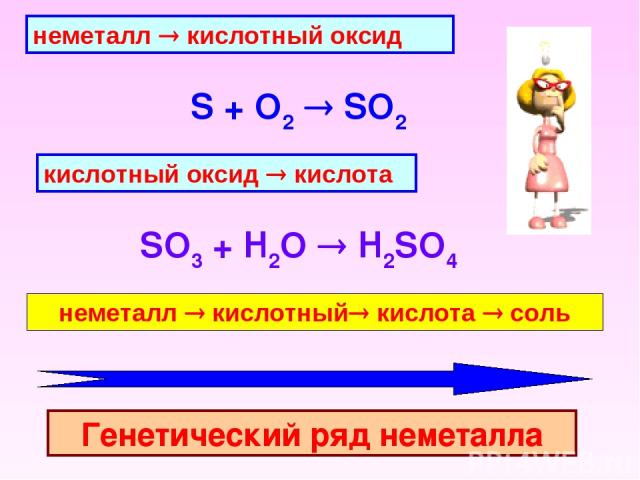
металл ® основной оксид 4Li + O2 2Li2O основной оксид ® основание Li2O + H2O 2LiOH металл ® основной оксид ® основание ® соль Генетический ряд металла
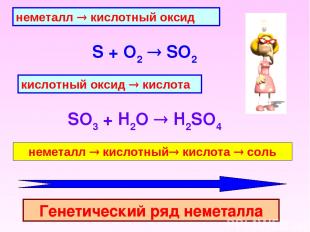
неметалл ® кислотный оксид S + O2 SO2 кислотный оксид ® кислота SO3 + H2O H2SO4 неметалл ® кислотный® кислота ® соль Генетический ряд неметалла