Презентация на тему: Карбоновые кислоты

Карбоновые кислоты 900igr.net

Карбоновые кислоты — класс органических соединений, молекулы которого содержат карбоксильную группу - COOH. Состав предельных одноосновных карбоновых кислот соответствует общей формуле О R – C OH.

Классификация По числу карбоксильных групп карбоновые кислоты делятся на: монокарбоновые или одноосновные (уксусная кислота) дикарбоновые или двухосновные (щавелевая кислота) В зависимости от строения углеводородного радикала, с которым связана карбоксильная группа, карбоновые кислоты делятся на: алифатические ( уксусная или акриловая) алициклические (циклогексанкарбоновая) ароматические (бензойная, фталевая)
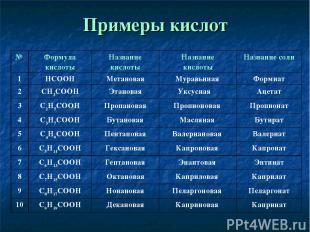
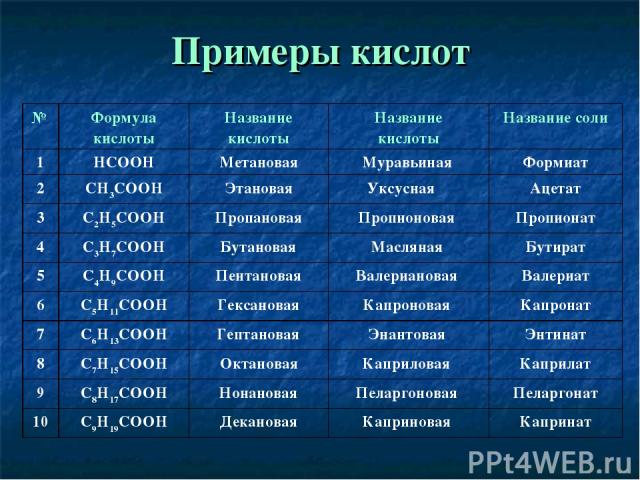
Примеры кислот № Формула кислоты Название кислоты Название кислоты Название соли 1 HCOOH Метановая Муравьиная Формиат 2 CH3COOH Этановая Уксусная Ацетат 3 C2H5COOH Пропановая Пропионовая Пропионат 4 C3H7COOH Бутановая Масляная Бутират 5 C4H9COOH Пентановая Валериановая Валериат 6 C5H11COOH Гексановая Капроновая Капронат 7 C6H13COOH Гептановая Энантовая Энтинат 8 C7H15COOH Октановая Каприловая Каприлат 9 C8H17COOH Нонановая Пеларгоновая Пеларгонат 10 C9H19COOH Декановая Каприновая Капринат

Изомерия 1.Изомерия углеродной цепи. 2. Изомерия положения кратной связи, например: СН2=СН—СН2—СООН Бутен-3-овая кислота (винилуксусная кислота) СН3—СН=СН—СООН Бутен-2-овая кислота (кротоновая кислота) 3. Цис-, транс-изомерия, например: 4. Межклассовая изомерия: например: С4Н8О2 СН3 — СН2— СО — О — СНз метиловый эфир пропановой кислоты СН3 — СО — О — CH2— СН3 этиловый эфир этановой кислоты С3Н7 – СООН бутановая кислота

Строение Карбоксильная группа СООН состоит из карбонильной группы С=О и гидроксильной группы ОН. В группе СО атом углерода несет частичный положительный заряд и притягивает к себе электронную пару атома кислорода в группе ОН. При этом электронная плотность на атоме кислорода уменьшается, и связь О-Н ослабляется: В свою очередь, группа ОН "гасит" положительный заряд на группе СО.

Физические и химические свойства Низшие карбоновые кислоты — жидкости с острым запахом, хорошо растворимые в воде. С повышением относительной молекулярной массы растворимость кислот в воде уменьшается, а температура кипения повышается. Высшие кислоты, начиная с пеларгоновой С8Н17СООН — твердые вещества, без запаха, нерастворимые в воде. Наиболее важные химические свойства, характерные для большинства карбоновых кислот: 1) Взаимодействие с активными металлами: 2 CH3COOH + Mg (CH2COO)2Mg + H2 2) Взаимодействие с оксидами металлов: 2СН3СООН + СаО (СН3СОО)2Са + Н2О

3) Взаимодействие с основаниями: CH3COOH + NaOH CH3COONa + H2O 4) Взаимодействие с солями: CH3COOH + NaHCO3 CH3COONa + СО2 + Н2О 5) Взаимодействие со спиртами (реакция этерификации): CH3COOH + СН3СН2ОН CH3COOСН2СН3 + H2O 6) Взаимодействие с аммиаком: CH3COOH + NH3 CH3COONH4 При нагревании аммонийных солей карбоновых кислот образуются их амиды: CH3COONH4 CH3CONH2 + H2O 7) Под действием SOCl2 карбоновые кислоты превращаются в соответствующие хлорангидриды. CH3COOH + SOCl2 CH3COCl + HCl + SO2

Способы получения Окисление альдегидов и первичных спиртов — общий способ получения карбоновых кислот: 2. Другой общий способ — гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода: 3. Взаимодействие реактива Гриньяра с СО2: -3NaCl

4. Гидролиз сложных эфиров: 5. Гидролиз ангидридов кислот:

Специфические способы получения Для отдельных кислот существуют специфические способы получения: Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия: Уксусную кислоту получают в промышленных масштабах каталитическим окислением бутана кислородом воздуха: Муравьиную кислоту получают нагреванием оксида углерода (II) с порошкообразным гидроксидом натрия под давлением и обработкой полученного формиата натрия сильной кислотой:

Применение карбоновых кислот Клей Гербициды Консервант, приправа Парфюмерия, косметика Искусственные волокна
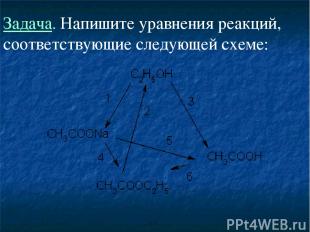
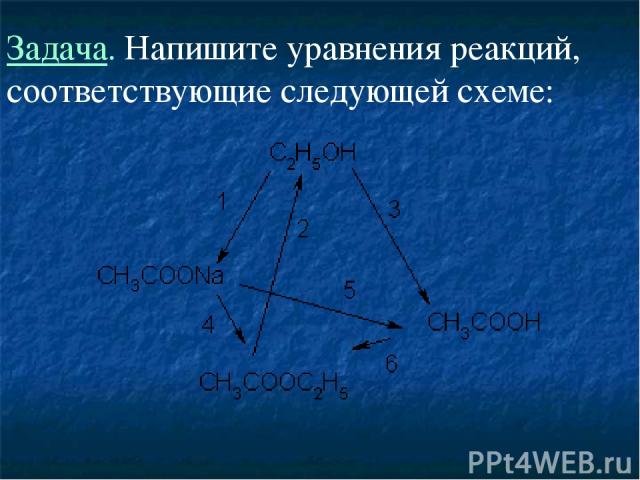
Задача. Напишите уравнения реакций, соответствующие следующей схеме:

Решение. 1) Этанол окисляется до ацетата натрия хроматом натрия в щелочном растворе: ЗС3Н5ОН + 4Na2CrO4 + 7NaOH + 4H2O 3CH3COONa + 4Na3[Cr(OH)6]. 2) Этилацетат гидролизуется под действием щелочей: СН3СООС2Н5 + NaOH CH3COONa + С2Н5ОН. 3) Этанол окисляется до уксусной кислоты дихроматом калия в кислом растворе: 5С2Н5ОН + 4KMnO4 + 6H2SO4 5СН3СООН + 2K2SO4 +4MnSO4 + + 11H2O. 4) Этилацетат можно получить из ацетата натрия действием этилиодида: CH3COONa + C2H5I СН3СООС2Н5 + Nal. 5) Уксусная кислота — слабая, поэтому сильные кислоты вытесняют ее из ацетатов: CH3COONa + HCl СН3СООН + NaCl 6) Сложный эфир образуется при нагревании уксусной кислоты с этанолом в присутствии серной кислоты: СН3СООН + С2Н5ОН СН3СООС2Н5 + Н2О












![Решение. 1) Этанол окисляется до ацетата натрия хроматом натрия в щелочном растворе: ЗС3Н5ОН + 4Na2CrO4 + 7NaOH + 4H2O 3CH3COONa + 4Na3[Cr(OH)6]. 2) Этилацетат гидролизуется под действием щелочей: СН3СООС2Н5 + NaOH CH3COONa + С2Н5ОН. 3) Этанол окисл… Решение. 1) Этанол окисляется до ацетата натрия хроматом натрия в щелочном растворе: ЗС3Н5ОН + 4Na2CrO4 + 7NaOH + 4H2O 3CH3COONa + 4Na3[Cr(OH)6]. 2) Этилацетат гидролизуется под действием щелочей: СН3СООС2Н5 + NaOH CH3COONa + С2Н5ОН. 3) Этанол окисл…](https://fs3.ppt4web.ru/images/132073/183558/640/img13.jpg)











