Презентация на тему: Щелочноземельные

Вторая группа главная подгруппа наряду с семейством щелочноземельных металлов включает и два типических элемента –бериллий и магний 900igr.net
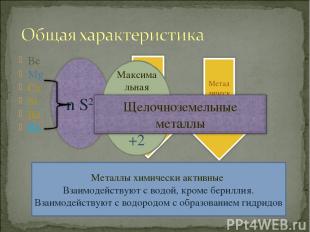
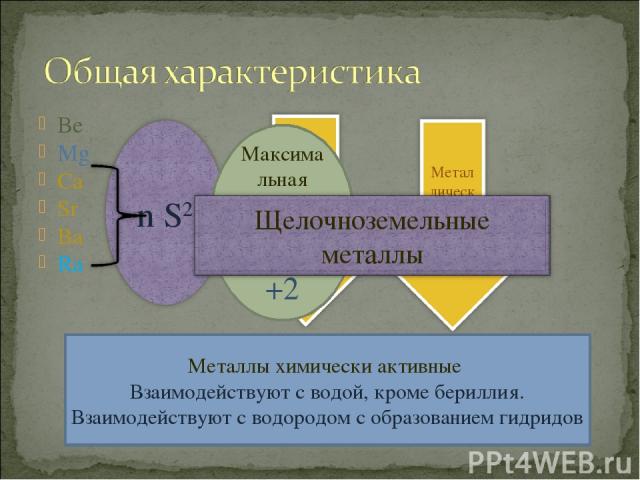
Be Mg Ca Sr Ba Ra Максимальная степень окисления +2 Металлы химически активные Взаимодействуют с водой, кроме бериллия. Взаимодействуют с водородом с образованием гидридов

Бериллий сходствует с алюминием и магнием…Получил своё название потому, что находится в минерале берилле. Металл называют также глицием от греческого слова «сладкий», потому что соли его имеют сладковатый вкус. Д.И.Менделеев

Берилл 3Be * Al2O3 *6SiO2 изумруд

В виде простого вещества бериллий получили в 1828году немецкий учёный Фридрих Вёлер и французский химик Антуан Бюсси. Они действовали калием на безводный хлорид бериллия BeCl2+2K=Be+2KCl

BeF2+Mg=Be+MgF2 В настоящее время бериллий получают, восстанавливая его фторид магнием, либо электролизом расплава смеси хлоридов бериллия и натрия.
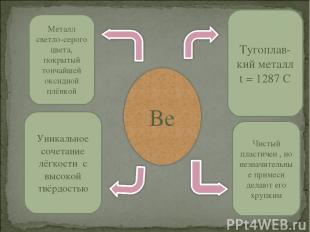
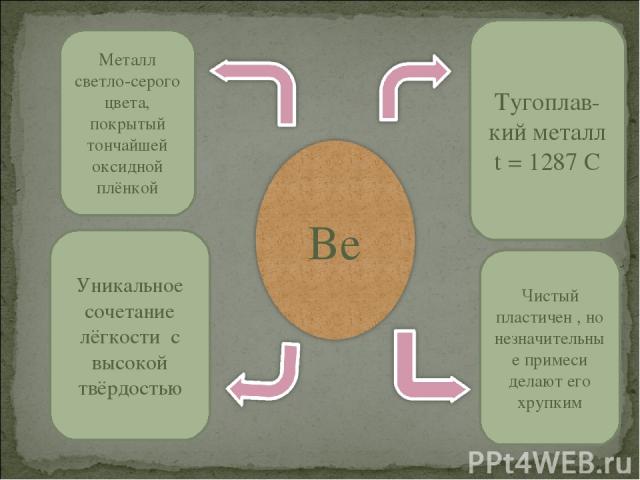
Металл светло-серого цвета, покрытый тончайшей оксидной плёнкой Тугоплав- кий металл t = 1287 C Уникальное сочетание лёгкости с высокой твёрдостью Чистый пластичен , но незначительные примеси делают его хрупким

Обладая высокой химической активностью бериллий вступает в реакции с галогенами, серой и азотом. Вода на него не действует, зато подобно алюминию он легко растворяется как в разбавленных кислотах , так в растворах щелочей. Be+2NaOH+2H2O= Na2 Be(OH)4 +H2

Магний был открыт при анализе воды из минерального источника вблизи города Эпсом в Англии. Горькая на вкус она привлекла внимание исследователей, при упаривании такой воды на стенках сосуда образовывалась белая корка вещества, соль MgSO4 7H2O
Впервые магний был получен в 1808г Гемфри Деви при электролизе влажной магнезии . По его предложению элемент назвали Magnium


Входит в состав минералов магнезит MgCO3 Доломит MgCO3 CaCO3

Горение на воздухе 2Mg+ O2=2MgO При комнатной температуре не взаимодействует с водой, лишь при кипячении Mg+2H2O=Mg(OH)2 +H2 Магний легко взаимодействует с разбавленными кислотами Химически активен Сильный восстанови- тель

Mg Твёрдые и прочные сплавы с алюминием магналий- 30 Mg Электрон –включает цинк, марганец, медь Автомобильная , авиационная и ракетная промышленность В медицине Оксид магния -для понижения кислотности желудка Сульфат магния - слабительное
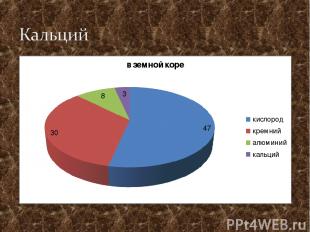



С простыми веществами Ca+H2=CaH2 Ca+Cl2=CaCl2 Ca+N2=Ca3N

Со сложными веществами Ca+ NH3=Ca(NH2)2 +H2 Ca+ H2O=Ca(OH)2+H2 Ca+ HCl=CaCl2+H2 любая кислота кроме азотной

Соединения кальция, стронция и бария применяют в разных отраслях промышленности и строительстве. Соединения стронция(нитрат, карбонат ,хлорид, оксалат) используют в производстве осветительных ракет, химического и термически устойчивого стекла. Оксид стронция входит в состав эмалей для защиты металлических предметов.

Презентацию выполнила учитель химии Тихомирова И.Ю. МОУ лицей № 20 г.Кострома