Презентация на тему: ЩЕЛОЧНОЗЕМЕЛЬНЫЕ МЕТАЛЛЫ


Изучение строения атомов щелочноземельных металлов, физических и химических свойств. Изучение строения атомов щелочноземельных металлов, физических и химических свойств.

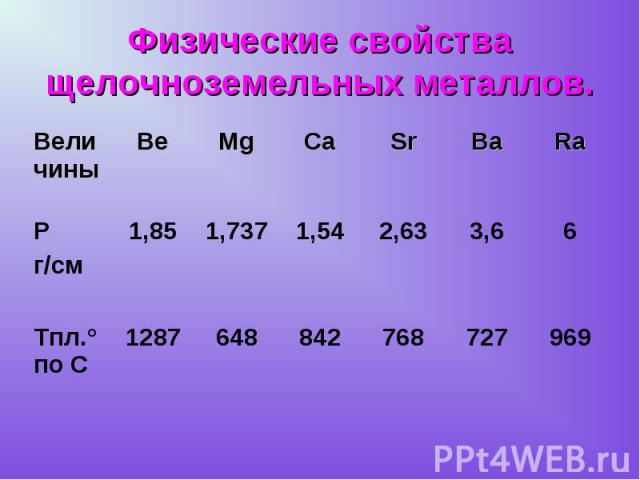
Be Mg Ca Sr Ba Ra Be Mg Ca Sr Ba Ra




1.Взаимодйествие с простыми веществами: 1.Взаимодйествие с простыми веществами: А) с кислородом 2Са+ О2= 2СаО Б) с галогенами Са +Сl2= CaCl2 В) с водородом Са +Н2 = СаН2 Г) с азотом 3Са + N2 = Ca3N2

2. Взаимодействие со сложными веществами. 2. Взаимодействие со сложными веществами. а) с водой Са + 2Н2О = Са(ОН)2 + Н2 б) с солями менее активных металлов Mg +CuSO4 =Cu +MgSO4 в) с оксидами металлов FeO + Mg = MgO +Fe Его используют для получения чистых металлов из оксидов. Этот способ получил название магниотермия.

Са с разбавленными кислотами не реагирует Са с разбавленными кислотами не реагирует


Решить задачу №1после §12 Решить задачу №1после §12 Осуществить превращения: Ca → CaO→ CaCl2→ Ca(OH)2 → CaCO3 →CaO