Презентация на тему: Процесс электролитической диссоциации

Интегрированный урок по химии и физике

Электролитическая диссоциация
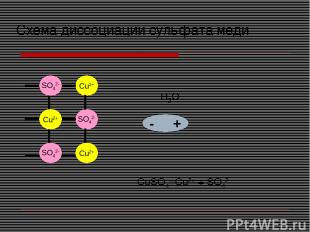
Cu2+ SO42- Cu2+ Cu2+ Cu2+ SO42- SO42- + - H2O - + - + Схема диссоциации сульфата меди CuSO4=Cu2+ + SO42-

Схема электролиза сульфата меди CuSO4 ↔ Cu2+ +SO42− K(-): Cu2+ + 2e = Cu0 A(+): 4OH− — 4e = 2H2O + O2 Вывод: CuSO4 (электролиз) → Cu + 2H2O + O2

Выводы: При растворении электролитов под влиянием электрического поля полярных молекул воды происходит распад молекул электролитов на ионы -этот процесс называется электролитической диссоциацией. Процесс выделения на электроде вещества, связанный с окислительно-восстановительными реакциями, называют электролизом. При тепловом (хаотическом) движении может происходить обратный процесс – рекомбинация – ионы разных знаков при встрече могут снова объединиться в нейтральные молекулы. В растворе электролита наряду с ионами находятся и молекулы.

Масса вещества, выделившегося на электроде за время t при прохождении электрического тока, пропорциональна силе тока и времени.

Майкл Фарадей (1711 -1867)
Задача. При никелировании детали в течении 50 минут сила тока, проходящего через ванну, была равна 2А. Какова масса, выделившегося вещества на детали, если электрохимический эквивалент никеля к=3·10-7 кг/Кл?

Применение электролиза I Химическая промышленность: Получение галогенов, водорода, щелочей. II Металлургия: Получение активных металлов, очистка металлов от примесей III Защита от коррозии: Электролитическим путем покрывают поверхность одного металла тонким слоем другого. IV Очистка сточных вод (процессы электрокоагуляции, электроэкстракции, электрофлотации).
Заключение Электрический ток в жидкостях создается движением ионов. Причина их появления – диссоциация. Электролиз – сложный физико-химический процесс, происходящий не только внутри жидкости, но и на электродах. При создании определенных условий можно получить целевой продукт с заранее заданными свойствами и качествами.