Презентация на тему: Окислительно-восстановительные реакции

Окислительно-восстановительные реакции 900igr.net

Цель урока: Закрепление, обобщение и углубление знаний об окислительно-восстановительных реакциях, расстановка коэффициентов методом электронного баланса

Опорные понятия Процесс восстановления – процесс принятия электронов частицей (атомом, молекулой, ионом). При восстановлении степень окисления элемента понижается. Процесс окисления – процесс отдачи электронов данной частицей (атомом, молекулой, ионом). При окислении степень окисления элемента повышается. Восстановители – частицы (атомы, молекулы или ионы), отдающие электроны. Восстановители – доноры электронов (от лат. donare – дарить). Окислители – частицы (атомы, молекулы или ионы), принимающие электроны. Окислители – акцепторы электронов (от лат. аcceptor – получатель).
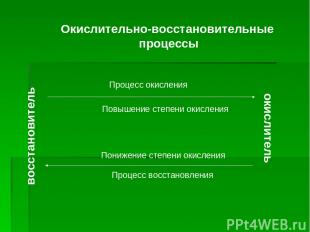
восстановитель окислитель Процесс окисления Повышение степени окисления Понижение степени окисления Процесс восстановления Окислительно-восстановительные процессы

Правила определения функции соединения в окислительно-восстановительных реакциях 1. Если элемент проявляет в соединении высшую степень окисления, то это соединение может быть окислителем. 2. Если элемент проявляет в соединении низшую степень окисления, то это соединение может быть восстановителем. 3. Если элемент проявляет в соединении промежуточную степень окисления, то это соединение может быть как окислителем, так и восстановителем.

Задание. Предскажите функции веществ в окислительно-восстановительных реакциях: H2SO4(конц), SO2, S, H2S Ответ H2SO4(конц) – окислитель, так как элемент сера проявляет в данном соединении высшую степень окисления (+6). H2S – восстановитель, так как элемент сера проявляет в данном соединении низшую степень окисления (-2). SO2, S – окислитель или восстановитель ( в зависимости от сореагентов), так как элемент сера проявляет в данных соединениях промежуточную степень окисления. Нами предсказаны функции веществ по сере. Если же рассматривать оба элемента, входящие в состав вещества, например, в случае H2S, то наряду с восстановительными свойствами соединение обладает и окислительными свойствами по элементу водороду, имеющему степень окисления +1. H2S + Zn = ZnS + H2

Важнейшие окислители 1. Простые вещества-неметаллы с наибольшими значениями электроотрицательности – F2, O2; 2. Сложные вещества, молекулы которых содержат элементы в высшей степени окисления – KMnO4, K2Cr2O7, HNO3, нитраты, H2SO4(конц), PbO2, HClO4, перхлораты 3. Среди веществ, содержащих элементы в промежуточных степенях окисления, более характерны окислительные свойства для Cl2, Br2, HClO, KClO3, MnO2, соли трехвалентного железа (FeCl3).

Важнейшие восстановители 1. Все простые вещества-металлы. Наиболее активными восстановителями являются щелочные и щелочно-земельные металлы, Mg, Al, Zn. 2. Сложные вещества, молекулы которых одержат элементы в низшей степени окисления – CH4, SiH4, NH3, PH3, нитриды и фосфиды металлов (например NaN3, Ca3P2), H2S, сульфиды металлов, HI, HBr, HCl, галогениды металлов, гидриды металлов (например, NaH, CaH2. 3. Среди веществ, содержащих элементы в промежуточных степенях окисления, более характерны восстановительные свойства для С, СО, сульфитов металлов (Na2SO3), соли двухвалентного железа (FeSO4).

Задания В каких из указанных ниже веществ марганец может проявлять только восстановительные свойства или только окислительные, или те и другие: KMnO4, MnO2, Mn2O7, Mn0, K2MnO4, MnO? В каких из перечисленных ниже веществ хром может проявлять только восстановительные свойства, только окислительные или те и другие: Сr2(SO4)3, CrO3, K2CrO4, Cr, CrCl2, K2Cr2O7? Укажите, в каких из приведенных ниже веществ сера может проявлять только восстановительные свойства, только окислительные, те и другие: S, H2S, H2SO3, SO3, FeS, SO2, H2SO4, Na2S2O3.
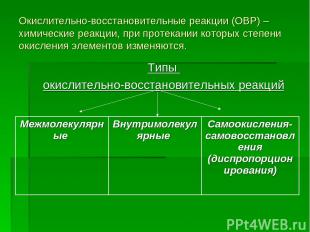
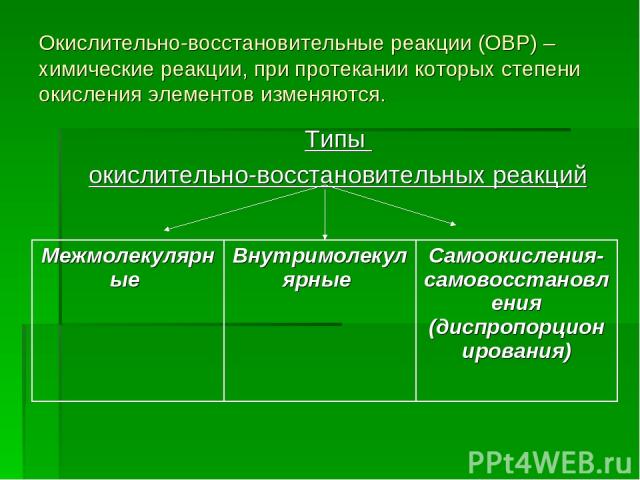
Окислительно-восстановительные реакции (ОВР) – химические реакции, при протекании которых степени окисления элементов изменяются. Типы окислительно-восстановительных реакций Межмолекулярные Внутримолекулярные Самоокисления- самовосстановления (диспропорционирования)

Межмолекулярные (ОВР) В этих реакциях элемент-окислитель и элемент-восстановитель входят в состав молекул различных веществ 0 0 -3 +1 N2 + H2 → NH3 +3 -1 +2 0 FeCl3 + KI → FeCl2 + I2 + KCl

Внутримолекулярные (ОВР) В этих реакциях элемент-окислитель и элемент-восстановитель входят в состав одного вещества. -3 +6 0 +3 (NH4)2Cr2O7 → N2 + Cr2O3 + H2O -3 +5 0 NH4NO2 → N2 + H2O

Самоокисления- самовосстановления (диспропорционирования) (ОВР) Это ОВР, при протекании которых один и тот же элемент, находится в промежуточной степени окисления, и окисляется и восстанавливается. Часть атомов данного элемента отдает электроны другой части атомов этого же элемента. +4 +3 +5 NO2 + H2O → HNO2 + HNO3 0 -1 +1 Cl2 + Ca(OH)2 → CaCl2 + Ca(ClO)2 + H2O

Составление ОВР методом электронного баланса В основе данного метода лежит следующее правило: общее число электронов, которое отдает восстановитель, должно быть равно общему числу электронов, которое присоединяет окислитель. Рассмотрим применение метода электронного баланса на примере реакции, которая выражается следующей схемой: KMnO4 + KBr + H2SO4 → MnSO4 + Br2 + K2SO4 + H2O

Алгоритм 1. Определим степени окисления всех элементов в молекулах исходных веществ и продуктов реакции: +1 +7 -2 +1 -1 +1+6 -2 +2 +6 -2 0 +1+6 -2 +1-2 KMnO4 + KBr + H2SO4 → MnSO4 + Br2 + K2SO4 + H2O 2. Подчеркнем символы элементов, которые изменяют степени окисления в ход реакции: +7 -1 +2 0 KMnO4 + KBr + H2SO4 → MnSO4 + Br2 + K2SO4 + H2O

3. Составим уравнения процессов окисления и восстановления: +7 +2 Mn + 5ē → Mn (восстановление) -1 0 2Br - 2ē → Br2 (окисление) 4. Находим множители для уравнений процессов окисления и восстановления, при умножении на которые числа отданных и присоединенных электронов будут равны. Так как наименьшим общим кратным чисел «5» и «2» является «10», то уравнение процесса восстановления нужно умножить на «2», а уравнение процесса окисления - на «5» +7 +2 Mn + 5ē → Mn ן2 -1 0 2Br - 2ē → Br2 ן5

5. Найденные множители запишем как коэффициенты перед формулами веществ, которые содержат элементы, участвующие в процессах окисления и восстановления: 2KMnO4 + 10KBr + H2SO4 → 2MnSO4 + 5Br2 + K2SO4 + H2O 6. После этого уравняем числа атомов элементов, которые не изменяют степени окисления. В данном случае это атомы калия, серы, водорода и кислорода. 2KMnO4 + 10KBr + 8H2SO4 → 2MnSO4 + 5Br2 + 6K2SO4 + 8H2O Обычно числа атомов водорода и кислорода уравнивают в последнюю очередь. Во многих случаях равенство чисел атомов кислорода в левой и правой частях уравнения ОВР свидетельствует о том, что это уравнение составлено правильно.

Выполните задания 1. В каких из приведенных уравнений реакций соединения железа является окислителями, в каких восстановителями, расставьте коэффициенты методом электронного баланса: A) Fe2О3 + Al = Fe + Al2O3 B) Fe2О3 + KNO3 + KOH = K2FeO4 + KNO2 + H2O C) FeSO4 + Mg = MgSO4 + Fe D) FeSO4 + KMnO4 + H2SO4 = Fe2(SO4)3 + MnSO4 + K2SO4 + H2O E) Fe(OH)2 + O2 + H2O = Fe(OH)3

2. Определите типы окислительно-восстановительных реакций, расставьте коэффициенты методом электронного баланса: H2S + HNO3 = H2SO4 + NO2 + H2O H2S + H2SO3 = S + H2О Pb(NO3)2 = PbO + NO2 + O2 NaNO3 = NaNO2 + O2 NH4NO2 = N2 + H2О HNO2 = HNO3 + NO + H2O 3. В схемах реакций растворения металлов в азотной кислоте подберите коэффициенты методом электронного баланса: Ag + HNO3 → AgNO3 + NO2 + H2O Cu + HNO3 → Cu(NO3)2 +NO +H2O Ca + HNO3 → Ca(NO3)2 + N2O + H2O Mg + HNO3 → Mg(NO3)2 + N2 + H2O Mg + HNO3 → Mg(NO3)2 + NH4NO3 + H2O Fe + HNO3 → Fe(NO 3)3 + NO2 +H2O

Домашнее задание А.С. Егоров Репетитор по химии. Ростов-на-Дону: Феникс, 2004г. параграф 4,1. с.149-157, упражнение 4,5 с.158