Презентация на тему: Общая характеристика галогенов

Тема урока: Общая характеристика галогенов. 5klass.net Муниципальное общеобразовательное учреждение «Сланцевская средняя общеобразовательная школа №3» Автор: Зайцева Галина Александровна учитель химии

Цели урока: 1.Систематизировать знания учащихся о галогенах. 2.Ознакомить учащихся с окислительными свойствами галогенов. 3.Повторить, обобщить и закрепить на материале химии галогенов химические понятия, как «химическая связь», « кристаллические решетки», «окисление и восстановление». Оборудование: ТСО, презентация, ПСХЭ, образцы галогенов, диск «Химия для всех».

План урока: • определить положение галогенов в ПСХЭ, • рассмотреть строение атомов галогенов, • физические свойства простых веществ, • химические свойства.

Определите положение галогенов в ПСХЭ. Перечислите их. Галогены (от греч. halos - соль и genes - образующий) - элементы главной подгруппы VII группы периодической системы. F Cl Br I At

Строение атомов галогенов: На внешнем энергетическом уровне по 7 электронов. Малый радиус атома (в сравнении с элементами других групп ПС). В связи с этим имеют высокие значения электроотрицательности и сильные неметаллические свойства. Как изменяется окислительная способность и значение ЭО в ряду элементов? F Cl Br I At - радиусы атомов увеличиваются - уменьшается значение ЭО - уменьшается окислительная способность
Возможные степени окисления галогенов ПОСТОЯННАЯ ПЕРЕМЕННАЯ Только у F У всех остальных (-1) галогенов (-1,+1, +3, +5, +7).

Галогены как простые вещества. 1. Г2 - общая формула галогенов- простых веществ. 2. Тип химической связи в молекуле- ковалентная неполярная химическая связь. 3. Тип кристаллической решетки - молекулярная (I2- йод). кр. решетка йода

4. Возможные агрегатные состояния Галогены как простые вещества. газообразное жидкое твёрдое F Cl Br I ХЛОР БРОМ ЙОД 5. Разная цветовая гамма. Интенсивность окраски галогенов увеличивается от фтора к йоду.

6. Температуры кипения и плавления с увеличением атомной массы галогенов увеличиваются. Галогены как простые вещества.

7. Все галогены – токсичные вещества! Галогены как простые вещества. Жидкий хлор вызывает серьезные ожоги кожи. Газообразный хлор оказывает сильное раздражающее действие, особенно на глаза и дыхательную систему. Очень радиоактивен, поэтому о нём сравнительно мало известно. 8. Галогены имеют характерный резкий запах .
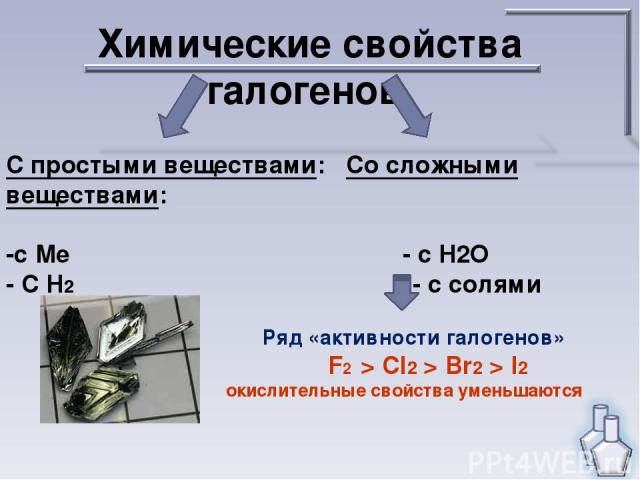
Химические свойства галогенов. С простыми веществами: Со сложными веществами: -с Ме - с Н2О - С Н2 - с солями Ряд «активности галогенов» F2 > Cl2 > Br2 > I2 окислительные свойства уменьшаются

Вопросы для закрепления материала: Галогенами называют элементы ... подгруппы. Это ... . Внешний энергетический уровень атомов галогенов содержит ... валентных электронов, поэтому высшая валентность равна ... , а низшая равна ... . 3. Галогены – типичные ... . 4. С увеличением радиуса атома неметаллические свойства ... . ... – самый активный неметалл. 5. Галогены окрашены, причем интенсивность окраски ... с увеличением их массы. Фтор – ... , хлор – ... , бром – ... , йод – ... . 6. Химическая активность галогенов ... . 7. Галогены взаимодействуют с водой с образованием ... . Их активность ... от фтора к йоду. 8. Каждый ... галоген вытесняет ... галоген из его соединений.


Источники материалов: 1. Габриелян О.С. Химия. 9 класс: учебник для общеобразовательных учреждений.(базовый) – М.: Дрофа, 2007. 2. Габриелян О.С., Методическое пособие. Химия. 8-9 класс. - М.: Дрофа, 2008. 3. Габриелян О.С., Настольная книга учителя. Химия. 9 класс. - М.: Дрофа, 2007. 4.http://ru.wikipedia.org/wiki/%D0%93%D0%B0%D0%BB%D0%BE%D0%B3%D0%B5%D0%BD%D1%8B 5. http://nanolife.info/tablica-mendeleeva/13-himicheskiy-element-astat.html 6. http://nanolife.info/tablica-mendeleeva/21-brom-soedineniya-broma.html 7. http://www.kristallikov.net/page20.html