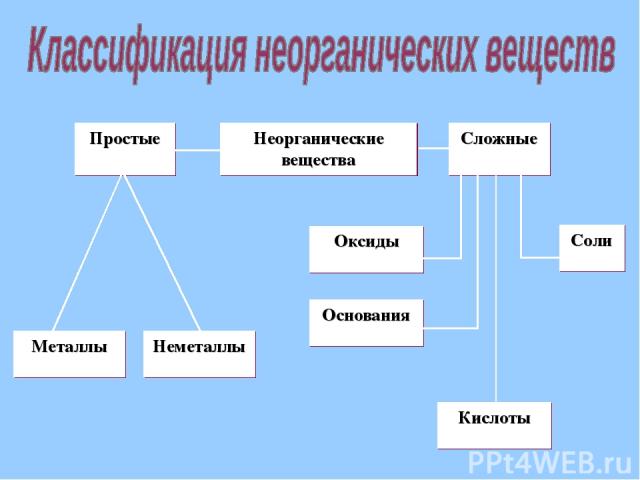
Презентация на тему: Неорганические соединения

Тема: “Обобщение сведений об основных классах неорганических соединений”. 900igr.net

Цель: Повторить и обобщить знания, умения и навыки по данной теме

Фронтальный опрос Что такое степень окисления? Какие соединения называются бинарными? Что такое гидриды? Дайте определение оксидам. Как называются растворимые основания?

По каким признакам можно классифицировать кислоты? Приведите примеры.

Правило разбавления серной кислоты в воде

Что такое соли? Какие типы кристаллических решеток вы знаете? Что такое массовая доля?

Третий лишний а) SO2, НСl, Na2O; б) НNО3, Н2SiО3, Н2СО3;

Третий лишний в) NаОН, Мg(OH)2, SO3; г)Nа2O, СаО, SO2

Составьте формулы данных соединений: оксид азота(V), сульфид калия, гидроксид меди (I), сернистая кислота

Химический диктант Ответ “да” или “нет” “да”-1 “нет”-0

1. Соляная кислота образована ионной связью. 2.В соединении НСl , хлор является более электроотрицательным элементом. 3.Нулевые значение степени окисления имеют атомы в молекулах простых веществ и атомы в свободном состоянии. 4. В соединении NO2 у азота степень окисления равняется +2. 5.Заряженные частицы называются ионами.

6. Металлы 1 группы главной подгруппы в соединениях имеют степень окисления +1. 7.В гидридах степень окисления водорода равна +1 8.Соли азотистой кислоты называются нитраты 9.Аморфные вещества не имеют определенной температуры плавления 10. Массовая доля выражается в г/моль

Правильный ответ 0110110010

Попасть в кислоту – для него неудача Но он перетерпит без вздоха, без плача Зато в щелочах у такого блондина Начнется не жизнь, а сплошная малина

Чтоб появиться я сумел, прокаливают белый мел меня дает огонь в печи И пламя маленькой свечи. И стоит только сделать вдох, Чтоб я на свет явиться мог. Я в газированной воде, Я в хлебе, соде, я везде!

Ах, что же я поделаю с собой - Ведь в щелочи я сине-голубой. А в кислоте быть синим я не смею: Я - ..., и в кислотах я краснею. Как на прогулке от мороза, От кислого я стану розов. Но вид мой в щелочи смешон: Я сразу желтый, как лимон.

Найдите родственников
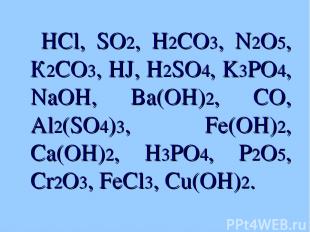
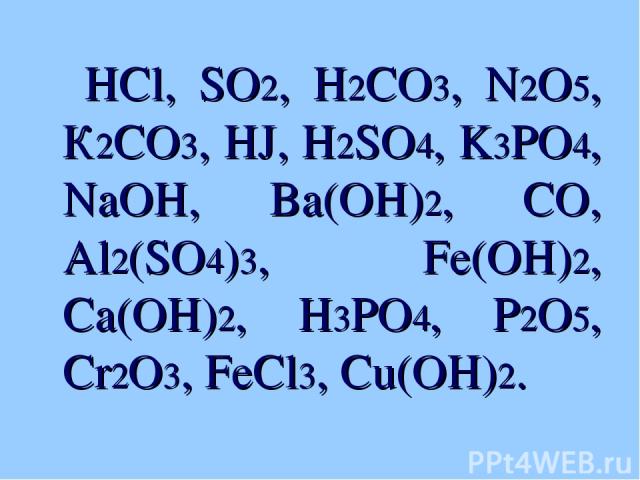
HCl, SO2, H2CO3, N2O5, К2CO3, HJ, H2SO4, K3PO4, NaOH, Ba(OH)2, CO, Al2(SO4)3, Fe(OH)2, Ca(OH)2, H3PO4, P2O5, Cr2O3, FeCl3, Cu(OH)2.
оксиды основания кислоты соли
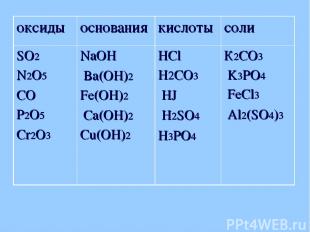
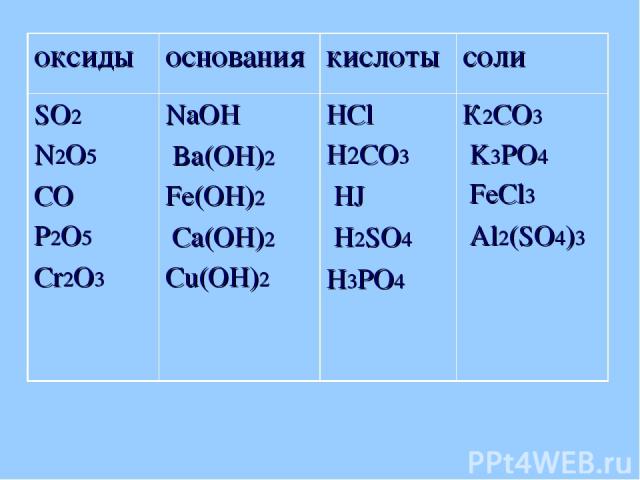
оксиды основания кислоты соли SO2 N2O5 CO P2O5 Cr2O3 NaOH Ba(OH)2 Fe(OH)2 Ca(OH)2 Cu(OH)2 HCl H2CO3 HJ H2SO4 H3PO4 К2CO3 K3PO4 FeCl3 Al2(SO4)3

1.мел 2.угарный газ 3.веселящий газ 4.плавиковая кислота 5.поваренная соль 6.аммиак 7.негашенная известь Д. NaCl Е. NH3 О. CO М. Ca CO3 О. HF Ц. CaO Л. N2O

Всем спасибо за хорошую работу на уроке

Решите задачу 1-Вариант Вычислить массовую долю кислорода в серной кислоте. 2-Вариант Вычислить массовую долю азота в нитрате калия

Решите задачу 1-вариант Вычислить сколько граммов соли и воды потребуется для приготовления 25 г раствора с массовой долей растворенного вещества 8 % ? 2-вариант Какие массы соли и воды необходимо взять для приготовления 500 г раствора с массовой долей соли 6 %.