Презентация на тему: Неметаллы

Неметаллы Химия 9 класс Учитель Кулешова С.Е. 900igr.net

Положение в ПСМ Назовите неметаллы Где они располагаются в таблице Менделеева? Как вы думаете, в таблице больше металлов или неметаллов? Назовите самые активные и сильные неметаллы
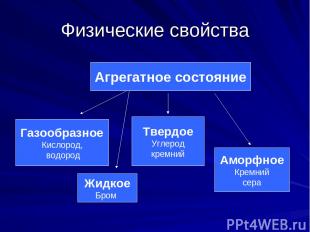
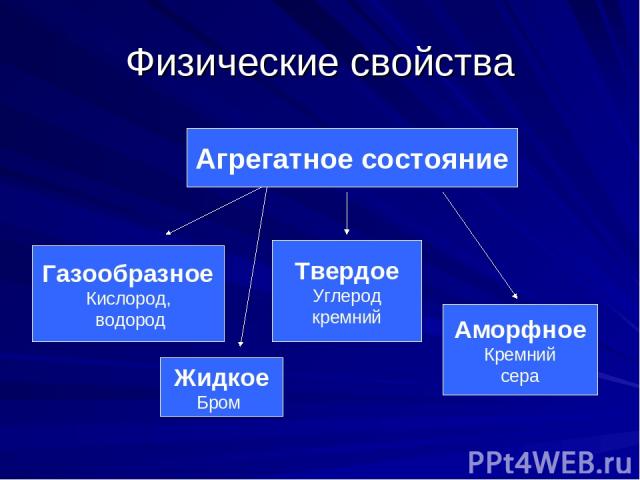
Физические свойства Агрегатное состояние Газообразное Кислород, водород Жидкое Бром Твердое Углерод кремний Аморфное Кремний сера

Чем объясняется разнообразие агрегатного состояния неметаллов Наличие кристаллической решетки: Атомные Молекулярные бор сера алмаз йод графит белый фосфор

Физические свойства Некоторые имеют металлический блеск Проводят электрический ток Обладают теплопроводностью Пластичность НО , они хрупкие вещества

Аллотропия Способность элемента образовывать несколько простых веществ Причина – различие в строении кристаллической решетки, различный состав молекул. Примеры: Алмаз – графит ( крист. Решетка) Красный фосфор – белый фосфор (строение молекулы Р2 и Р4)
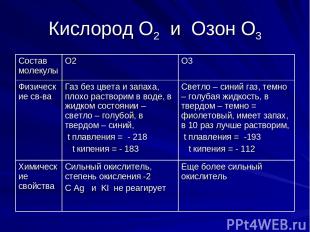
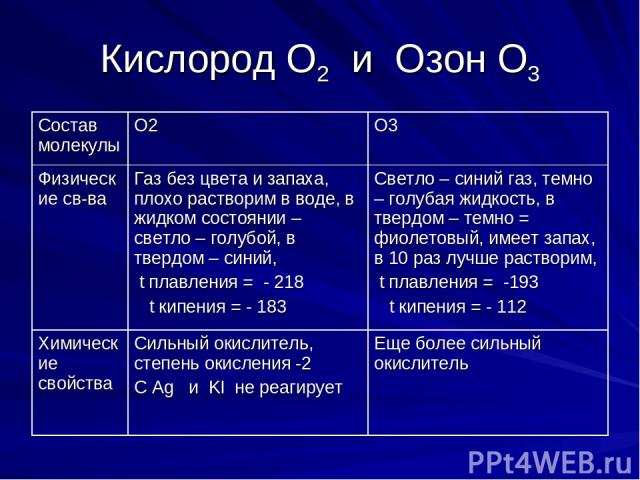
Кислород О2 и Озон О3 Состав молекулы О2 О3 Физические св-ва Газ без цвета и запаха, плохо растворим в воде, в жидком состоянии – светло – голубой, в твердом – синий, t плавления = - 218 t кипения = - 183 Светло – синий газ, темно – голубая жидкость, в твердом – темно = фиолетовый, имеет запах, в 10 раз лучше растворим, t плавления = -193 t кипения = - 112 Химические свойства Сильный окислитель, степень окисления -2 С Ag и KI не реагирует Еще более сильный окислитель

Химические свойства неметаллов Окислители: взаимодействуют с металлами Восстановители ( кроме фтора, гелия, неона) взаимодействуют друг с другом Примечание : см. РЯД ЭЛЕКТРООТРИЦАТЕЛЬНОСТИ НЕМЕТАЛЛОВ

ЗАГАДКИ Он повсюду и везде В камне , в воздухе, в воде Он и в утренней росе И в небесной синеве Если вдруг он когда –то иссякнет, в недрах звезд весь сгорит без следа, во вселенной светило погаснет, и наступит здесь мрак навсегда Родня большая у меня: кислоты, соли – всюду я. В составе пороха, друзья, большую часть составляю я Из меня состоит все живое: я графит, антрацит и алмаз, я на улице , в школе и в поле, я в деревьях и в каждом из вас

Тест На внешнем уровне у неметаллов А) более 3 электронов Б) менее 3 электронов Агрегатное состояние неметаллов может быть: А)газообразное Б) жидкое В) твердое Г) аморфное Разнообразие физических свойств неметаллов объясняется а) они могут иметь атомную кристаллическую решетку Б) молекулярную кристаллическую решетку В) различие в количественном составе молекул Многообразие простых веществ объясняется А) аморфностью Б) аллотропией По химическим свойствам неметаллы могут быть А) окислителями Б) восстановителями

Водород Дайте характеристику водорода Газ без цвета и запаха, легче воздуха, плохо растворим в воде, растворим в металлах: железе, свинце, никеле Применение: дирижабли, метеорологические зонды. Используется как восстановитель в металлургии и органическом синтезе, для получения аммиака, в качестве экологического топлива

Получение водорода В промышленности из углеводородов СН4 = С + 2Н2 Взаимодействием угля с водой С + Н2О = СО + Н2 Метана с водой СН4 + Н2О = СО + Н2 Электролизом воды 2Н2О = 2Н2 + О2 в лабораториях при взаимодействии цинка с кислотой

Химические свойства водорода С металлами, образуя гидриды С неметаллами восстанавливает металлы из оксидов В смеси с фтором, кислородом, хлором – взрывоопасен Допишите уравнения реакций: H2 + S H2+ O2 H2+ Cl2 H2+ N2

Домашнее задание Записи в тетрадях Параграф 15,16,17