Презентация на тему: Насыщенные углеводороды

Предельные ( насыщенные) углеводороды, парафины 900igr.net
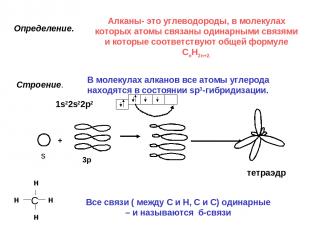
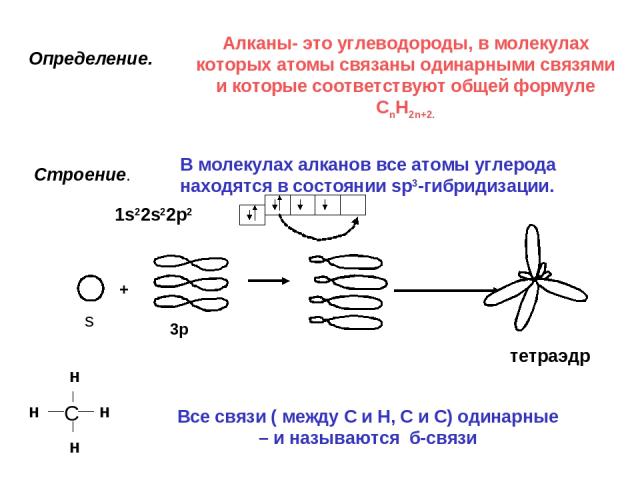
Определение. Алканы- это углеводороды, в молекулах которых атомы связаны одинарными связями и которые соответствуют общей формуле CnH2n+2. Строение. В молекулах алканов все атомы углерода находятся в состоянии sp3-гибридизации. тетраэдр + 1s22s22p2 Все связи ( между С и Н, С и С) одинарные – и называются б-связи s 3p С н н н н
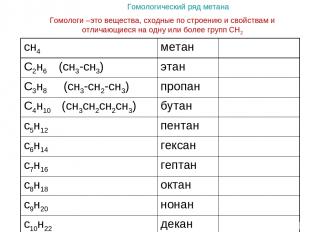
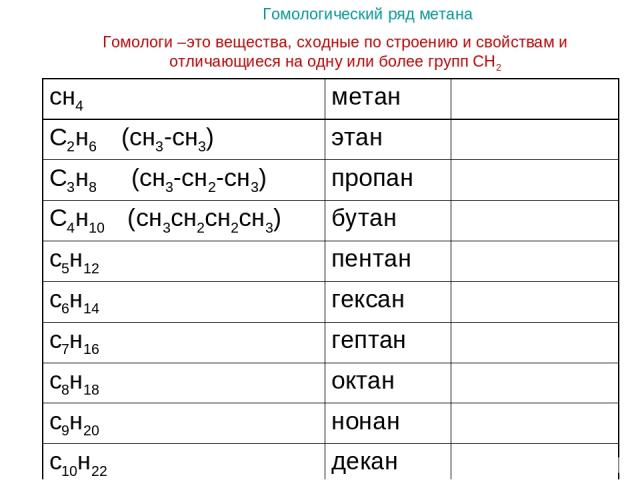
Гомологический ряд метана Гомологи –это вещества, сходные по строению и свойствам и отличающиеся на одну или более групп СН2 сн4 метан С2н6 (сн3-сн3) этан С3н8 (сн3-сн2-сн3) пропан С4н10 (сн3сн2сн2сн3) бутан с5н12 пентан с6н14 гексан с7н16 гептан с8н18 октан с9н20 нонан с10н22 декан

Изомерия и номенклатура. Названия предельных углеводородов имеют окончание -ан Для алканов характерна структурная изомерия Выбор главной цепи -самая длинная цепочка атомов С в молекуле- это основа Нумерация атомов главной цепи - начинают с того конца к которому ближе стоит заместитель; если заместители равноудалены, то нумерацию начинают с того конца, где расположен старший заместитель- метил, этил, пропил, и т.д.. Формирование названия: 1) указывается номер атома углерода, при котором находится заместитель, если их несколько, то номер повторяется через запятую( 2 метил-, 2,3-диметил), указывая и число заместителей ( ди,три, тетра и т.д.) С-с-с-с-с-с 2 метил 5этилгексан С-с-с-с-с-с- сс 3 -этилгексан с С С 1 2 3 4 5 6 1 2 3 4 5 6
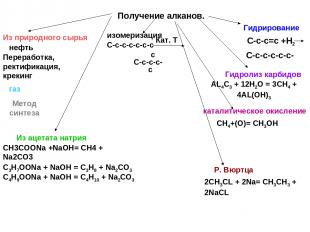
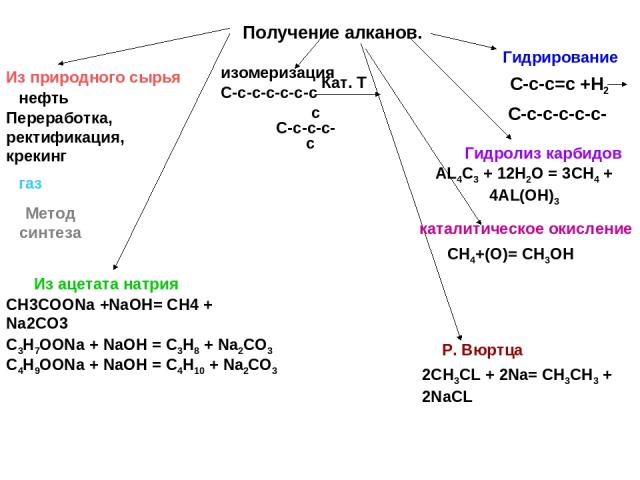
Получение алканов. Из природного сырья нефть газ Переработка, ректификация,крекинг Метод синтеза изомеризация С-с-с-с-с-с-с Кат. Т С-с-с-с- Гидрирование С-с-с=с +Н2 С-с-с-с-с-с- Из ацетата натрия СН3СООNa +NaOH= CH4 + Na2CO3 C3H7OONa + NaOH = C3H8 + Na2CO3 C4H9OONa + NaOH = C4H10 + Na2CO3 Р. Вюртца 2СН3CL + 2Na= CH3CH3 + 2NaCL Гидролиз карбидов AL4C3 + 12H2O = 3CH4 + 4AL(OH)3 каталитическое окисление СН4+(О)= СН3ОН с с
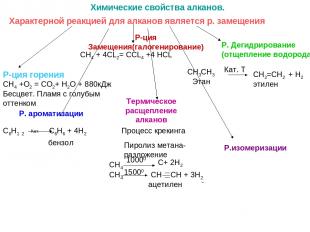
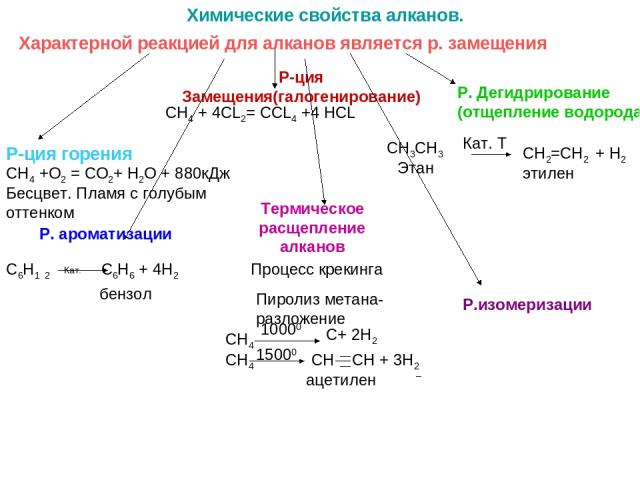
Химические свойства алканов. Р-ция Замещения(галогенирование) Р. Дегидрирование (отщепление водорода) СН3СН3 Кат. Т СН2=СН2 + Н2 Этан этилен Р-ция горения СН4 +О2 = СО2+ Н2О + 880кДж Термическое расщепление алканов Процесс крекинга Пиролиз метана- разложение СН4 10000 С+ 2Н2 СН4 15000 СН СН + 3Н2 ацетилен Р.изомеризации Р. ароматизации С6Н1 2 С6Н6 + 4Н2 Кат. бензол Бесцвет. Пламя с голубым оттенком Характерной реакцией для алканов является р. замещения CH4 + 4CL2= CCL4 +4 HCL

Задания по теме. 1. Составьте формулу алкана, имеющего 12 атомов углерода, 35 атомов углерода, 36 атомов водорода, 24 атома водорода. 2. Найти в-ва, относящиеся к классу алканов:С5Н10, С8Н18, С6Н6, С6Н12, С6Н14, С2Н6, С2Н2, С9Н20, С9Н18, С9Н16. 3. Составьте формулы гомологов гексана, декана,пропана, этана. 4. Напишите формулы возможных изомеров пентана, октана. 5. Среди указанных формул найдите формулы гомологов и изомеров: 1) гептан 2) 2метилпентан 3) 2,3-диметипропан 4) пентан 5) 2,2-диметилпентан 6) 2-метилбутан 6) Определить сколько веществ указано: 1) сн3-сн2-сн3 2) сн3-сн2-сн2-сн3 3) сн3-сн-сн3 сн3 4) сн-сн3 сн3 5) с с с с 6) с с с с

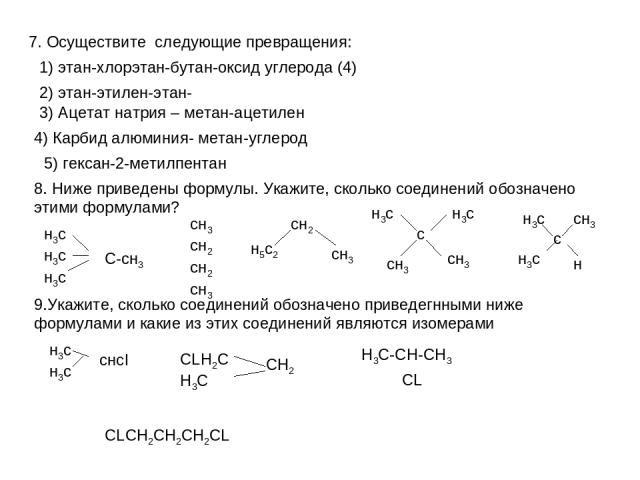
7. Осуществите следующие превращения: 1) этан-хлорэтан-бутан-оксид углерода (4) 2) этан-этилен-этан- 3) Ацетат натрия – метан-ацетилен 4) Карбид алюминия- метан-углерод 5) гексан-2-метилпентан 8. Ниже приведены формулы. Укажите, сколько соединений обозначено этими формулами? н3сн3сн3с С-сн3 сн3сн2сн2сн3 сн2 н5с2 сн3 с н3с сн3 сн3 н3с с н3с сн3 н н3с 9.Укажите, сколько соединений обозначено приведегнными ниже формулами и какие из этих соединений являются изомерами н3сн3с снсl CLH2CH3C CH2 H3C-CH-CH3 CL CLCH2CH2CH2CL

10. Напишите структурные формулы 2,4,4-триметилгексана и 2,2-диметилпентана. 11. Скелет молекулы пропана схематически изображают Составьте подобные схемы для бутана и изобутана, Напишите также полную формулу углеводорода, скелет которого 12.Чем являются друг для друга: 1) н-бутан и 2-метилпропан; 2) н-бутан и н-пентан? Контрольные работы для 10класса, стр.112-113, Методическое пособие для 10 класса, стр.70.
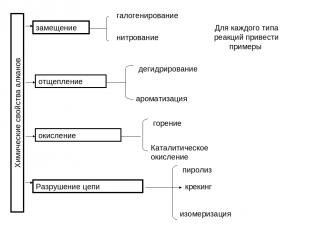
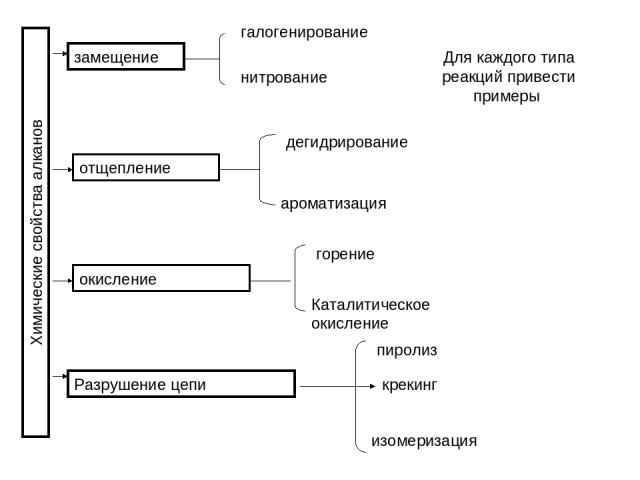
Химические свойства алканов замещение галогенирование нитрование Для каждого типа реакций привести примеры отщепление дегидрирование ароматизация окисление горение Каталитическое окисление Разрушение цепи пиролиз крекинг изомеризация