Презентация на тему: Предельные углеводороды

урок № 4 в теме«ПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ» Презентацию подготовила: Учитель химии высшей категории Отрошко Елена Александровна МОУ СОШ № 6 Ст. Старотитаровской Темрюкский район Краснодарский край 2008 год

ТЕМА УРОКА: «Химические свойства алканов» Цели урока: На основе представлений о составе и строении молекул, природе химических связей рассмотреть химические свойства предельных углеводородов. Обратить внимание на соблюдение правил пользования бытовым газом вследствие его взрывоопасности.

В обычных условиях алканы химически инертны. Они устойчивы к действию многих реагентов: не взаимодействуют с концентрированными серной и азотной кислотами, с концентрированными и расплавленными щелочами, не окисляются сильными окислителями – перманганатом калия KMnO4 и т. п. Химическая устойчивость алканов объясняется высокой прочностью б - связей С-С и С-Н, а также их неполярностью. Неполярные связи С-С и С-Н не склонны к ионному разрыву, но способны расщепляться гомолитически под действием активных свободных радикалов.
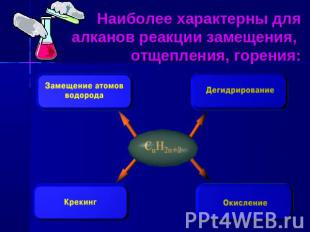
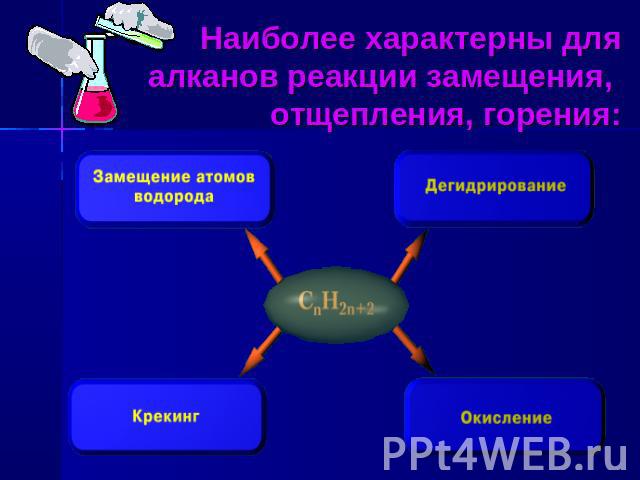
Наиболее характерны для алканов реакции замещения, отщепления, горения:

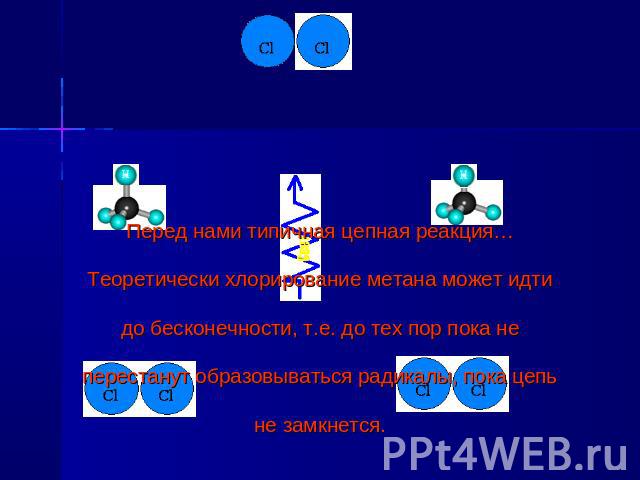
Реакции замещения. Протекают по механизму радикального замещения, обозначаемого Sr (англ. substitution radicalic). а) с галогенами (с Cl2 – на свету, с Br2 – при нагревании). Хлорирование метана

Механизм реакции замещения Состоит из 3 стадий: -зарождение цепи -развитие цепи -обрыв цепи
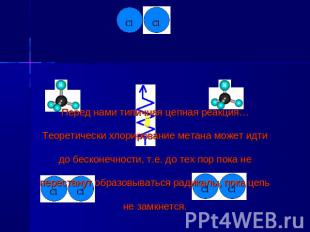
Перед нами типичная цепная реакция… Теоретически хлорирование метана может идти до бесконечности, т.е. до тех пор пока не перестанут образовываться радикалы, пока цепь не замкнется.

Общая схема реакции Sr * Замещение у хлорметана идет легче, чем у метана, так как атом хлора поляризует связи С-Н и делает их реакционноспособными. * Замещение легче всего идет у третичного атома углерода, сложнее – у вторичного, первичного атомов.

Взаимодействие со фтором в) в атмосфере фтора происходит следующая реакция:
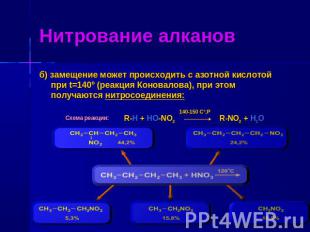
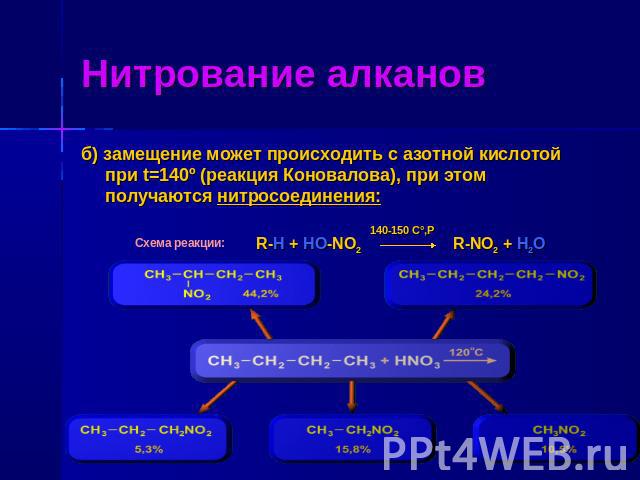
Нитрование алканов б) замещение может происходить с азотной кислотой при t=140º (реакция Коновалова), при этом получаются нитросоединения:

Реакции отщепления. а) дегидрирование: б) крекинг алканов: в) полное термическое разложение: г) для метана характерен пиролиз:

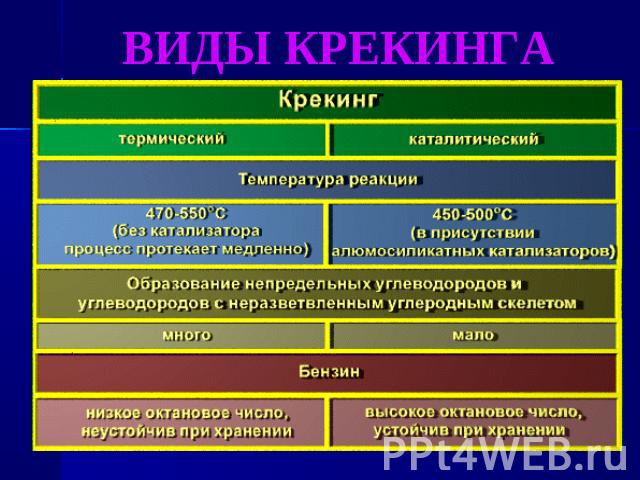
Крекинг алканов Крекинг – реакции расщепления углеродного скелета крупных молекул при нагревании и в присутствии катализаторов. При температуре 450 – 700 ° С алканы распадаются за счет разрыва связей С – С (более прочные связи С – Н при этом сохраняются) и образуются алканы и алкены с меньшим числом углеродных атомов. Распад связей происходит гомолитически с образованием свободных радикалов:
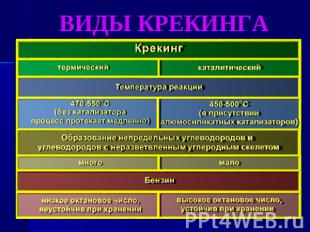
ВИДЫ КРЕКИНГА

Реакции окисления. а) все алканы горят с образованием углекислого газа и воды : б) при недостатке кислорода алканы могут сгорать до угарного газа или с образованием сажи (коптят): в) каталитически алканы могут окисляться с разрывом С – С связи примерно в середине молекулы:

Горение алканов:

Взрыв метана с кислородом Для полного сгорания метана на один объем метана нужно взять два объема кислорода (см. уравнение реакции). Пластиковую бутылку, разделенную метками на три равные части, заполним способом вытеснения воды одной частью метана и двумя частями кислорода. При поджигании смеси происходит взрыв - полное сгорание метана в кислороде. CH4 + 2О2 = СО2 + 2 Н2О Оборудование: пробирка, газоотводная трубка, промывалка, кристаллизатор, цилиндр, горелка, штатив. Техника безопасности. Соблюдать правила работы с горючими газами и нагревательными приборами.

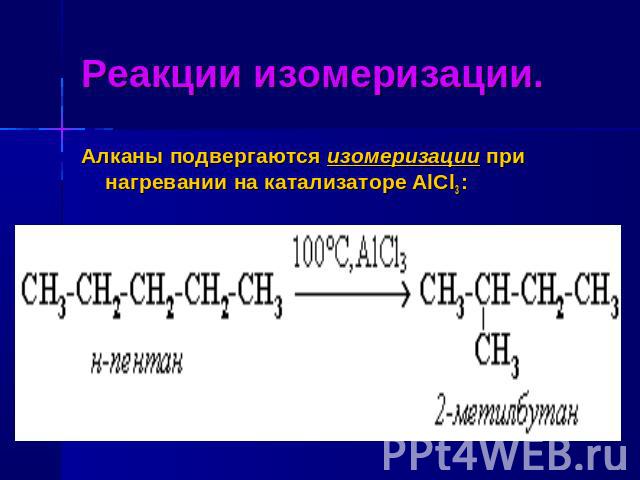
Реакции изомеризации. Алканы подвергаются изомеризации при нагревании на катализаторе AlCl3 :
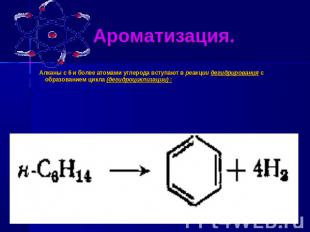
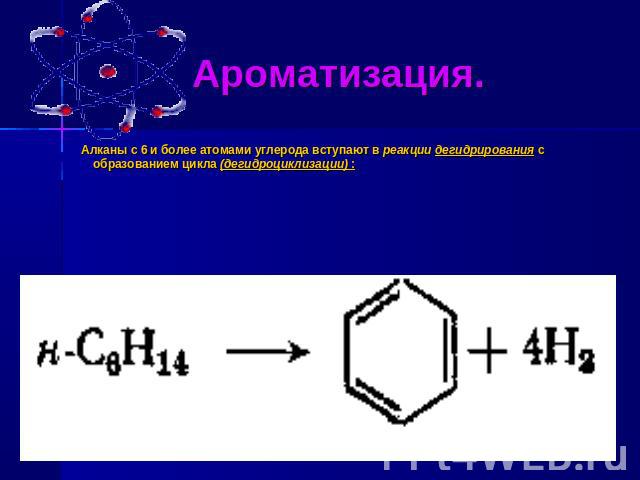
Ароматизация. Алканы с 6 и более атомами углерода вступают в реакции дегидрирования с образованием цикла (дегидроциклизации) :

Домашнее задание: ξ 6 , задание 3-5