Презентация на тему: Алкены - непредельные углеводороды. Получение, химические свойства и применение

АЛКЕНЫ – НЕПРЕДЕЛЬНЫЕ УГЛЕВОДОРОДЫ.ПОЛУЧЕНИЕ, ХИМИЧЕСКИЕ СВОЙСТВА И ПРИМЕНЕНИЕ.

Учебная цель: изучить состав, строение молекул,способы получения,химические свойства и применение алкенов на примере непредельного углеводорода - этилена
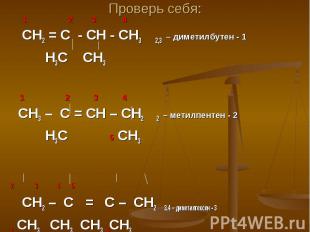
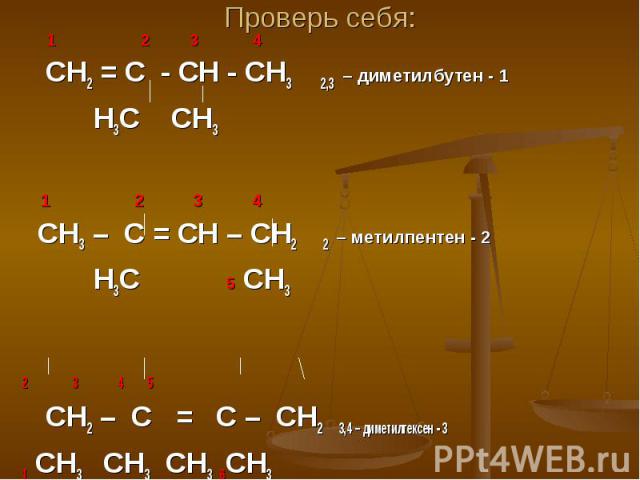
Проверь себя: 1 2 3 4 СН2 = С - СН - СН3 2,3 – диметилбутен - 1 Н3С СН3 1 2 3 4 СН3 – С = СН – СН2 2 – метилпентен - 2 Н3С 5 СН3 2 3 4 5 СН2 – С = С – СН2 3,4 – диметилгексен - 3 1 СН3 СН3 СН3 6СН3

Физические свойства Алкены – этен, пропен и бутен – при обычных условиях (20 °С, 1 атм) – газы, от С5Н10 до С18Н36 – жидкости, высшие алкены – твердые вещества. Алкены нерастворимы в воде, но хорошо растворимы в органических растворителях.

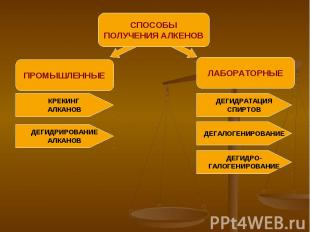
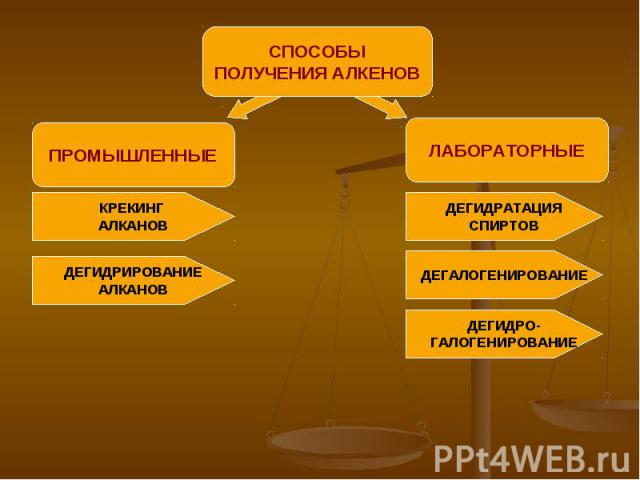
СПОСОБЫПОЛУЧЕНИЯ АЛКЕНОВ

ПРОМЫШЛЕННЫЙСПОСОБ ПОЛУЧЕНИЯ КРЕКИНГ НЕФТЕПРОДУКТОВАЛКАН → АЛКАН + АЛКЕН С БОЛЕЕ ДЛИННОЙ С МЕНЕЕ ДЛИНОЙ УГЛЕРОДНОЙ УГЛЕРОДНОЙ ЦЕПЬЮ ЦЕПЬЮ ПРИМЕР: t=400-700C С10Н22 → C5H12 + C5H10 декан пентан пентен

ПРОМЫШЛЕННЫЙСПОСОБ ПОЛУЧЕНИЯ ДЕГИДРИРОВАНИЕ АЛКАНОВ АЛКАН → АЛКЕН + ВОДОРОДПРИМЕР: Ni, t=500C Н3С - СН3 → Н2С = СН2 + Н2 этан этен (этилен)

ЛАБОРАТОРНЫЙСПОСОБ ПОЛУЧЕНИЯ ДЕГИДРАТАЦИЯ СПИРТОВСПИРТ → АЛКЕН + ВОДАПРИМЕР: t≥140C, Н Н Н2SO4(конц.) Н-С – С-Н → Н2С = СН2 + Н2О Н ОН этен (этилен)

ЛАБОРАТОРНЫЙСПОСОБ ПОЛУЧЕНИЯ ДЕГАЛОГЕНИРОВАНИЕПРИМЕР: tН2С – СН2 + Zn → Н2С = СН2 + ZnBr2 Br Br этен 1,2-дибромэтан (этилен)

ЛАБОРАТОРНЫЙСПОСОБ ПОЛУЧЕНИЯ ДЕГИДРОГАЛОГЕНИРОВАНИЕ УДАЛИТЬ ВОДОРОД ГАЛОГЕН ДЕЙСТВИЕПРИМЕР: спиртовой H H раствор Н-С–С-Н+KOH→Н2С=СН2+KCl+H2O Н Cl этен хлорэтан (этилен)

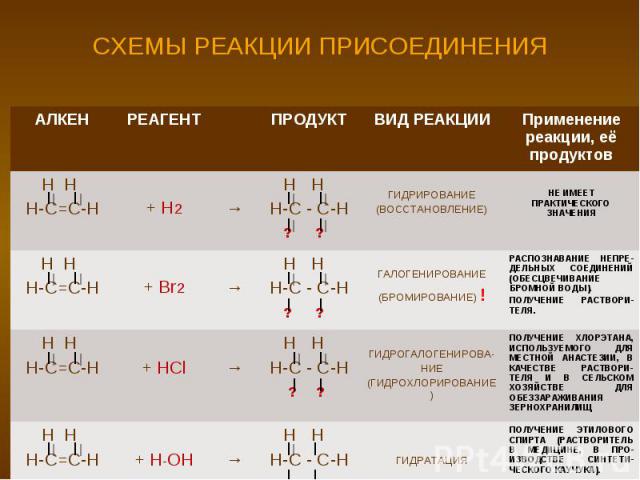
СХЕМЫ РЕАКЦИИ ПРИСОЕДИНЕНИЯ

РЕАКЦИЯ ПОЛИМЕРИЗАЦИИ Это процесс соединения одинаковых молекул в более крупные.ПРИМЕР: n CH2=CH2 (-CH2-CH2-)n этилен полиэтилен (мономер) (полимер) n – степень полимеризации, показывает число молекул, вступивших в реакцию-CH2-CH2- структурное звено

РЕАКЦИИ ОКИСЛЕНИЯ ГОРЕНИЕ АЛКЕНОВ ПРИМЕР: 2С2Н6 + 7О2 4СО2 + 6Н2О

РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНАГАНАТА КАЛИЯ (реакция Е.Е.Вагнера)Н2С=СН2 + [O] + H2O H2C - CH2 OH OH этиленгликоль (этандиол-1,2) ! Качественная реакция на непредельность углеводорода – на кратную связь.

Применение этилена


Ответьте, пожалуйста, на следующие вопросы: Какие углеводороды называются алкенами?Какова общая формула алкенов?Каковаособенность строения представителей гомологического ряда алкенов? Назовите первого представителя ряда.Какие способы получения алкенов вы знаете? Каким лабораторным способом можно получить алкены?Какие химические свойства обуславливает наличие кратной (двойной) связи в молекулах алкенов?Для чего используют алкены?

ДОМАШНЕЕ ЗАДАНИЕ Оценка «3»: & 4, Оценка «4»: & 4, Хомченко И.Г.: 20.21Оценка «5»: & 4, Составить уравнения реакций по цепочке превращений, используя материал по теме «Алкены» C2H5CL C2H4C2H6 C2H4C2H5OH

СПАСИБОЗА РАБОТУ!












![РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНАГАНАТА КАЛИЯ (реакция Е.Е.Вагнера)Н2С=СН2 + [O] + H2O H2C - CH2 OH OH этиленгликоль (этандиол-1,2) ! Качественная реакция на непредельность углеводорода – на кратную связь. РЕАКЦИИ ОКИСЛЕНИЯ МЯГКОЕ ОКИСЛЕНИЕ – ВЗАИМОДЕЙСТВИЕ С РАСТВОРОМ ПЕРМАНАГАНАТА КАЛИЯ (реакция Е.Е.Вагнера)Н2С=СН2 + [O] + H2O H2C - CH2 OH OH этиленгликоль (этандиол-1,2) ! Качественная реакция на непредельность углеводорода – на кратную связь.](https://fs1.ppt4web.ru/images/3958/60630/640/img14.jpg)
















