Презентация на тему: Аммиак

Автор- Салтанова Наталья Викторовна ГБОУ СОШ № 599 *
* Состав вещества Строение Свойства Получение Применение
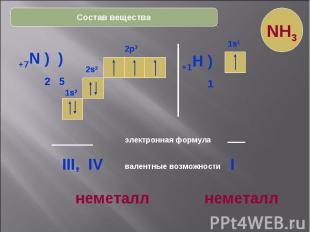
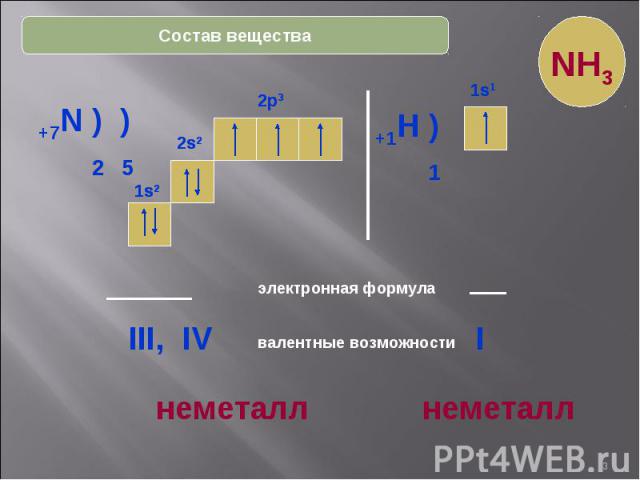
* Состав вещества +7N ) ) 2 5 2s2 2p3 электронная формула 2s2 1s2 1s2 2p3 валентные возможности III, IV +1H ) 1 1s1 1s1 I неметалл неметалл NH3
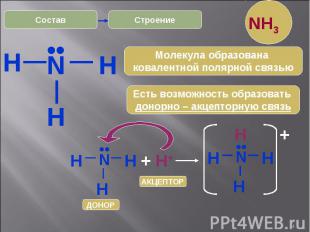
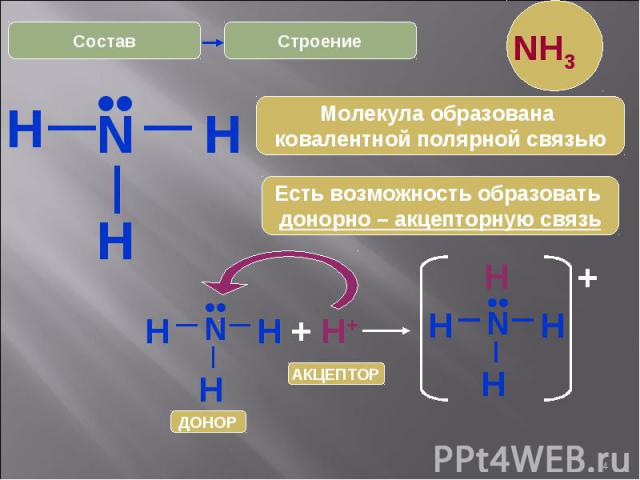
* H Строение N H H •• Есть возможность образовать донорно – акцепторную связь Молекула образована ковалентной полярной связью N H H H •• + H+ N H H H •• H + АКЦЕПТОР ДОНОР Состав NH3
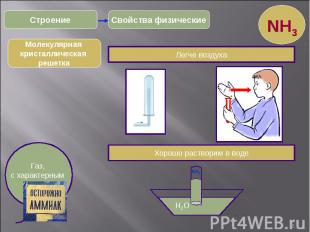
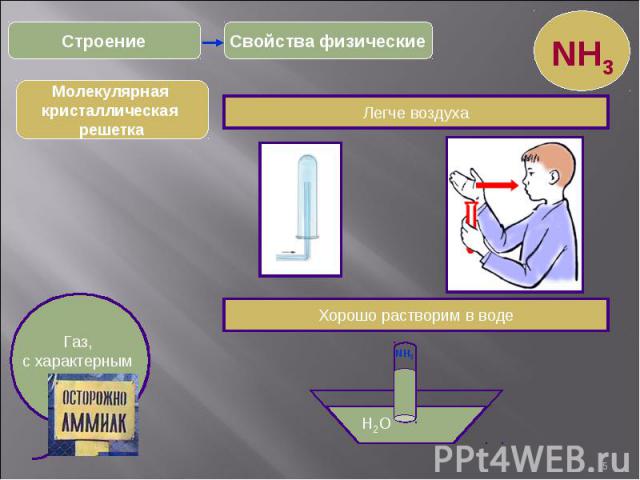
* Свойства физические Строение Газ, с характерным запахом. Легче воздуха Хорошо растворим в воде H2O NH3 NH3 Молекулярная кристаллическая решетка
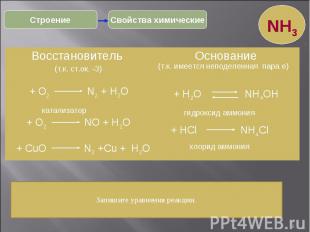
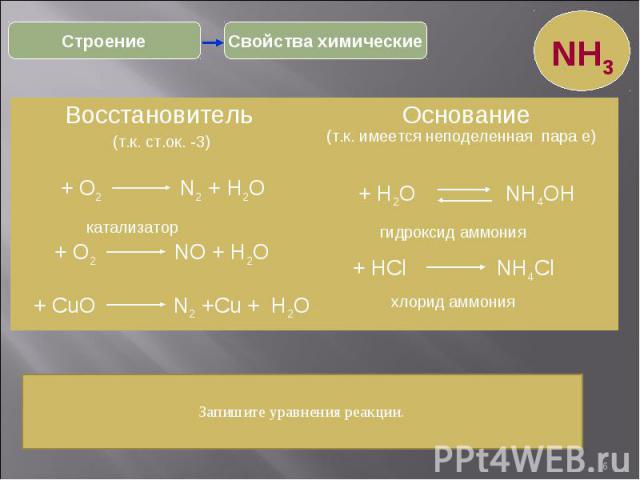
* Свойства химические Строение NH3 Восстановитель Основание (т.к. ст.ок. -3) (т.к. имеется неподеленная пара е) + О2 N2 + Н2О + О2 NО + Н2О катализатор + CuО N2 +Cu + Н2О + HCl NH4Cl + H2O NH4OH гидроксид аммония хлорид аммония Запишите уравнения реакции.
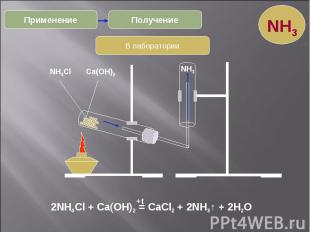
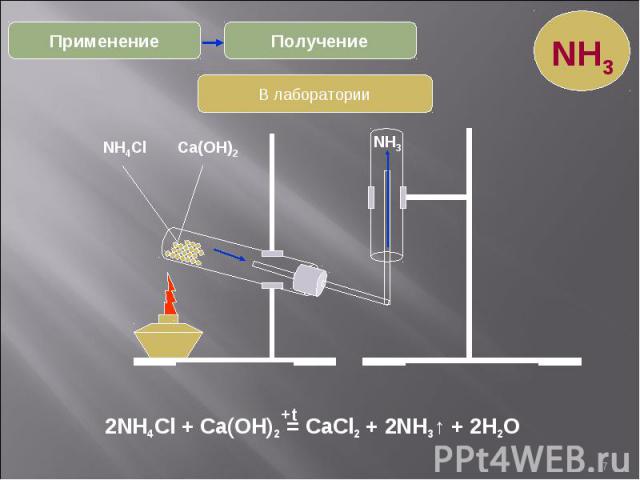
* Получение Применение В лаборатории 2NH4Cl + Ca(OH)2 = CaCl2 + 2NH3↑ + 2H2O +t NH4Cl Ca(OH)2 NH3 NH3
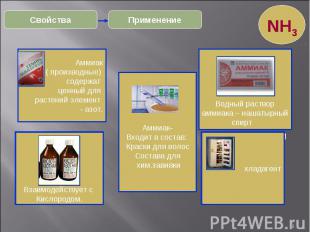
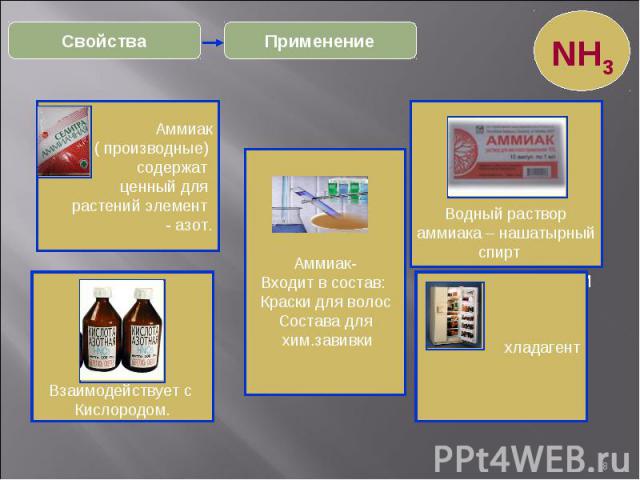
* Применение Свойства NH3 Рассчитайте массовую долю азота в аммиачной селитре Рассчитайте объем аммиака для приготовления 50г 5% - ного нашатырного спирта (при н.у.) Как осуществить превращения? NH3 → NO → NO2 HNO3 Составьте окислительно-восстановител Какой объем при нормальных условиях будет занимать 1 кг жидкого аммиака. Аммиак ( производные) содержат ценный для растений элемент - азот. Водный раствор аммиака – нашатырный спирт Взаимодействует с Кислородом. хладагент Аммиак- Входит в состав: Краски для волос Состава для хим.завивки
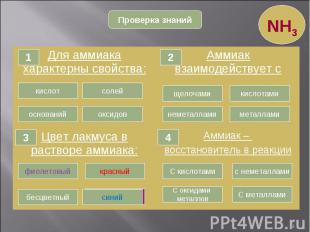
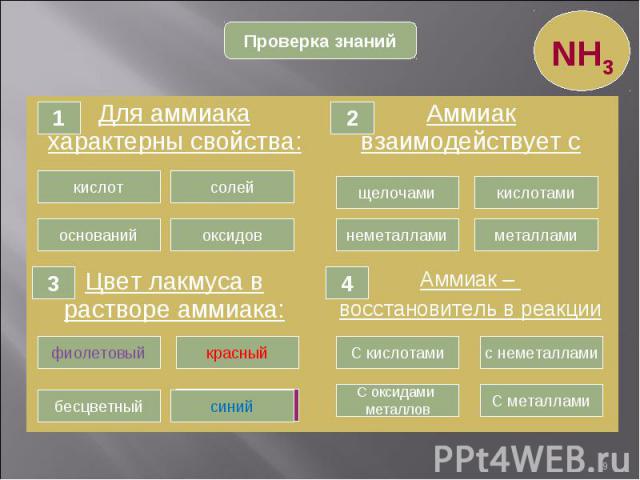
* NH3 Проверка знаний Для аммиака характерны свойства: Аммиак взаимодействует с Цвет лакмуса в растворе аммиака: Аммиак – восстановитель в реакции Правильно! Ошибка Ошибка Ошибка 1 кислот солей оксидов оснований 2 Ошибка Правильно! Ошибка Ошибка щелочами кислотами металлами неметаллами 3 Ошибка Правильно! Ошибка Ошибка Ошибка Ошибка Ошибка Правильно! фиолетовый бесцветный красный синий С кислотами С оксидами металлов с неметаллами С металлами 4