Презентация на тему: Окислительно-восстановительные равновесия в аналитической химии

Лекция № 20 Тема: Окислительно-восстановительные равновесия в аналитической химии

План лекции: Использование ОВР в аналитической химии. Типы ОВР. Количественное описание ОВР. Константа равновесия ОВР. Устойчивость водных растворов окислителей и восстановителей.

Использование ОВР в аналитической химии При пробоподготовке для переведения в раствор пробы. Для разделения смеси ионов. Для маскирования. Для проведения реакций обнаружения катионов и анионов в качественном химическом анализе. В титриметрическом анализе. В электрохимических методах анализа.

Например, при гипоксии (состояние кислородного голодания) происходит замедление транспорта Н+ и е – в дыхательной цепи и накопление восстановленных форм соединений. Этот сдвиг сопровождается снижением ОВ потенциала (ОВП) ткани и по мере углубления ишемии (местное малокровие, недостаточное содержание крови в органе или ткани) ОВП снижается. Это связано как с угнетением процессов окисления вследствие недостатка кислорода и нарушения каталитической способности окислительно-восстановительных ферментов, так и с активацией процессов восстановления в ходе гликолиза.

Типы ОВР 1. Межмолекулярные – изменяются степени окисления (С.О.) атомов элементов, входящих в состав разных веществ:

2. Внутримолекулярные – окислитель и восстановитель - атомы одной молекулы:

3. Самоокисления – самовосстановления (диспропорционирования) – один и тот же элемент повышает и понижает С.О. Cl2 - является окислителем и восстановителем.

Количественное описание ОВР Например, чем сильнее основание, тем больше его сродство в протону. Также и сильный окислитель обладает большим сродством к электрону. Например, в кислотно-основных реакциях участвует растворитель (вода), отдавая и принимая протон, а в ОВР вода тоже может терять или присоединять электрон. Например, для проведения кислотно-основных реакций необходимы как кислота, так и основание, а в ОВР – и окислитель и восстановитель.

Рассматривая ОВ пару в целом, можно записать схематичное уравнение реакции: Ox + nē = Red Равновесие в растворе можно описать с помощью равновесного потенциала, который зависит от состава раствора по уравнению Нернста:

При температуре 298 К уравнение Нернста принимает вид:
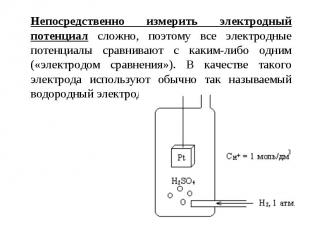
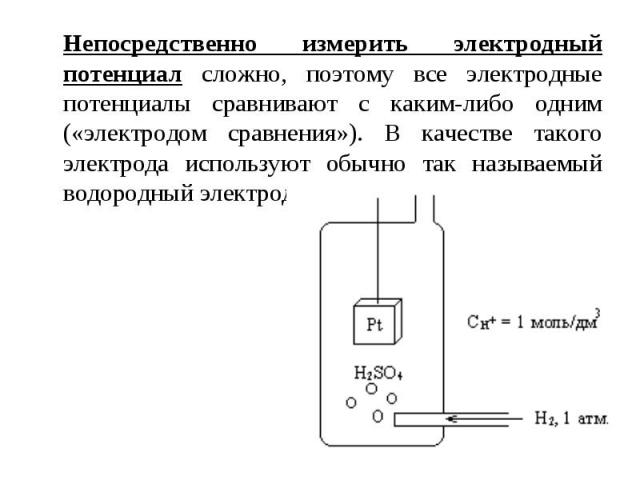
Непосредственно измерить электродный потенциал сложно, поэтому все электродные потенциалы сравнивают с каким-либо одним («электродом сравнения»). В качестве такого электрода используют обычно так называемый водородный электрод.

В уравнении Нернста можно использовать вместо активностей ионов их концентрации, но тогда необходимо знать коэффициенты активностей ионов:

На силу окислителя и восстановителя могут влиять: значение рН, реакции осаждения реакции комплексообразования. Тогда свойства редокс-пары будут описываться реальным потенциалом.

Для расчета реального потенциала полуреакций, получаемых сочетанием ОВР и реакций осаждения, используются формулы: если окисленная форма представляет собой малорастворимое соединение:

если восстановленная форма представляет собой малорастворимое соединение:

Сочетание ОВР и реакций комплексообразования если окисленная форма связана в комплекс:

если восстановленная форма связана в комплекс:

если обе формы связаны в комплекс:

Сочетание ОВР и реакций протонирования если протонируется окисленная форма:

если протонируется восстановленная форма:

если протонируются обе формы:

если реакция протекает по следующему уравнению: Ox + mH+ + nē = Red + H2O тогда

Константа равновесия ОВР Расчет константы равновесия для реакции: Sn2+ + 2Fe3+ = Sn4+ + 2Fe2+ Константа равновесия рассчитывается:

Выражения для реальных ОВ потенциалов каждой редокс-пары будут выглядеть следующим образом:

В условиях равновесия:

Проведя математические операции, получим: К = 1021

Используя приведенное вычисление константы равновесия, получим для любого обратимого ОВ процесса при 20 0С следующее уравнение:

Например, в цериметрии (окислитель Се4+): Fe2+ + Се4+ = Fe3+ + Се3+ К = 1011,4 = 2,3 · 1011

Устойчивость водных растворов окислителей и восстановителей Наибольшее практическое значение имеет полуреакция: О2 + 4Н+ + 4ē = 2Н2О Е = 1,23 В Термодинамические неустойчивыми являются водные растворы восстановителей с потенциалом < 1,23 В и окислителей с Е > 1,23 В.