Презентация на тему: Аллотропия кислорода

Аллотропия кислорода Ахрамович Наталья Михайловнаучитель химии ГБОУ СОШ № 450 Курортного районаСанкт – Петербурга

Оглавление Аллотропия.Аллотропные модификации кислорода.История открытия кислорода и озона.Нахождение в природе.Строение молекулы.Физические свойства.Химические свойства.Получение в природе.Значение кислорода и озона в природе.Проверь себя.Литература.
Аллотропия(от греческих слов allos – другой и tropos – образ, способ) Способность атомов одного элемента образовывать несколько простых веществ.

Аллотропные модификации кислорода. О2 кислород (простое вещество)К. В. Шееле 1772 г.Дж. Пристли 1774 г.А. Лавуазье 1777г. «рождающий кислоты» О3 озон (простое вещество)Х. Ф. Шёнбейн 1839 г. «пахнущий»

1772 год. Карл Вильгельм Шееле (шведский учёный) хотел раскрыть загадку огня и при этом неожиданно обнаружил, что воздух — не элемент, а смесь двух газов, которые он называл воздухом «огненным». В 1777 г. был опубликован труд Шееле «Химический трактат о воздухе и огне». Однако приоритет открытия кислорода принадлежит Джозефу Пристли, который описал его в 1774 г. независимо от Шееле.

1774 год. Джозеф Пристли, изучая состав воздуха, пытался выяснить, какие его составляющие могут выделиться из химических веществ при их нагревании. Нагревая оксид ртути (II), он получил газ и назвал его «дефлогистированным воздухом». Исследуя свойства полученного газа, Пристли обнаружил, что зажженная свеча горела в нем ослепительно ярко и что он поддерживает дыхание. Прибор для получения кислорода ( Д.Пристли )

Впервые количественный состав воздуха установил французский ученый Антуан Лоран Лавуазье ( 1775 г. ) По результатам своего известного 12-дневного опыта он сделал вывод, что весь воздух в целом состоит из кислорода, пригодного для дыхания и горения, и азота, неживого газа, в пропорциях 1/5 и 4/5 объема соответственно. Ученый предложил «жизненный воздух» переименовать в «кислород», поскольку при сгорании в кислороде большинство веществ превращается в кислоты, а «удушливый воздух» – в «азот», т.к. он не поддерживает жизнь, вредит жизни. Опыт Лавуазье

Впервые озон обнаружил в 1785 голландский физик М. ван Марум по характерному запаху (свежести) и окислительным свойствам, которые приобретает воздух после пропускания через него электрических искр. Однако как новое вещество он описан не был, ван Марум считал, что образуется особая «электрическая материя».
Кристиан Фридрих Шёнбей Термин озон предложен немецким химиком X.Ф. Шёнбейном в 1840 г., вошёл в словари в конце 19-ого века. Многие источники именно ему отдают приоритет открытия озона в 1839 г.

Нахождение в природе. О2 Воздух – 21% по объёму 23% по массе. О3Атмосфера (верхний слой) – озоновый экран Земли.

Строение молекулы. О2 О3 О = О неполярная полярная Mr = 32 Mr = 48 устойчив неустойчив

Физические свойства.

Химические свойства О2 Сильный окислитель, но не окисляет Au и Pt, окисляет многие металлы, образуя оксиды. 2Cu + O2 = 2CuO Взаимодействует со всеми неметаллами, кроме галогенов, за исключением F S+ O2 = SO2 Горение сложных веществ: 2H2S + 3O2 = 2H2O + 2SO2 О3 Очень сильный окислитель, более реакционноспособнее, чем двухатомный кислород. Окисляет почти все металлы (за исключением золота, платины и иридия). 2Ag + O3 = Ag2O + O2 (комнатная температура) Окисляет многие неметаллы. C + 2O3 = CO2+ 2O2 Окисление сложных веществ2KI + O3 + H2O = 2KOH + I2 +O2

Получение в природе. О26СО2 + 6Н2О = С6Н12О6 + 6О2 Процесс фотосинтеза. О3 3О2 ⇄ 2О3 Грозовые разряды.
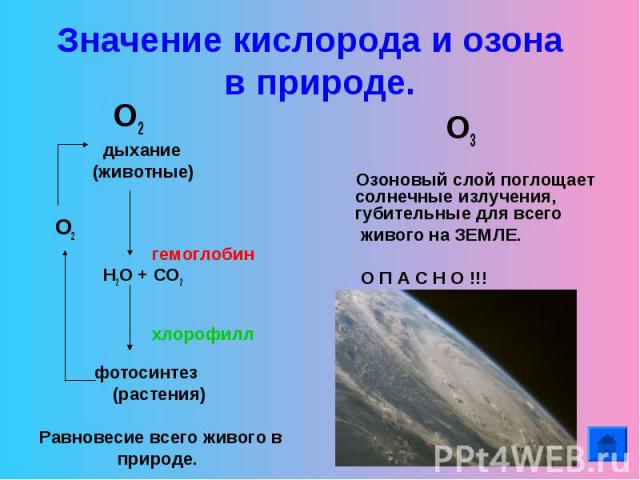
Значение кислорода и озона в природе. О2 дыхание (животные) О2 гемоглобин Н2О + СО2 хлорофилл фотосинтез (растения)Равновесие всего живого в природе. О3 Озоновый слой поглощает солнечные излучения, губительные для всего живого на ЗЕМЛЕ. О П А С Н О !!! «озоновые дыры»

Проверь себя! 1. Что такое аллотропия? 2. Назовите фамилии трех ученых, открывших кислород. 3. В результате какого процесса в природе образуется кислород? 4. Какая химическая реакция происходит при грозовых разрядах? 5. Газ, образующий защитную оболочку Земли. 6. В чём одна из причин многообразия веществ?

Литература, интернет-ресурсы. О.С.Габриелян « Химия. 9 кл.» М. Дрофа, 2010 г..Ю.М.Малиновская «Химия. 6 кл.» (пропедевтический курс) С-Пб ТОО фирма Икар, 1999г.Н.Г.Назина «Введение в химию» С-Пб, изд-во НИИХ С-ПбГУ, 2006г.http://www.newsland.ru/ http//www.alhimik.ru/http://www.xumuk.ru/spravochnik/

Спасибоза внимание!