Презентация на тему: Неметаллы. Аллотропия

Неметаллы. Аллотропия Куцапкина Людмила Васильевнаучитель химии ГБОУ гимназии № 343Невского района Санкт- Петербурга

Положение неметаллов в ПС Д.И.Менделеева.Неметаллы расположены в правом верхнем углу ПС (вдоль и над диагональю B-At). Всего 22 элемента- неметалла в Периодической системеЭлементы-неметаллы располагаются только в главных подгруппах ПС.

Особенности атомного строения элементов-неметаллов.Для атомов-неметаллов характерно:Небольшой атомный радиус ( в сравнении с радиусами атомов-металлов одного с ними периода).Большее число электронов на внешнем уровне (4-8), исключения Н, Не, В.Происходит заполнение электронами только внешнего энергетического уровня. Для элементов-неметаллов характерны высокие значения электроотрицательности.

Для неметаллов - простых веществ более характерно различие свойствах (физических и химических), чем их общность. Разнообразие свойств неметаллов объясняется, тем, что неметаллы могут иметь два типа кристаллической решетки: молекулярную (все газы, белый фосфор, сера, йод) и атомную (бор, кристаллический кремний, алмаз, графит). Для сравнения – металлы имеют металлическую кристаллическую решетку.

Для неметаллов (простых веществ) характерны все 3 агрегатных состояния при обычных условиях (сравнить – все металлы, кроме ртути, в обычных условиях твердые вещества)Твердые вещества: различные модификации серы, йод кристаллический, графит, фосфор, уголь активированный, кристаллический или аморфный кремний, бор (единственное жидкое при обычных условиях простое вещество – это бром). Газообразные вещества – неметаллы – это О2, N2, H2, Cl2, F2.

Для неметаллов характерна разнообразная цветовая гамма: белый ,черный ,красный фосфор, красно-бурый бром, желтая сера, фиолетовый йод, черный графит, алмазы разного цвета, бесцветный – кислород, азот, водород (тогда как абсолютное большинство металлов имеют серебристо-белый цвет).Температуры плавления: от 38000 С (графит) до -2100 С (азот). Для сравнения – металлы: от 33800 С (вольфрам) до -38,90 С (ртуть).Некоторые неметаллы электропроводны (графит, кремний), имеют металлический блеск (йод, графит, кремний). По этим признакам напоминают металлы, но все они – хрупкие вещества.

Среди неметаллов распространено явление аллотропии. Один элемент может образовывать несколько простых веществ.Причины аллотропии:Разные типы кристаллических решеток (белый фосфор Р4 – молекулярная, красный фосфор Р – атомная).Разная структура кристаллической решетки (алмаз – тетраэдрическая, графит – слоистая).Разный состав молекул аллотропных модификаций (О2 и О3).

Кислород- газ, без цвета, вкуса и запаха, плохо растворим в воде, в жидком состоянии светло-голубой, в твердом – синий. Озон- светло-синий газ, темно-голубая жидкость, в твердом состоянии темно-фиолетовый, имеет сильный запах, в 10 раз лучше, чем кислород, растворим в воде.

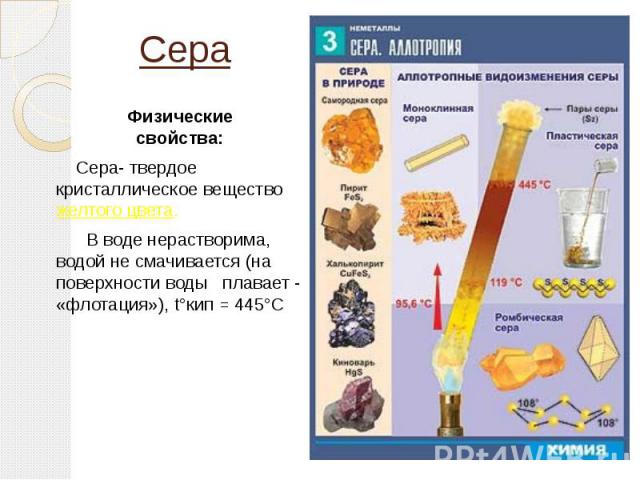
Физические свойства: Сера- твердое кристаллическое вещество желтого цвета. В воде нерастворима, водой не смачивается (на поверхности воды плавает - «флотация»), t°кип = 445°С
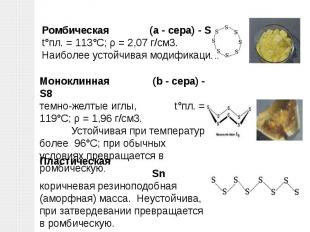
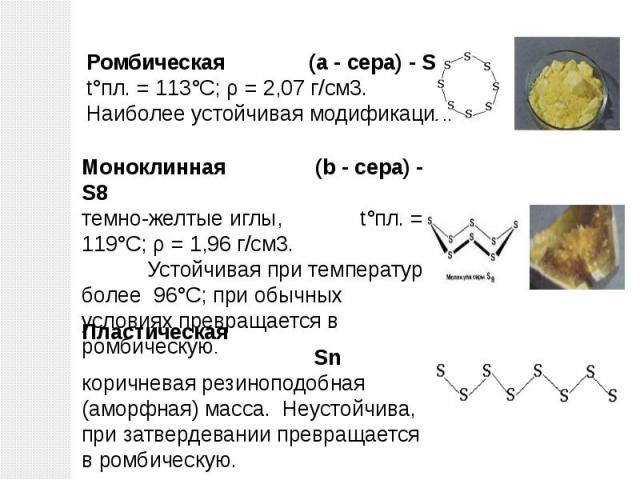
Ромбическая (a - сера) - S8t°пл. = 113°C; ρ = 2,07 г/см3. Наиболее устойчивая модификация. Моноклинная (b - сера) - S8темно-желтые иглы, t°пл. = 119°C; ρ = 1,96 г/см3. Устойчивая при температуре более 96°С; при обычных условиях превращается в ромбическую. Пластическая Snкоричневая резиноподобная (аморфная) масса. Неустойчива, при затвердевании превращается в ромбическую.

Элементарный фосфор в обычных условиях представляет собой несколько устойчивых аллотропических модификаций; вопрос аллотропии фосфора сложен и до конца не решён. Обычно выделяют четыре модификации простого вещества — белый, красный, чёрный и металлический фосфор. Иногда их ещё называют главными аллотропными модификациями, подразумевая при этом, что все остальные являются разновидностью указанных четырёх. В обычных условиях существует только три аллотропических модификации фосфора, а в условиях сверхвысоких давлений — также металлическая форма. Все модификации различаются по цвету, плотности и другим физическим характеристикам; заметна тенденция к резкому убыванию химической активности при переходе от белого к металлическому фосфору и нарастанию металлических свойств.

Биологическая роль соединений фосфора Фосфор присутствует в живых клетках в виде орто- и пирофосфорной кислот, входит в состав нуклеотидов, нуклеиновых кислот, фосфопротеидов, фосфолипидов, коферментов, ферментов. Кости человека состоят из гидроксилапатита 3Са3(РО4)3·Ca(OH)2. В состав зубной эмали входит фторапатит. Основную роль в превращениях соединений фосфора в организме человека и животных играет печень. Обмен фосфорных соединений регулируется гормонами и витамином D. Суточная потребность человека в фосфоре 800—1500 мг. При недостатке фосфора в организме развиваются различные заболевания костей.

Белый, красный, чёрный и металлический фосфор

Белый фосфор представляет собой белое вещество (из-за примесей может иметь желтоватый оттенок). По внешнему виду он очень похож на очищенный воск или парафин, легко режется ножом и деформируется от небольших усилий.Белый фосфор имеет молекулярное строение; формула P4.Химически белый фосфор чрезвычайно активен, медленно окисляется кислородом воздуха уже при комнатной температуре и светится (бледно-зелёное свечение) ; ядовит. Открыт гамбургским алхимиком Хеннигом Брандом в 1669 году

Красный фосфор имеет формулу Рn и представляет собой полимер со сложной структурой. Имеет оттенки от пурпурно-красного до фиолетового, а в литом состоянии - тёмно-фиолетовый с медным оттенком, имеет металлический блеск. Химическая активность красного фосфора значительно ниже, чем у белого; ему присуща исключительно малая растворимость. Ядовитость его в тысячи раз меньше, чем у белого. Получен в 1847 году в Швеции австрийским химиком А. Шрёттером

Чёрный фосфор представляет собой чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, и с полностью отсутствующей растворимостью в воде или органических растворителях.Проводит электрический ток и имеет свойства полупроводника. Впервые чёрный фосфор был получен в 1914 году американским физиком П. У. Бриджменом

При 8,3·1010 Па чёрный фосфор переходит в новую, ещё более плотную и инертную металлическую фазу с плотностью 3,56 г/см³, а при дальнейшем повышении давления до 1,25·1011 Па — ещё более уплотняется и приобретает кубическую кристаллическую решётку, при этом его плотность возрастает до 3,83 г/см³. Металлический фосфор очень хорошо проводит электрический ток.

В свободном виде углерод встречается в нескольких аллотропных модификациях – алмаз, графит, карбин, крайне редко фуллерены. В лабораториях также были синтезированы многие другие модификации: новые фуллерены, нанотрубки, наночастицы и др.

Бесцветное, прозрачное, сильно преломляющее свет вещество. Алмаз тверже всех найденных в природе веществ, но при этом довольно хрупок. Он настолько тверд, что оставляет царапины на большинстве материалов. Плотность алмаза – 3,5 г/см3, tплав=3730С, tкип=4830оС. Алмаз можно получить из графита при p > 50 тыс. атм. и tо = 1200оC В алмазе каждый 4-х валентный атом углерода связан с другим атомом углерода ковалентной связью и количество таких связанных в каркас атомов чрезвычайно велико.

Куллинан (алмаз)- 621,35 грамма, размеры: 100х65х50 мм Бриллианты: Куллинан-1, Куллинан-2, Куллинан-3 и 4

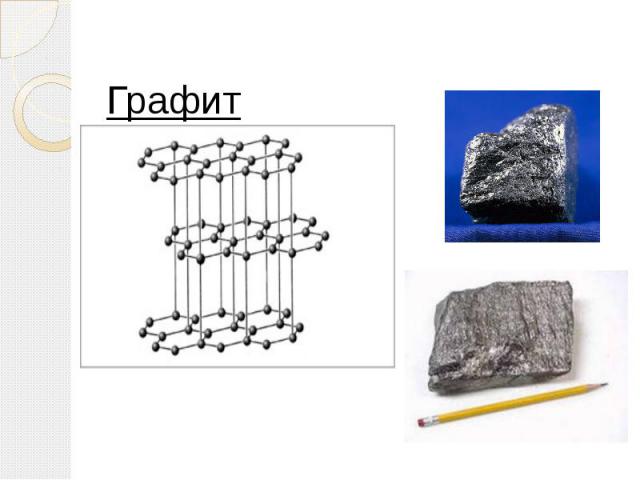
Графит – устойчивая при нормальных условиях аллотропная модификация углерода, имеет серо-черный цвет и металлический блеск, кажется жирным на ощупь, очень мягок и оставляет черные следы на бумаге. Атомы углерода в графите расположены отдельными слоями, образованными из плоских шестиугольников. Каждый атом углерода на плоскости окружен тремя соседними, расположенными вокруг него в виде правильного треугольника. Графит характеризуется меньшей плотностью и твердостью, а также графит может расщепляться на тонкие чешуйки. Чешуйки легко прилипают к бумаге – вот почему из графита делают грифели карандашей. В пределах шестиугольников возникает склонность к металлизации, что объясняет хорошую тепло- и электропроводность графита, а также его металлический блеск.

Графит

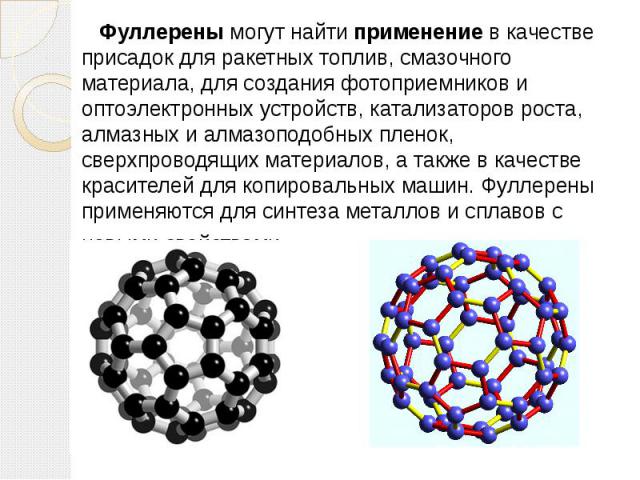
Фуллерены – класс химических соединений, молекулы которых состоят только из углерода, число атомов которого четно, от 32 и более 500, они представляют по структуре выпуклые многогранники, построенные из правильных пяти- и шестиугольников. Третья форма чистого углерода является молекулярной. Это означает, что минимальным элементом ее структуры является не атом, а молекула углерода, представляющая собой замкнутую поверхность, которая имеет форму сферы. В фуллерене плоская сетка шестиугольников (графитовая сетка) свернута и сшита в замкнутую сферу. При этом часть шестиугольников преобразуется в пятиугольники. Образуется структура – усеченный икосаэдр. Каждая вершина этой фигуры имеет трех ближайших соседей. Каждый шестиугольник граничит с тремя шестиугольниками и тремя пятиугольниками, а каждый пятиугольник граничит только с шестиугольниками.
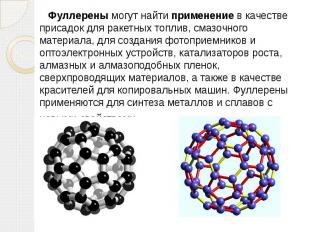
Фуллерены могут найти применение в качестве присадок для ракетных топлив, смазочного материала, для создания фотоприемников и оптоэлектронных устройств, катализаторов роста, алмазных и алмазоподобных пленок, сверхпроводящих материалов, а также в качестве красителей для копировальных машин. Фуллерены применяются для синтеза металлов и сплавов с новыми свойствами.

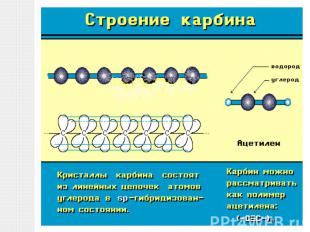
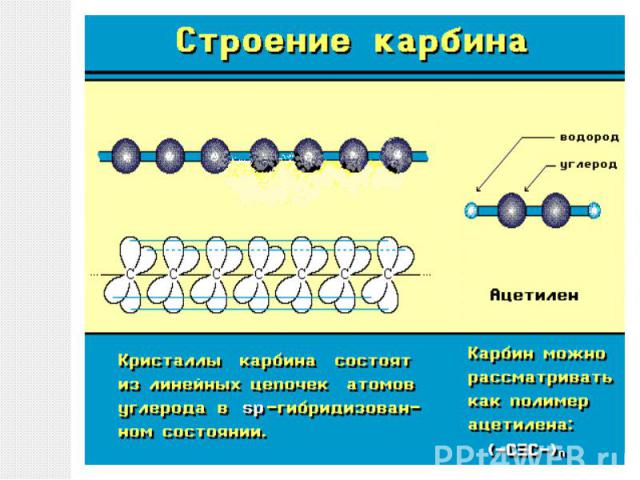
Карбин конденсируется в виде белого углеродного осадка на поверхности при облучении пирографита лазерным пучком света. Кристаллическая форма карбина состоит из параллельно ориентированных цепочек углеродных атомов с sp-гибридизацией валентных электронов в виде прямолинейных макромолекул полиинового ( -С= С-С= С-... ) или кумуленового (=С=С=С=...) типов.