Презентация на тему: Комплексные соединения

Комплексные соединения.

Координационная теория А.Вернера В 1893 г. швейцарским химиком-неоргаником Альфредом Вернером (1866–1919) была сформулирована теория, позволившая понять строение и некоторые свойства комплексных соединений и названная координационной теорией. Поэтому комплексные соединения часто называют координационными соединениями.Соединения, в состав которых входят сложные ионы, существующие как в кристалле, так и в растворе, называются комплексными, или координационными.

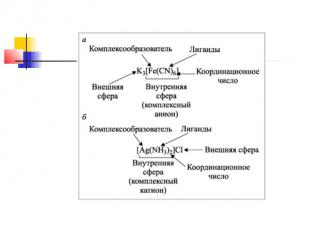
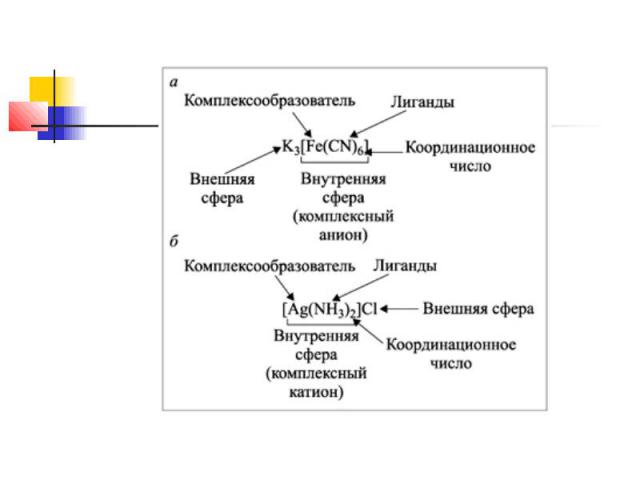
Состав. Согласно теории Вернера центральное положение в комплексных соединениях занимает, как правило, ион металла, который называют центральным ионом, или комплексообразователем.

Комплексообразователь – частица (атом, ион или молекула), координирующая (располагающая) вокруг себя другие ионы или молекулы.

Комплексообразователь обычно имеет положительный заряд, является d-элементом, проявляет амфотерные свойства, имеет координационное число 4 или 6. Вокруг комплексообразователя располагаются (координируются) молекулы или кислотные остатки – лиганды (адденды).

Лиганды – частицы (молекулы и ионы), координируемые комплексообразователем и имеющие с ним непосредственно химические связи (например, ионы: Cl–, I–, NO3–, OH–; нейтральные молекулы: NH3, H2O, CO).

Лиганды не связаны друг с другом, так как между ними действуют силы отталкивания. Когда лигандами являются молекулы, между ними возможно молекулярное взаимодействие. Координация лигандов около комплексообразователя является характерной чертой комплексных соединений

Классификация Большое многообразие комплексных соединений и их свойств не позволяет создать единую классификацию. Однако можно группировать вещества по некоторым отдельным признакам.
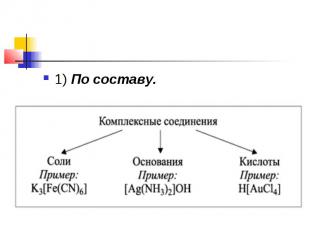
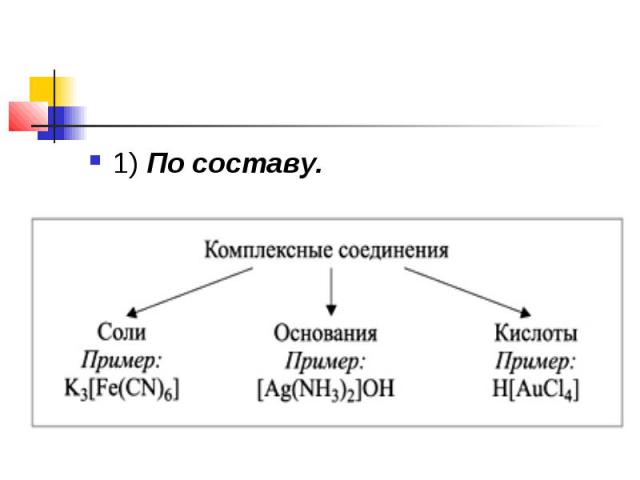
1) По составу.

2) По типу координируемых лигандов.а) Аквакомплексы – это комплексные катионы, в которых лигандами являются молекулы H2O. Их образуют катионы металлов со степенью окисления +2 и больше, причем способность к образованию аквакомплексов у металлов одной группы периодической системы уменьшается сверху вниз.Примеры аквакомплексов:[Al(H2O)6]Cl3, [Cr(H2O)6](NO3)3.

б)Гидроксокомплексы – это комплексные анионы, в которых лигандами являются гидроксид-ионы OH–. Комплексообразователями являются металлы, склонные к проявлению амфотерных свойств – Be, Zn, Al, Cr.Например: Na[Al(OH)4], Ba[Zn(OH)4].в) Аммиакаты – это комплексные катионы, в которых лигандами являются молекулы NH3. Комплексообразователями являются d-элементы.Например: [Cu(NH3)4]SO4, [Ag(NH3)2]Cl.

г) Ацидокомплексы – это комплексные анионы, в которых лигандами являются анионы неорганических и органических кислот.Например: K3[Al(C2O4)3], Na2[Zn(CN)4], K4[Fe(CN)6].

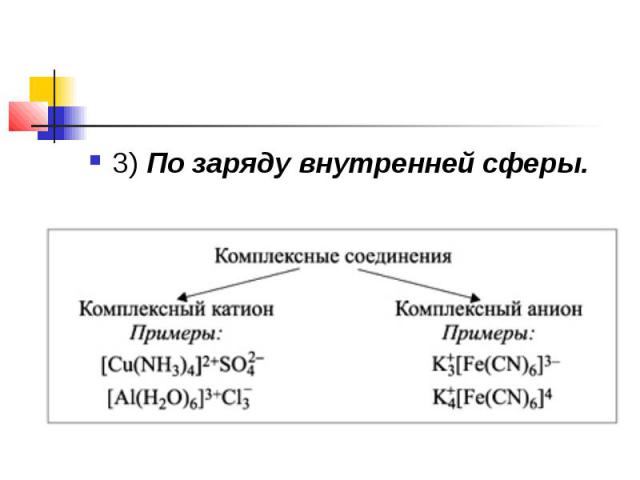
3) По заряду внутренней сферы.

Номенклатура комплексных соединений Наибольшее распространение имеет номенклатура, рекомендованная IUPAC. Название комплексного аниона начинается с обозначения состава внутренней сферы: число лигандов обозначается греческими числительными: 2–ди, 3–три, 4–тетра, 5–пента, 6–гекса и т.д., далее следуют названия лигандов, к которым прибавляют соединительную гласную «о»: Cl– – хлоро-, CN– – циано-, OH– – гидроксо- и т.п.

Если у комплексообразователя переменная степень окисления, то в скобках римскими цифрами указывают его степень окисления, а его название с суффиксом -ат: Zn – цинкат, Fe – феррат(III), Au – аурат(III). Последним называют катион внешней сферы в родительном падеже
![Примеры:K3[Fe(CN)6] – гексацианоферрат(III) калия,K4[Fe(CN)6] – гексацианоферрат Примеры:K3[Fe(CN)6] – гексацианоферрат(III) калия,K4[Fe(CN)6] – гексацианоферрат](https://fs1.ppt4web.ru/images/3958/62583/310/img16.jpg)
Примеры:K3[Fe(CN)6] – гексацианоферрат(III) калия,K4[Fe(CN)6] – гексацианоферрат(II) калия,K2[Zn(OH)4] – тетрагидроксоцинкат калия.
![Например:[Cu(NH3)4]SO4 – сульфат тетраамминмеди(II),[Al(H2O)6]Cl3 – хлорид гекса Например:[Cu(NH3)4]SO4 – сульфат тетраамминмеди(II),[Al(H2O)6]Cl3 – хлорид гекса](https://fs1.ppt4web.ru/images/3958/62583/310/img17.jpg)
Например:[Cu(NH3)4]SO4 – сульфат тетраамминмеди(II),[Al(H2O)6]Cl3 – хлорид гексаакваалюминия.

Химические свойства комплексных соединений 1. В растворе комплексные соединения ведут себя как сильные электролиты, т.е. полностью диссоциируют на катионы и анионы.[Pt(NH3)4]Cl2 = Pt(NH3)4] 2+ + 2Cl –,K2[PtCl4] = 2K+ + [PtCl4] 2–

2. При действии сильных кислот происходит разрушение гидроксокомплексов а) при недостатке кислоты Na3[Al(OH)6] + 3HCl = 3NaCl + Al(OH)3 + 3H2O;б) при избытке кислоты Na3[Al(OH)6] + 6HCl = 3NaCl + AlCl3 + 6H2O.

3. Нагревание (термолиз) всех аммиакатов приводит к их разложению, например:[Cu(NH3)4]SO4 = CuSO4 + 4NH3 .

Значение комплексных соединений Координационные соединения имеют исключительно большое значение в природе. Достаточно сказать, что почти все ферменты, многие гормоны, лекарства, биологически активные вещества представляют собой комплексные соединения. Например, гемоглобин крови, благодаря которому осуществляется перенос кислорода от легких к клеткам ткани, является комплексным соединением, содержащим железо, а хлорофилл, ответственный за фотосинтез в растениях, – комплексным соединением магния.

Значительную часть природных минералов, в том числе полиметаллических руд и силикатов, также составляют координационные соединения. Более того, химические методы извлечения металлов из руд, в частности меди, вольфрама, серебра, алюминия, платины, железа, золота и других, также связаны с образованием легкорастворимых, легкоплавких или летучих комплексов. Например: Na3[AlF6] – криолит, KNa3[AlSiO4]4 – нефелин (минералы, комплексные соединения, содержащие алюминий).

Современная химическая отрасль промышленности широко использует координационные соединения как катализаторы при синтезе высокомолекулярных соединений, при химической переработке нефти, в производстве кислот.

Задания. Письменно дать характеристику следующим комплексным соединениям по строению и классифицировать по признакам: K3[Cr(OH)6], [Cr(H2O)6](NO3)3, Na2[Zn(CN)4], [Ag(NH3)2]OH.

Написать уравнения реакций, при помощи которых можно осуществить превращения:










![б)Гидроксокомплексы – это комплексные анионы, в которых лигандами являются гидроксид-ионы OH–. Комплексообразователями являются металлы, склонные к проявлению амфотерных свойств – Be, Zn, Al, Cr.Например: Na[Al(OH)4], Ba[Zn(OH)4].в) Аммиакаты – это … б)Гидроксокомплексы – это комплексные анионы, в которых лигандами являются гидроксид-ионы OH–. Комплексообразователями являются металлы, склонные к проявлению амфотерных свойств – Be, Zn, Al, Cr.Например: Na[Al(OH)4], Ba[Zn(OH)4].в) Аммиакаты – это …](https://fs1.ppt4web.ru/images/3958/62583/640/img11.jpg)
![г) Ацидокомплексы – это комплексные анионы, в которых лигандами являются анионы неорганических и органических кислот.Например: K3[Al(C2O4)3], Na2[Zn(CN)4], K4[Fe(CN)6]. г) Ацидокомплексы – это комплексные анионы, в которых лигандами являются анионы неорганических и органических кислот.Например: K3[Al(C2O4)3], Na2[Zn(CN)4], K4[Fe(CN)6].](https://fs1.ppt4web.ru/images/3958/62583/640/img12.jpg)


![Примеры:K3[Fe(CN)6] – гексацианоферрат(III) калия,K4[Fe(CN)6] – гексацианоферрат(II) калия,K2[Zn(OH)4] – тетрагидроксоцинкат калия. Примеры:K3[Fe(CN)6] – гексацианоферрат(III) калия,K4[Fe(CN)6] – гексацианоферрат(II) калия,K2[Zn(OH)4] – тетрагидроксоцинкат калия.](https://fs1.ppt4web.ru/images/3958/62583/640/img16.jpg)
![Например:[Cu(NH3)4]SO4 – сульфат тетраамминмеди(II),[Al(H2O)6]Cl3 – хлорид гексаакваалюминия. Например:[Cu(NH3)4]SO4 – сульфат тетраамминмеди(II),[Al(H2O)6]Cl3 – хлорид гексаакваалюминия.](https://fs1.ppt4web.ru/images/3958/62583/640/img17.jpg)
![Химические свойства комплексных соединений 1. В растворе комплексные соединения ведут себя как сильные электролиты, т.е. полностью диссоциируют на катионы и анионы.[Pt(NH3)4]Cl2 = Pt(NH3)4] 2+ + 2Cl –,K2[PtCl4] = 2K+ + [PtCl4] 2– Химические свойства комплексных соединений 1. В растворе комплексные соединения ведут себя как сильные электролиты, т.е. полностью диссоциируют на катионы и анионы.[Pt(NH3)4]Cl2 = Pt(NH3)4] 2+ + 2Cl –,K2[PtCl4] = 2K+ + [PtCl4] 2–](https://fs1.ppt4web.ru/images/3958/62583/640/img18.jpg)
![2. При действии сильных кислот происходит разрушение гидроксокомплексов а) при недостатке кислоты Na3[Al(OH)6] + 3HCl = 3NaCl + Al(OH)3 + 3H2O;б) при избытке кислоты Na3[Al(OH)6] + 6HCl = 3NaCl + AlCl3 + 6H2O. 2. При действии сильных кислот происходит разрушение гидроксокомплексов а) при недостатке кислоты Na3[Al(OH)6] + 3HCl = 3NaCl + Al(OH)3 + 3H2O;б) при избытке кислоты Na3[Al(OH)6] + 6HCl = 3NaCl + AlCl3 + 6H2O.](https://fs1.ppt4web.ru/images/3958/62583/640/img19.jpg)
![3. Нагревание (термолиз) всех аммиакатов приводит к их разложению, например:[Cu(NH3)4]SO4 = CuSO4 + 4NH3 . 3. Нагревание (термолиз) всех аммиакатов приводит к их разложению, например:[Cu(NH3)4]SO4 = CuSO4 + 4NH3 .](https://fs1.ppt4web.ru/images/3958/62583/640/img20.jpg)



![Задания. Письменно дать характеристику следующим комплексным соединениям по строению и классифицировать по признакам: K3[Cr(OH)6], [Cr(H2O)6](NO3)3, Na2[Zn(CN)4], [Ag(NH3)2]OH. Задания. Письменно дать характеристику следующим комплексным соединениям по строению и классифицировать по признакам: K3[Cr(OH)6], [Cr(H2O)6](NO3)3, Na2[Zn(CN)4], [Ag(NH3)2]OH.](https://fs1.ppt4web.ru/images/3958/62583/640/img24.jpg)