Презентация на тему: Химия «Соли»

ВАЖНЕЙШИЕ КЛАССЫ НЕОРГАНИЧЕСКИХ СОЕДИНЕНИЙ 900igr.net

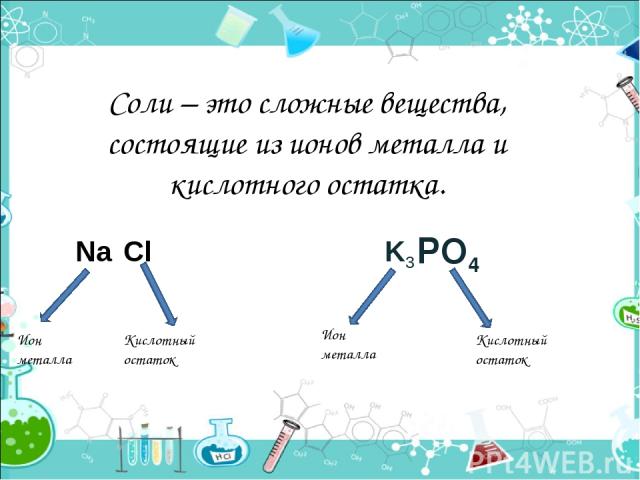
Соли – это сложные вещества, состоящие из ионов металла и кислотного остатка. PO4 Ион металла Кислотный остаток Ион металла Кислотный остаток Na Cl K3

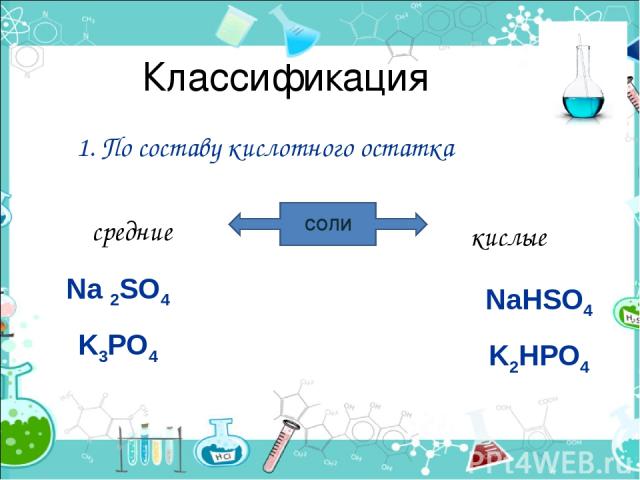
Классификация 1. По составу кислотного остатка СОЛИ средние кислые Na 2SO4 K3PO4 NaHSO4 K2HPO4

Номенклатура средних солей магния Название кислотного остатка Наименование металла в родительном падеже МgСL2 хлорид

Номенклатура кислых солей Указать название кислотного остатка К названию кислотного остатка прибавить «гидро-» Наименование металла в родительном падеже NaHSO4 сульфат гидро натрия

Химические свойства 1. Взаимодействие с металлами: SnCl2 + Zn ZnCl2 + Sn

Химические свойства 2. Взаимодействие со щелочами: 2NaОН + CuSO4 → Cu(OH)2 + Na2SO4

Химические свойства 3. Взаимодействие солей между собой КСl + AgNO3 → AgCl + KNO3
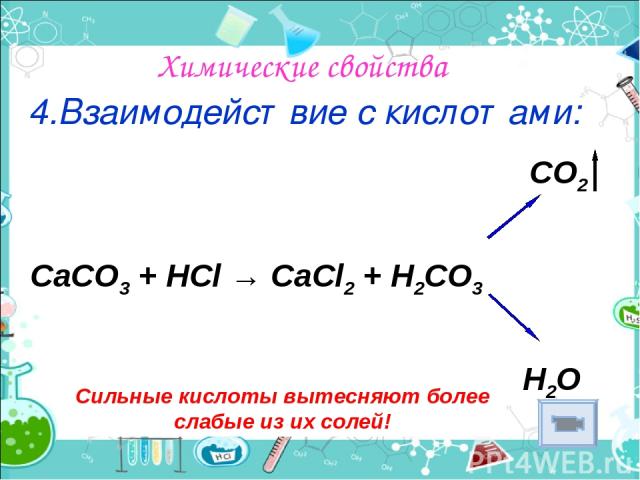
Химические свойства 4.Взаимодействие с кислотами: Сильные кислоты вытесняют более слабые из их солей! CO2 CaCO3 + HCl → CaCl2 + H2CO3 H2O

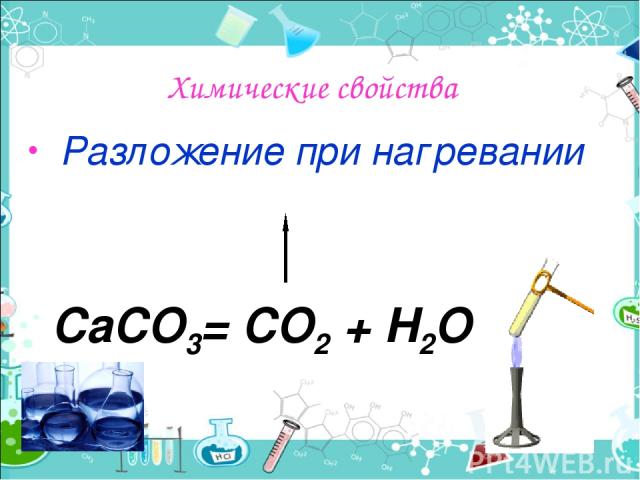
Химические свойства Разложение при нагревании СаСО3= СО2 + Н2О

Способы получения 1. Кислота + основание = соль + вода H2SO4 +2NaOH = Na2SO4 + 2H2O 2. Кислота + металл = соль + водород 2HCL +Zn = ZnCL2 + H2 3. Кислота + основный оксид = соль + вода 2HCL + CuO = CuCL2 + H2O 4. Кислота + соль = новая кислота + новая соль H2SO4 + BaCL2 = 2HCL + BaSO4 Условия: в результате реакции должны получиться газ, осадок или вода. Основаны на химических свойствах оксидов, оснований, кислот 10 способов 10 способов 10 способов 10 способов 10 способов

Способы получения 5. Основание + соль = новое основание + новая соль 2КОН + СаSO4 = Са(ОН) 2 + К2SO4 6. Основание + кислотный оксид + = соль + вода 2NaOH + SO3 = Na2SO4 + H2O 7. Кислотный оксид + основный оксид = соль СО2+ СаО = СаСО3 8. Соль + соль = новая соль + новая соль КСl + AgNO3 → AgCl + KNO3 9. Соль + металл = новая соль + металл CuSO4 + Fe = FeSO4 + Cu 10. Металл + неметалл = соль Fe +S = FeS 10 способов 10 способов 10 способов 10 способов