Презентация на тему: Химический элемент фосфор

ФОСФОР- ЭЛЕМЕНТ V ГРУППЫ Петрова Нина - руководитель группы Мусабекова Эльмира Кенжабаева Гульнара Смычков Никита 5klass.net

Цель: рассмотреть особенности фосфора как химического элемента и простого вещества.

Задачи: 1)Изучить теоретический материал о фосфоре ( строение атома, нахождение в природе, физические и химические свойства, получение и применение). 2)Результаты изучения теоретического материал представить в наглядном виде. 3)Сделать вывод о химической активности фосфора.

ФОСФОР Электронная формула: +15 Р 1s2 2s2 2P6 3S2 3P3

Относительная атомная масса 30,9738 Порядковый номер 15 Число протонов в ядре 15 Число нейтронов 16 Наиболее характерная степень окисления +3, +5, реже встречается -3, -2, +1, +4

Фосфор в природе Из-за большой химической активности фосфор в природе встречается только в соединениях. Фосфор входит в состав: минералов фосфоритов и апатитов, в виде соединения фосфата кальция Ca3 (PO4)2; крупнейшее месторождение апатитов находится на Кольском полуострове, в районе Хибинских гор. Залежи фосфоритов находятся в районе гор Каратау, в Московской, Калужской, Брянской областях и в других местах. белковых веществ, содержащихся в генеративных органах растений; нервной и костной тканей организмов животных и человека; мозговых клеток.

Аллотропные модификации фосфора
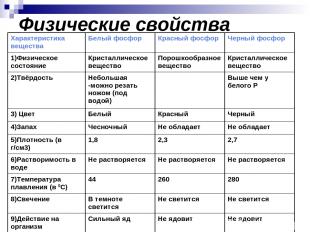
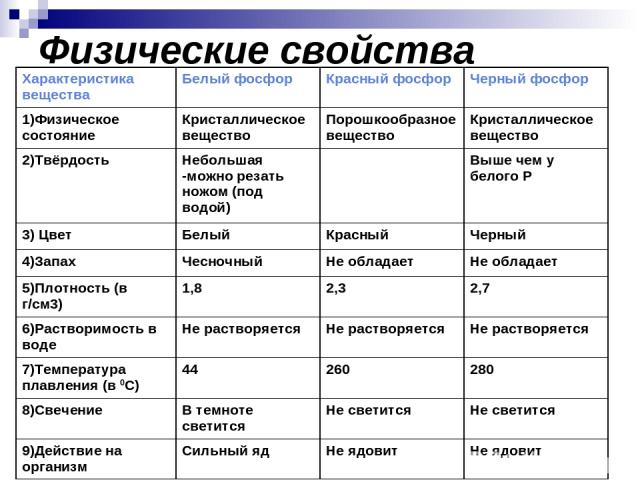
Физические свойства Характеристика вещества Белый фосфор Красный фосфор Черный фосфор 1)Физическое состояние Кристаллическое вещество Порошкообразное вещество Кристаллическое вещество 2)Твёрдость Небольшая -можно резать ножом (под водой) Выше чем у белого Р 3) Цвет Белый Красный Черный 4)Запах Чесночный Не обладает Не обладает 5)Плотность (в г/см3) 1,8 2,3 2,7 6)Растворимость в воде Не растворяется Не растворяется Не растворяется 7)Температура плавления (в 0С) 44 260 280 8)Свечение В темноте светится Не светится Не светится 9)Действие на организм Сильный яд Не ядовит Не ядовит

Химические свойства При длительном нагревании белого фосфора без доступа воздуха он желтеет и постепенно превращается в красный фосфор. При нагревании красного фосфора в тех же условиях он превращается в пар, при конденсации которого образуется белый фосфор. Фосфор проявляет окислительные и восстановительные свойства. Фосфор – восстановитель: 5О2 (изб.) + 4Р = 2Р2О5 3О2 (недост.) + 4Р = 2Р2О3 3Сl2 + 2P = 2PCl3 PСl3 + Cl2 = PCl5 3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO 4P + 16H2O = 4H3PO4 + 10H2 Фосфор – окислитель: 2Р + 3Mg = Mg3P2

Получение Фосфор получают из фосфоритов и апатитов, нагревая их в электрической печи без доступа воздуха в присутствии оксида кремния (IV) и угля Са3(РО4)2+5С+3SiO2 t 3CaSiO3+2P+5CO пары фосфора конденсируются под водой, и при этом образуется белый фосфор, в узлах кристаллической решётки которого находятся молекулы Р4.

Применение Красный фосфор применяют в производстве спичек. Его вместе с тонко измельченным стеклом и клеем наносят на боковую сторону коробка. При трении спичечной головки, в состав которой входят хлорат калия KClО3 и сера, происходит воспламенение: 6Р+5KClO3 5KCl+3P2O5 Белый фосфор в военное время использовали в зажигательных бомбах и для создания дымовых завес.

Важнейшие соединения Н3РО4 фосфорная кислота Р2О5 оксид фосфора (V)

Физические свойства P2O5 Белый, рыхлый порошок, гигроскопичный. Хранят в герметически закрытых сосудах.

Химические свойства P2O5 Проявляет свойства кислотного оксида. 1) реагирует с водой: P2O5 + H2O 2HPO3 P2O5 + 3H2O t 2H3PO4 2) реагирует с основными оксидами: P2O5 + 3К2O 2К3РО4 3) реагирует с основаниями: P2O5 + 6NaOH 2Na3РО4 + 3H2O

Получение P2O5 Образуется при горении фосфора в избытке воздуха: 4Р + 5О2 2Р2О5

Применение P2O5 Для осушки газов В качестве водоотнимающего вещества

Выводы: 1)Изучили теоретический материал о фосфоре. 2)Результаты изучения теоретического материала представили в виде презентации. 3)Фосфор активен с кислородом, галогенами и металлами. Проявляет окислительные и восстановительные свойства.

Информационные ресурсы 1) Глориозов П.А., Ходаков Ю.В., Эпштейн Д.А. Неорганическая химия: Учебник 9 класса. - М.: Просвещение, 1986. – 338с. 2) Рудзитис Г.Е., Фельдман Ф.Г. Химия. 9 класс: Учеб. для общеобразоват. учреждений. – М.: Просвещение,1990. – 175с. 3) Хомченко Г.П. Химия для поступающих в вузы: Учеб. Пособие.- 2-е изд., испр. – М.: Высшая школа, 1994. – 447с., ил.