Презентация на тему: Химия «Гидролиз солей»

Гидролиз солей 11 класс Всё познаётся в сравнении. 5klass.net

Цели урока: Ознакомиться с понятием гидролиза солей. Рассмотреть типы гидролиза. Научиться составлять ионные уравнения гидролиза солей. Научиться определять тип гидролиза соли по её формуле.

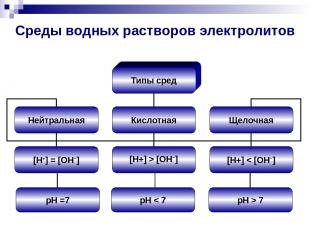
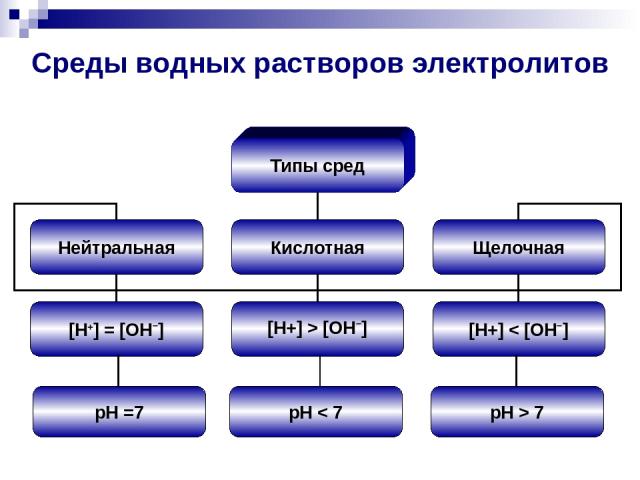
Среды водных растворов электролитов pH =7 pH < 7 pH > 7
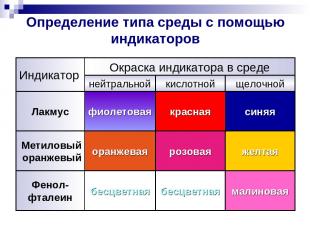
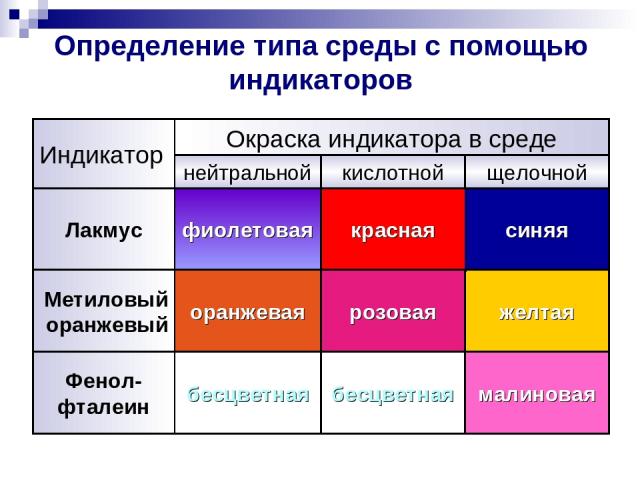
Определение типа среды с помощью индикаторов синяя красная фиолетовая Лакмус малиновая бесцветная бесцветная Фенол- фталеин желтая розовая оранжевая Метиловый оранжевый щелочной кислотной нейтральной Окраска индикатора в среде Индикатор
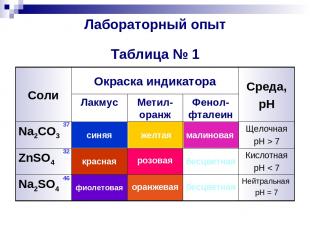
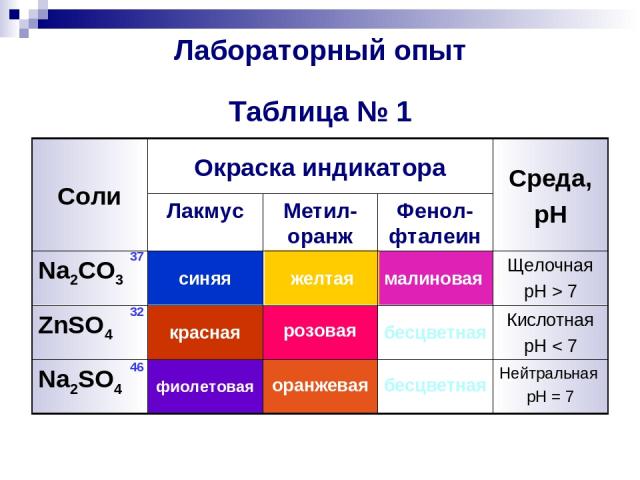
Лабораторный опыт Таблица № 1 Нейтральная pH = 7 бесцветная оранжевая фиолетовая Na2SO4 Кислотная pH < 7 бесцветная розовая красная ZnSO4 Щелочная pH > 7 малиновая желтая синяя Na2CO3 Фенол-фталеин Метил-оранж Лакмус Среда, pH Окраска индикатора Соли 37 32 46

Что такое гидролиз? Гидролиз (от греческого hydro – вода; lysis – разложение)
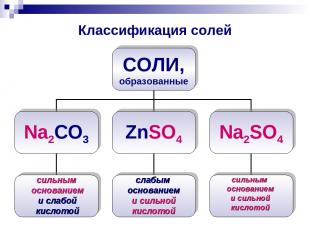
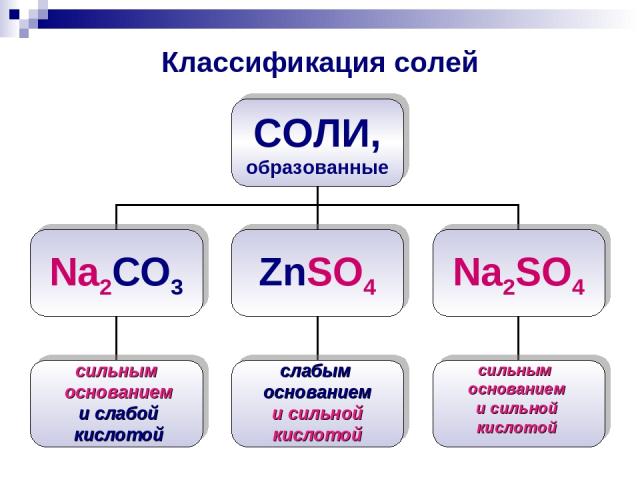
Классификация солей сильным основанием и слабой кислотой слабым основанием и сильной кислотой сильным основанием и сильной кислотой
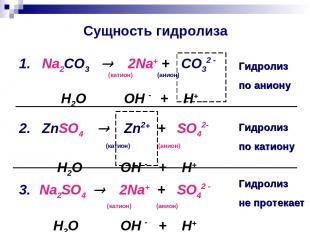
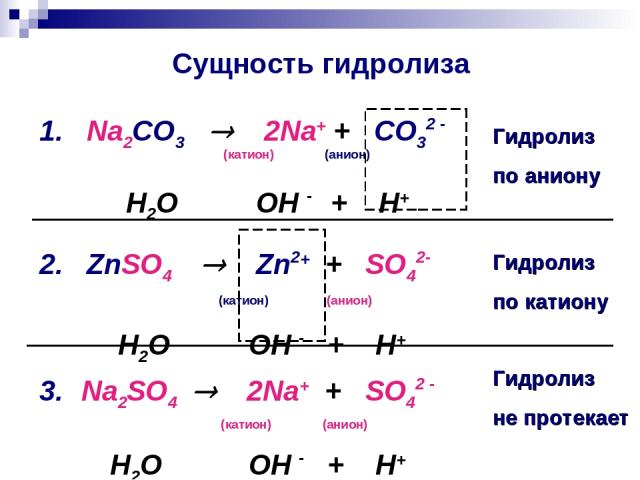
Сущность гидролиза 1. Na2CO3 2Na+ + CO32 - (катион) (анион) H2O ⇄ OH - + H+ 2. ZnSO4 Zn2+ + SO42- (катион) (анион) H2O ⇄ OH - + H+ 3. Na2SO4 2Na+ + SO42 - (катион) (анион) H2O ⇄ OH - + H+ Гидролиз по аниону Гидролиз по катиону Гидролиз не протекает

Определение гидролиза Гидролиз соли – это химическая реакция обмена соли с водой, в результате которой ионы слабого электролита, входящие в состав соли, соединяются с составными частями воды: H+ и OH- .
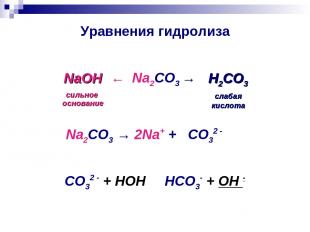
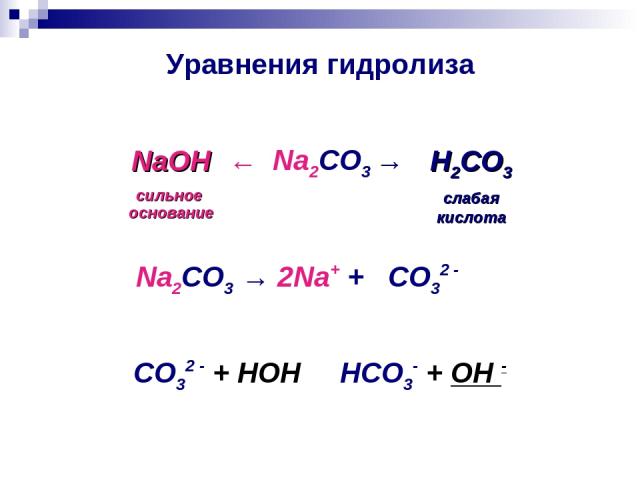
Уравнения гидролиза ← Na2CO3 → NaOH сильное основание H2CO3 слабая кислота Na2CO3 → 2Na+ + CO32 - CO32 - + HOH ⇄ HCO3- + OH -

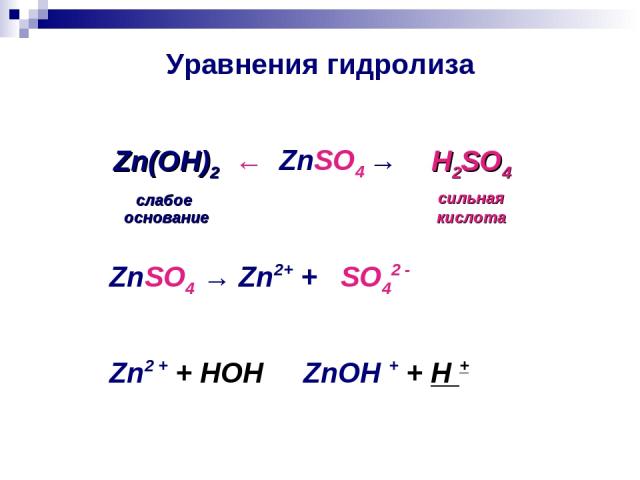
Уравнения гидролиза ← ZnSO4 → Zn(ОН)2 слабое основание H2SO4 сильная кислота ZnSO4 → Zn2+ + SO42 - Zn2 + + HOH ⇄ ZnOH + + H +
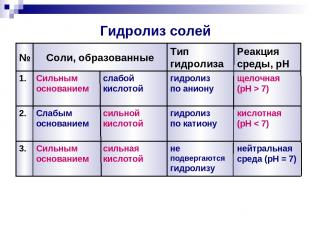
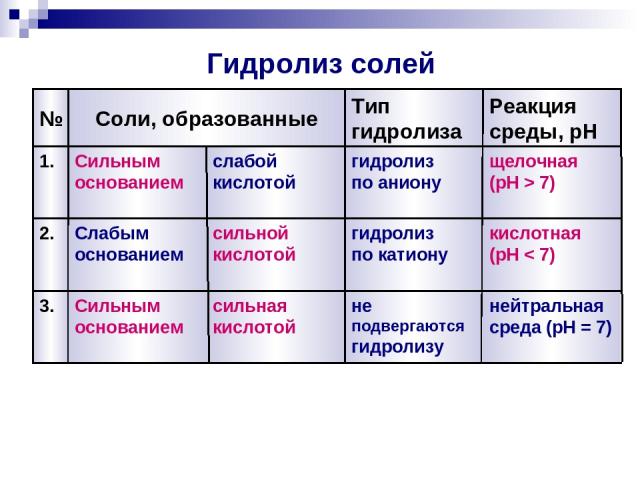
Гидролиз солей 3. 2. 1. № Реакция среды, pH Тип гидролиза Соли, образованные нейтральная среда (pH = 7) не подвергаются гидролизу сильная кислотой Сильным основанием кислотная (pH < 7) гидролиз по катиону сильной кислотой Слабым основанием щелочная (pH > 7) гидролиз по аниону слабой кислотой Сильным основанием

Задание. Определите реакцию среды водных растворов солей. Таблица № 2 NaNO3 K2S Na2SiO3 5. NH4NO3 LiNO3 NaClO4 4. KMnO4 KI K3PO 4 3. Na2SO3 FeCl3 CuSO4 2. KCl NaNO2 Li2SO4 1. III ряд II ряд I ряд № Н К Щ Н Щ Щ Н Н К Щ Н Щ Н К Н н-нейтральная; к – кислотная; щ - щелочная

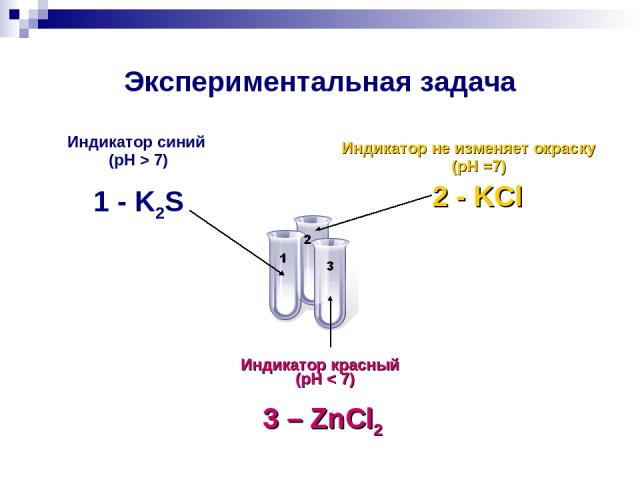
Экспериментальная задача В трех пронумерованных пробирках даны растворы солей: ZnCl2, K2S, KCl. а) Исследуйте каждый из них универсальной индикаторной бумагой; б) распознайте данные вещества; в) укажите тип гидролиза; г) напишите ионные уравнения гидролиза.
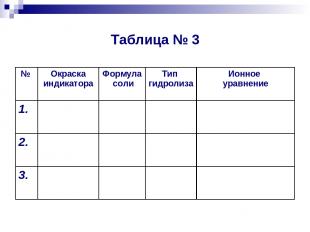
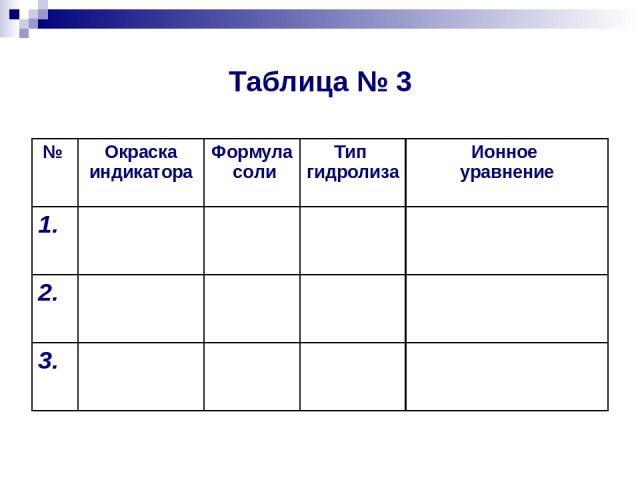
Таблица № 3 № Окраска индикатора Формула соли Тип гидролиза Ионное уравнение 1. 2. 3.
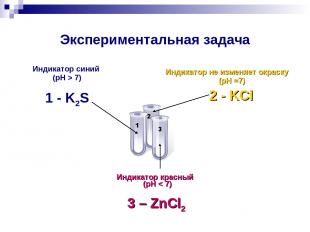
Экспериментальная задача Индикатор синий (pH > 7) 1 - K2S Индикатор не изменяет окраску (pH =7) 2 - KCl Индикатор красный (pH < 7) 3 – ZnCl2
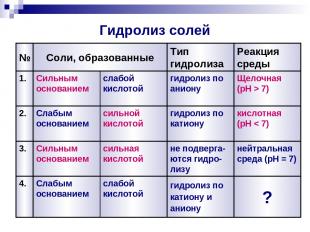
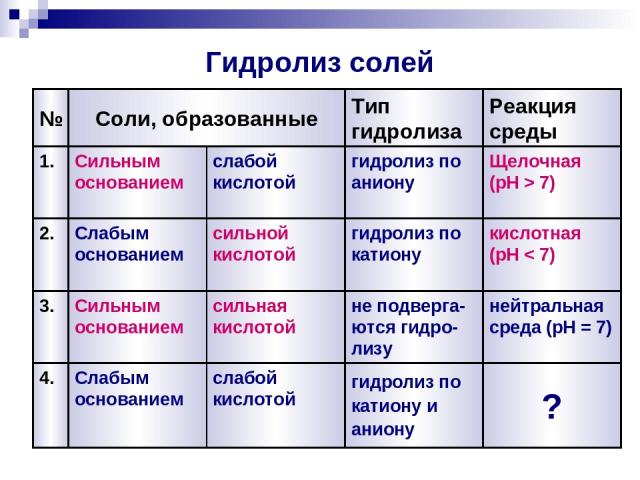
Гидролиз солей 4. 3. 2. 1. № Реакция среды Тип гидролиза Соли, образованные ? гидролиз по катиону и аниону слабой кислотой Слабым основанием нейтральная среда (pH = 7) не подверга-ются гидро-лизу сильная кислотой Сильным основанием кислотная (pH < 7) гидролиз по катиону сильной кислотой Слабым основанием Щелочная (pH > 7) гидролиз по аниону слабой кислотой Сильным основанием

Готовимся к ЕГЭ 1. Установите соответствие: Формула соли Тип гидролиза 1. FeCl2 А. по катиону 2. Ba(NO3)2 Б. по аниону 3. KF В. не гидролизуется 4. Na3PO4 Ответ: 1А; 2В; 3Б; 4Б

Готовимся к ЕГЭ 2. Установите соответствие: Формула соли Среда раствора 1. K2SO4 А. кислотная 2. Li2CO3 Б. щелочная 3. NH4Br В. нейтральная 4. CrCl3 Ответ: 1В; 2Б; 3А; 4А
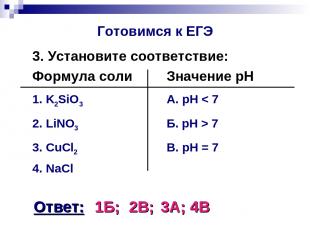
Готовимся к ЕГЭ 3. Установите соответствие: Формула соли Значение pH 1. K2SiO3 А. pH < 7 2. LiNO3 Б. pH > 7 3. CuCl2 В. pH = 7 4. NaCl Ответ: 1Б; 2В; 3А; 4В

Домашнее задание § 16 с. 163 – 168, упр. 3,4

Человек рождается на свет, Чтоб творить, дерзать – и не иначе, Чтоб оставить в жизни добрый след И решить все трудные задачи. Человек рождается на свет… Для чего? Ищите свой ответ!

Всё познаётся в сравнении.