Презентация на тему: Исследование наличия белков в составе пищевых продуктов

"Исследование наличия белков в составе пищевых продуктов"

Исследование белков Свое название белки получили от яичного белка, который с незапамятных времен использовался человеком как составная часть пищи. По описаниям Плиния Старшего, уже в Др. Риме яичный белок применялся и как лечебное средство. Впервые термин белковый(albumineise) применительно ко всем жидкостям животного организма использовал французкий физиолог Ф. Кене в 1747 г.

Первая концепция строения белков принадлежит голландскому химику Г. Мульдеру (1836). Основываясь на теории радикалов, он сформулировал понятие о минимальной структурной единице, входящей в состав всех белков. Эту единицу, которой приписовался состав 2C8H12N2+5O, Мульдер назвал протеином(Pr), а свою концепцию-теорией протеина. Вскоре наступают трудные времена для теории протеина. Понимая весомость аргументов оппонентов, Г. Мульдер пытался корректировать формулу протеина (C36H50O10), но в конце концов уступил под натиском новых фактов и открытий. И сейчас состав протеина уточнен:C40H62N10O12

В 1888 г. А. Я. Данилевский предположил существование в белках -N-S- химических группировок. В 1902 г. Э. Фишер предложил пептидную теорию строения белка. В 1934 г. Лайнус Полинг совместно с А. Е Мирски сформулировал теорию строения и функции белка.В 1951 г. Л. Полинг разработал модель вторичной структуры белка.

Классификация белков АльбуминыГлобулиныГистоныПротаминыПроламиныСклеропротеины(кератин, коллагены, эластин, фиброин) Фосфопротеины (казеин молока)НуклеопротеидыХромопротеидыГликопротеиды

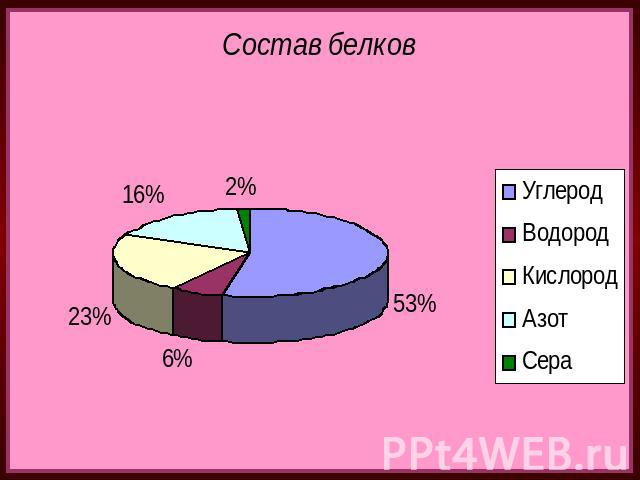
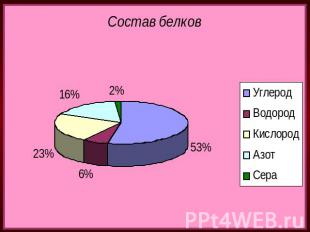
Состав и строение Составной частью белков являются аминокислоты.Аминокислоты -органические бифункциональные соединения, в состав которых входят карбоксильная группа –СООН и аминогруппа –NН2. В состав белков входят только 20 аминокислот, называемых иногда природными. Аминокислоты связаны между собой пептидной связью.Пептидная связь -это связь между двумя -аминокислотными остатками, а полимеры, построенные из остатков -аминокислот, соединенных пептидными связями, называют полипептидами
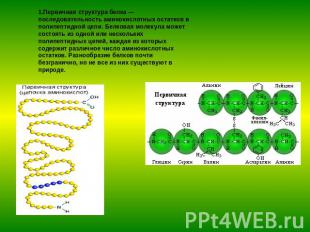
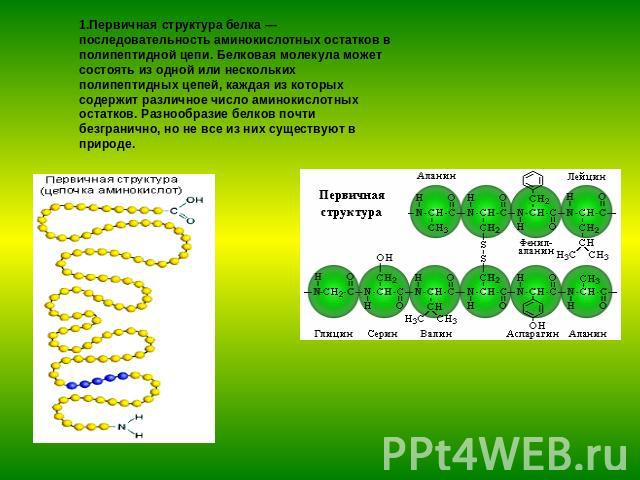
1.Первичная структура белка — последовательность аминокислотных остатков в полипептидной цепи. Белковая молекула может состоять из одной или нескольких полипептидных цепей, каждая из которых содержит различное число аминокислотных остатков. Разнообразие белков почти безгранично, но не все из них существуют в природе.

2.Вторичная структура белка — способ скручивания полипептидной цепи в пространстве (за счет водородной связи между водородом амидной группы — NH — и карбонильной группы — СО —, которые разделены четырьмя аминокислотными фрагментами). Вторичной структурой обладает большая часть белков, правда, не всегда на всем протяжении полипептидной цепи. В одном витке спирали обычно содержится 3,6 аминокислотных остатка, шаг спирали – 0,544 нм.

3.Третичная структура белка — реальная трехмерная конфигурация закрученной спирали полипептидной цепи в пространстве (спираль, скрученная в спираль). Третичная структура белка обуславливает специфическую биологическую активность белковой молекулы. В формировании третичной структуры, кроме водородных связей, большую роль играет ионное и гидрофобное взаимодействие. По характеру «упаковки» белковой молекулы различают белки глобулярные, или шаровидные, и фибрилллярные, или нитевидные, белки.
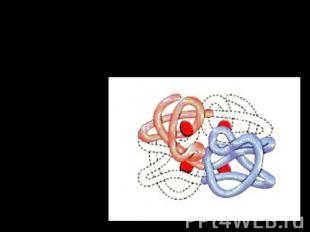
4.Четвертичная структура белка — относится к макромолекулам, в состав которых входит несколько полипептидных цепей (субъединиц), не связанных между собой ковалентно. Между собой эти субъединицы соединяются водородными, иоными, гидрофобными и другими связями. Примером может служить макромолекула гемоглобина.

ФИЗИЧЕСКИЕ СВОЙСТВА. Белки – амфотерные электролиты. При определенном значении pH среды число положительных и отрицательных зарядов в молекуле белка одинаково. Белки имеют разнообразное строение. Есть белки нерастворимые в воде и легко растворимые в воде. Есть белки малоактивные в химическом отношении, устойчивые к действию реагентов и крайне неустойчивые. Есть белки, имеющие вид нитей, достигающих в длину сотен нанометров; есть белки, имеющие форму шариков диаметром всего 5–7 нм. Они имеют большую молекулярную массу (104—107).

Гидролиз белков Реакция гидролиза идет с образованием аминокислот (т. е. разрушение первичной структуры в кислом или щелочном растворе). В общем виде ее можно записать так:

Химический синтез Химический синтез белков имеет большое практическое и теоретическое значение. В практическом отношении важны белковые гормоны — инсулин и вазопрессин, в настоящее время получаемые синтетическим путем. В частности, возможно получение гомополимеров или статистических сополимеров, состоящих из аминокислотных остатков, связанных пептидными связями (полиаминокислот). В качестве примера можно привести процесс получения полиаминокислот, основанный на конденсации карбоксиангидридов аминокислот, образуемых из соответствующих аминокислот:

Список использованной литературы: «ХИМИЯ—справочник для абитуриентов и студентов». Издательство acT-Фолио, Москва, 2000 год.Большая медицинская энциклопедия.«Энциклопедия для детей. Химия». Аванта+, Москва, 2000 год.Албертс Б., Брей Д., и др. Молекулярная биология клетки Москва, 1994.Биотехнология. Производство белковых веществ. В.А. Быков, М.Н. Манаков . Москва «Высшая школа» 1987г.Березин Б.Д., Березин Д.Б. Курс современной органической химии. Учебное пособие для вузов. —М.: Высшая школа, 1999. Кнорре Д.Г., Мызина С.Д. Биологическая химия. —М.: Высшая школа, 1998.Шамин А.Н. История химии белка. —Москва : «Наука», 1977. Якубке Х.-Д., Ешкайт Х. Аминокислоты, пептиды, белки. Москва: «Мир», 1985.Услуги Интернета - сайты: http://www.bestreferat.ru/referat-category-104.html, http://referat.na5.ru/load.php?id=501821