Презентация на тему: Физико-химические свойства алкинов
Физико-химические свойства алкинов

С2 – С4 газыС5 – С 15 жидкостиСвыше С16 – твердые веществаtпл и t кип алкинов увеличиваются с ростом молекулярной массы. Алкины плохо растворимы в воде, хорошо в органических растворителях.

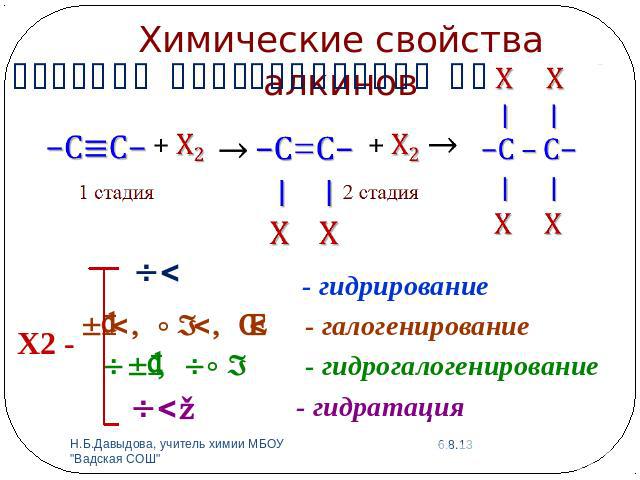
Химические свойства алкинов1. Реакции присоединения АЕгидрированиегалогенирование

1. Реакции присоединения АЕа) Гидрирование(+Н2) в 2 стадии:

1. Реакции присоединения АЕб) Галогенирование (+Г2) в 2 стадии:Качественная реакция на алкины – бромная вода Br2 (бурая жидкость) обесцвечивается.
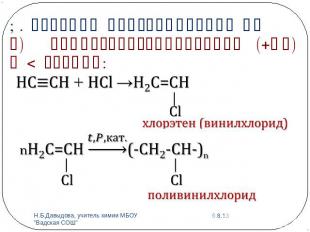
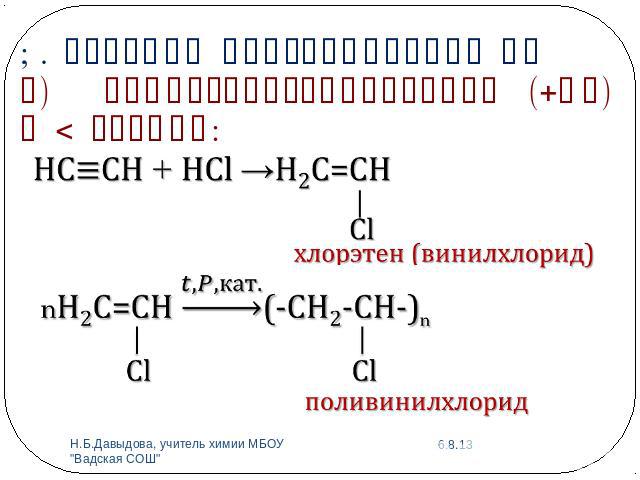
1. Реакции присоединения АЕв) Гидрогалогенирование (+НГ) в 2 стадии:

Изоляция для проводов, изоляционная лента, искусственная кожа, плащи, кленка.
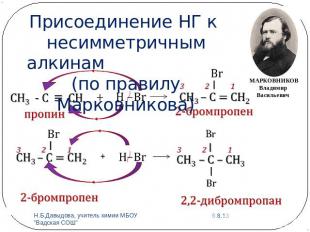
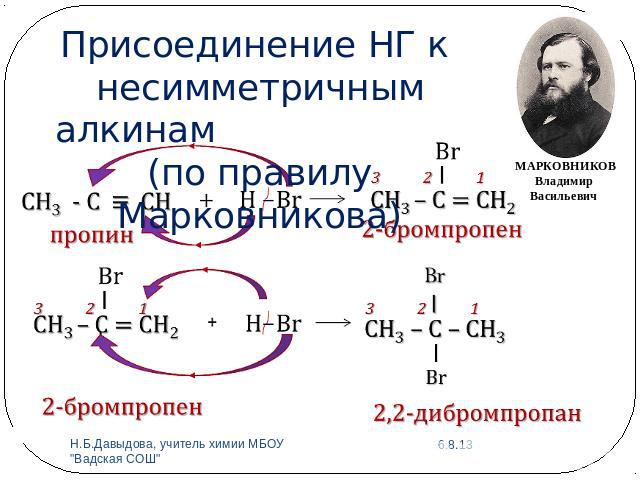
Присоединение НГ к несимметричным алкинам (по правилу Марковникова)

МАРКОВНИКОВ Владимир Васильевич (13 декабря 1837—29 января 1904) — русский химик, основатель научной школы. Развивая теорию химического строения А. М. Бутлерова, исследовал взаимное влияние атомов в органических соединениях и установил ряд закономерностей (в том числе правило присоединения гидрогалогенидов к непредельным углеводородам с двойной и тройной связью, впоследствии названное его именем в 1869 году).Открыл изомерию жирных кислот (1865). С начала 80-х гг. исследовал кавказские нефти, открыл нафтены. Содействовал развитию отечественной химической промышленности. Один из организаторов Русского химического общества (1868).

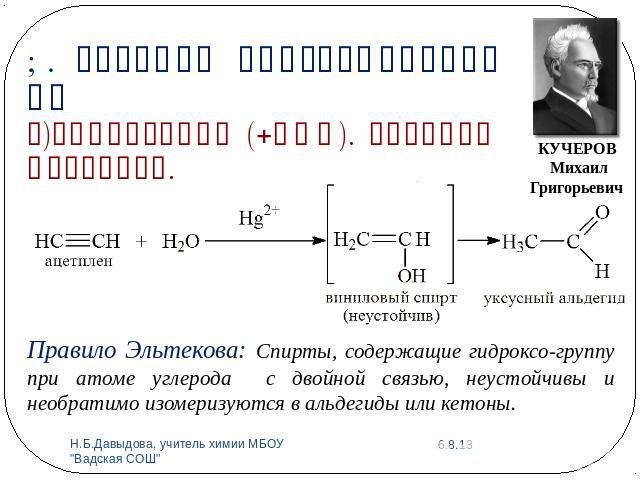
1. Реакции присоединения АЕг)Гидратация (+НОН). Реакция Кучерова.Правило Эльтекова: Спирты, содержащие гидроксо-группу при атоме углерода с двойной связью, неустойчивы и необратимо изомеризуются в альдегиды или кетоны.

КУЧЕРОВ Михаил Григорьевич (3 июня1850 – 26 июня 1911). Русский химик-органик. Основные работы посвящены развитию органического синтеза. Исследовал (1875) условия превращения бромвинила в ацетилен. Открыл (1881) реакцию каталитической гидратации ацетиленовых углеводородов, превращения ацетилена в уксусный альдегид в присутствии солей ртути (реакция Кучерова). Исследовал механизм этой реакции. Данный метод положен в основу промышленного получения уксусного альдегида и уксусной кислоты.Русское физико-химическое общество учредило (1915) премию имени М.Г. Кучерова для начинающих исследователей-химиков.
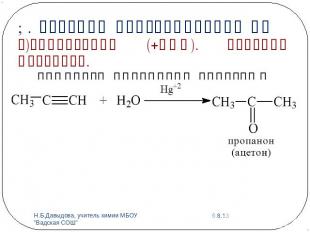
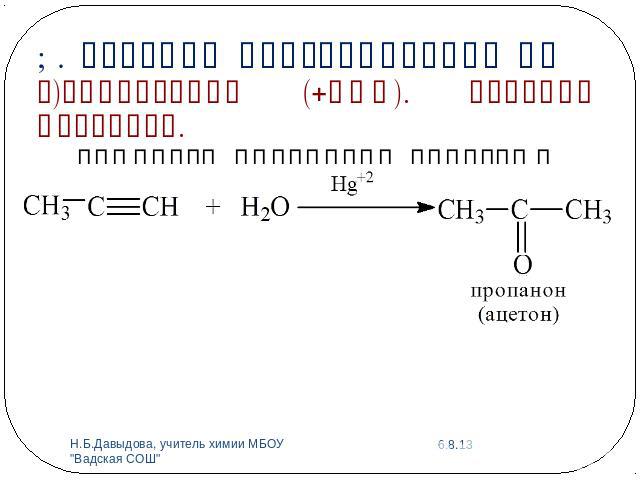
1. Реакции присоединения АЕг)Гидратация (+НОН). Реакция Кучерова.Гомологи ацетилена образуют кетоны:

Ацетилен образует с воздухом и кислородом взрывоопасные смеси.

2. Реакции окисления.а) Окисление раствором водным раствором перманганата калия (качественная реакция).В нейтральной и слабощелочной средах на холоде образуются соли карбоновых кислот; ацетилен окисляется до оксалатов (солей щавелевой кислоты): 3CH ≡ CH + 8KMnO4 → 3KOOC – COOK + 8MnO2 + 2KOH + 2H2O
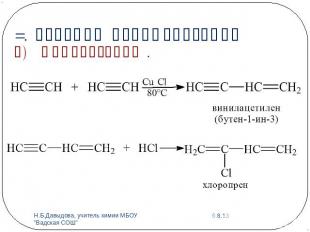
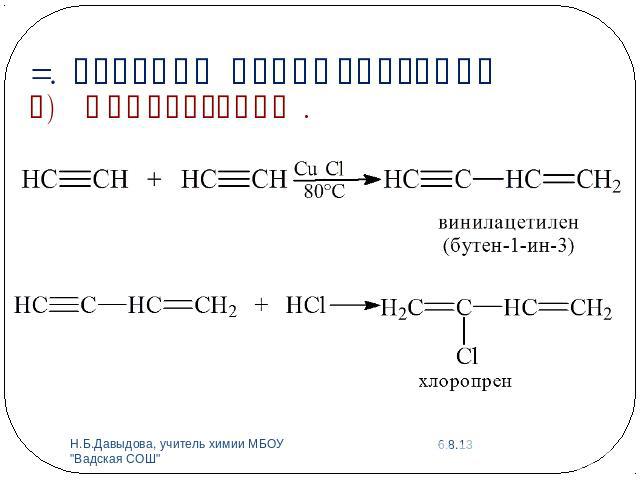
3. Реакции полимеризации а) Димеризация .
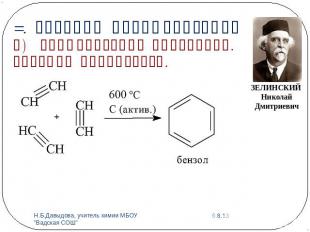
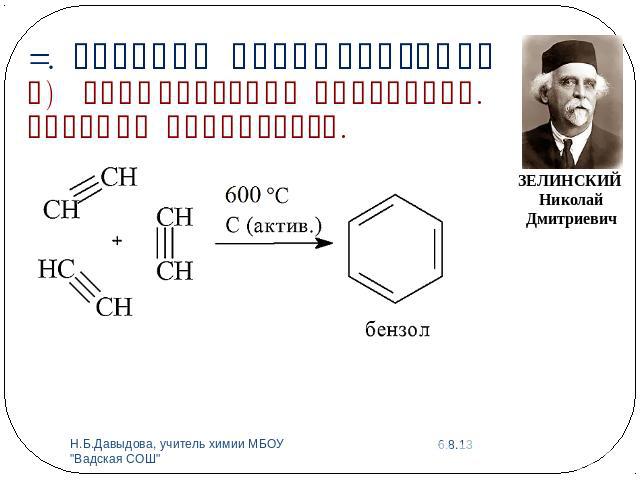
3. Реакции полимеризации б) Тримеризация ацетилена. Реакция Зелинского.

Химия часто одаряла меня величайшими наслаждениями познания еще не разведанных тайн природы. Она дала мне возможность послужить людям... Я уверен, что ни один из тех, кто заинтересуется химией, не пожалеет о том, что выберет эту науку в качестве своей специальности.Н.Д. ЗелинскийНиколай Дмитриевич Зелинский (25 января 1861 — 31 июля 1953) — замечательный русский химик, основоположник учения о гетерогенном органическом катализе, создатель первого в мире универсального угольного противогаза, учитель нескольких поколений химиков.

4. Реакции замещения (кислотные свойства)Опыт. Получение ацетиленида серебраHC≡CH + 2CuCl → CuC≡CCu↓+ 2HCl ацетиленид меди (I), коричневыйОпыт. Получение ацетиленида медиКачественная реакция на алкины с концевым положением тройной связи.

Типы химических реакций, характерные для алкиновУравнения реакций, характеризующие химические свойства ацетиленаХимические свойства алкинов

Базовый уровень сложности1. При гидратации ацетилена образуется 1) этанол2) этаналь3) этиленгликоль4) этен2. Реакция тримеризации ацетилена используется для получения 1) винилацетилена 3) циклогексана2) бензола 4) полипропилена 3. В результате реакции Кучерова образуется 1) этанол 2) этан 3) этаналь 4) этандиол-1,24. Этин можно отличить от этана с помощью1) лакмуса 3) гидроксида меди(II) 2) водного раствора щелочи 4) бромной воды

Базовый уровень сложности5. Пропин можно отличить от пропена с помощью1) водного раствора перманганата калия 2) раствора хлорида железа(III)3) бромной воды4) аммиачного раствора оксида серебра6. Бутин-2 можно отличить от бутина-1 с помощью1) бромной воды2) аммиачного раствора хлорида меди(I)3) водного раствора хлорида меди(II)4) водного раствора перманганата калияПовышенный уровень сложности7. По правилу Марковникова происходит взаимодействие между1) бутином-2 и хлороводородом 4) бутаном и хлором2) бутином-1 и водородом 5) пропеном и бромоводородом3) бутином-1 и водой 6) пропином и водой

Повышенный уровень сложности8. Бутин-1 способен реагировать с 1) натрием 4)кислородом2) гидроксидом натрия 5)хлоридом меди(II)3) водой 6)серебромВысокий уровень сложности9. (С5) Алкин массой 8 г может максимально присоединить 8,96 л (н.у.) водорода. Установите молекулярную формулу алкина. 10. (С5) Одинаковое количество алкина в результате присоединения хлора и брома образует соответственно 5,46 г тетрахлорпроизводного и 10,8 г тетрабромпроизводного. Установите молекулярную формулу алкина.

Домашнее задание:

Список литературы1. Учебник: Кузнецова Н.Е., Гара Н.Н. Титова И.М.; под ред. Н. Е. Кузнецовой. Химия: профильный уровень, - М.: Вентана - Граф, 20112. Интерактивный мультимедиа учебник Органическая химия - учебник для 10-11 кл.1998—2013 Г.И. Дерябина, Г.В. Кантари [Электронный ресурс]. http://www.chemistry.ssu.samara.ru/chem2/index2.htm3. Единая коллекция цифровых образовательных ресурсов. - «Химия», 10 класс, Габриелян О.С., Маскаев Ф.Н., Пономарев С.Ю., Теренин В.И. http://school-collection.edu.ru/catalog/rubr/d05469af-69bd-11db-bd13-0800200c9c10/75844/?interface=pupil&class=53&subject=31- Органическая химия. Видеоопыты. http://school-collection.edu.ru/catalog/rubr/528b6fb1-98e4-9a27-5ae1-2f785b646a41/?interface=pupil&class[]=53&subject[]=314. Химия. 10 класс. Тематические тестовые задания для подготовки к ЕГЭ. / Авт.-сост. Л.И. Асанова, Т.Н. Богданович, О.Н. Вережникова. – Ярославль: Академия развития, 2011. – (Единый государственный экзамен).