Презентация на тему: Процесс электролиза

Применение электролиза

Содержание Сущность электролиза Практическое применение электролиза

Сущность электролиза Электролиз — это окислительно-восстановительный процесс, протекающий на электродах при прохождении постоянного электрического тока через раствор или расплав электролитов. Для осуществления электролиза к отрицательному полюсу внешнего источника постоянного тока присоединяют катод, а к положительному полюсу — анод, после чего погружают их в электролизер с раствором или расплавом электролита. Электроды, как правило, бывают металлические, но применяются и неметаллические, например графитовые (проводящие ток).

В результате электролиза на электродах (катоде и аноде) выделяются соответствующие продукты восстановления и окисления, которые в зависимости от условий могут вступать в реакции с растворителем, материалом электрода и т. п., — так называемые вторичные процессы. Металлические аноды могут быть: а) нерастворимыми или инертными (Pt, Au, Ir, графит или уголь и др.), при электролизе они служат лишь передатчиками электронов; б) растворимыми (активными); при электролизе они окисляются.

В растворах и расплавах различных электролитов имеются разноименные по знаку ионы, т. е. катионы и анионы, которые находятся в хаотическом движении. Но если в такой расплав электролита, например расплав хлорида натрия NaCl, опустить электроды и пропускать постоянный электрический ток, то катионы Na+ будут двигаться к катоду, а анионы Cl– — к аноду. На катоде электролизера происходит процесс восстановления катионов Na+ электронами внешнего источника тока: Na+ + e– = Na0

На аноде идет процесс окисления анионов хлора, причем отрыв избыточных электронов от Cl– осуществляется за счет энергии внешнего источника тока: Cl– – e– = Cl0 Выделяющиеся электронейтральные атомы хлора соединяются между собой, образуя молекулярный хлор: Cl + Cl = Cl2, который и выделяется на аноде. Суммарное уравнение электролиза расплава хлорида натрия: 2NaCl —> 2Na+ + 2Cl– —электролиз—> 2Na0 + Cl20

Окислительно-восстановительное действие электрического тока может быть во много раз сильнее действия химических окислителей и восстановителей. Меняя напряжение на электродах, можно создать почти любой силы окислители и восстановители, которыми являются электроды электролитической ванны или электролизера.

Известно, что ни один самый сильный химический окислитель не может отнять у фторид-Иона F– его электрон. Но это осуществимо при электролизе, например, расплава соли NaF. В этом случае на катоде (восстановитель) выделяется из ионного состояния металлический натрий или кальций: Na+ + e– = Na0 на аноде (окислитель) выделяется ион фтора F–, переходя из отрицательного иона в свободное состояние: F– – e– = F0 ; F0 + F0 = F2

Продукты, выделяющиеся на электродах, могут вступать между собой в химическое взаимодействие, поэтому анодное и катодное пространство разделяют диафрагмой.

Практическое применение электролиза Электрохимические процессы широко применяются в различных областях современной техники, в аналитической химии, биохимии и т. д. В химической промышленности электролизом получают хлор и фтор, щелочи, хлораты и перхлораты, надсерную кислоту и персульфаты, химически чистые водород и кислород и т. д. При этом одни вещества получают путем восстановления на катоде (альдегиды, парааминофенол и др.), другие электроокислением на аноде (хлораты, перхлораты, перманганат калия и др.).

Электролиз в гидрометаллургии является одной из стадий переработки металлсодержащего сырья, обеспечивающей получение товарных металлов. Электролиз может осуществляться с растворимыми анодами - процесс электрорафинирования или с нерастворимыми - процесс электроэкстракции. Главной задачей при электрорафинировании металлов является обеспечения необходимой чистоты катодного металла при приемлемых энергетических расходах.

В цветной металлургии электролиз используется для извлечения металлов из руд и их очистки. Электролизом расплавленных сред получают алюминий, магний, титан, цирконий, уран, бериллий и др. Для рафинирования (очистки) металла электролизом из него отливают пластины и помещают их в качестве анодов в электролизер. При пропускании тока металл, подлежащий очистке, подвергается анодному растворению, т. е. переходит в раствор в виде катионов. Затем эти катионы металла разряжаются на катоде, благодаря чему образуется компактный осадок уже чистого металла. Примеси, находящиеся в аноде, либо остаются нерастворимыми, либо переходят в электролит и удаляются.

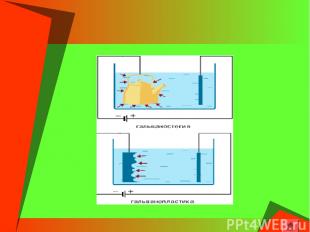
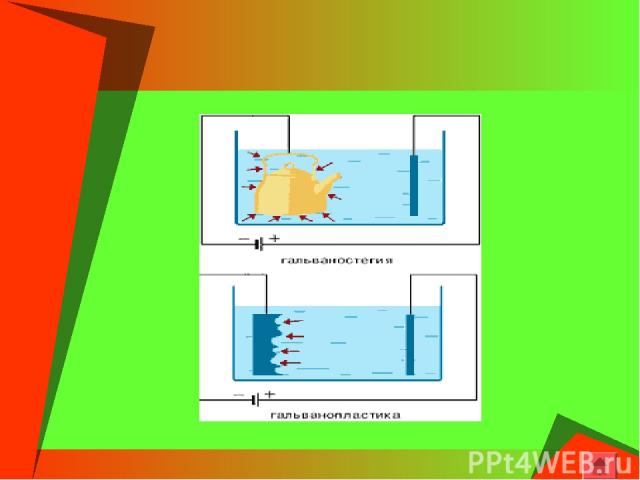
Гальванотехника – область прикладной электрохимии, занимающаяся процессами нанесения металлических покрытий на поверхность как металлических, так и неметаллических изделий при прохождении постоянного электрического тока через растворы их солей. Гальванотехника подразделяется на гальваностегию и гальванопластику.

Гальваностегия (от греч. покрывать) – это электроосаждение на поверхность металла другого металла, который прочно связывается (сцепляется) с покрываемым металлом (предметом), служащим катодом электролизера. Перед покрытием изделия необходимо его поверхность тщательно очистить (обезжирить и протравить), в противном случае металл будет осаждаться неравномерно, а кроме того, сцепление (связь) металла покрытия с поверхностью изделия будет непрочной. Способом гальваностегии можно покрыть деталь тонким слоем золота или серебра, хрома или никеля. С помощью электролиза можно наносить тончайшие металлические покрытия на различных металлических поверхностях. При таком способе нанесения покрытий, деталь используют в качестве катода, помещенного в раствор соли того металла, покрытие из которого необходимо получить. В качестве анода используется пластинка из того же металла.

Гальванопластика – получение путем электролиза точных, легко отделяемых металлических копий относительно значительной толщины с различных как неметаллических, так и металлических предметов, называемых матрицами. С помощью гальванопластики изготовляют бюсты, статуи и т. д. Гальванопластика используется для нанесения сравнительно толстых металлических покрытий на другие металлы (например, образование "накладного" слоя никеля, серебра, золота и т. д.).