Презентация на тему: Щелочные металлы


Отгадайте фамилию русского ученого, который сказал: «Металлом называется светлое тело, которое ковать можно». Металлы - чемпионыСамый тугоплавкий.Самый распространенный на земле.Самый легкий.Самый электропроводный.Самый твердый .Самый пластичный.Самый легкоплавкий.Самый тяжелый. Самый космический.

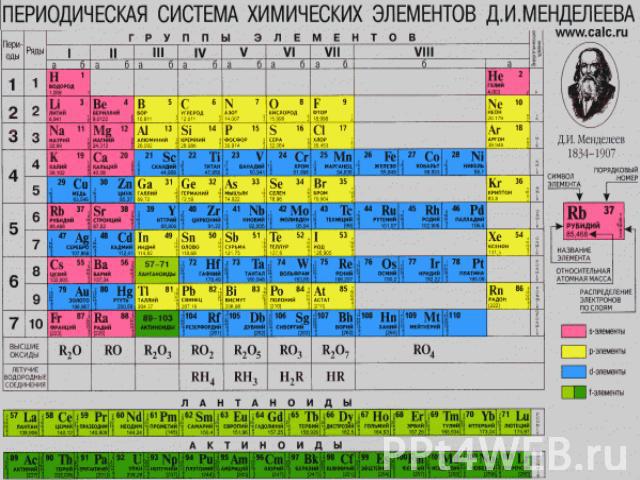
Цели урока Дать характеристику элементам IA группы по их положению в периодической системе химических элементов. На основе строения их атомов рассмотреть физические и химические свойства щелочных металлов.Указать области применения щелочных металлов

Щелочные металлы
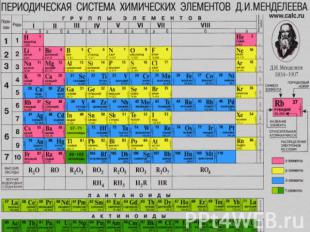
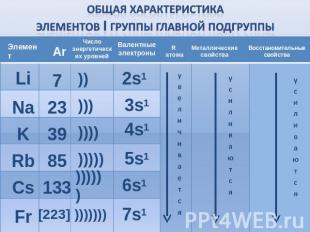
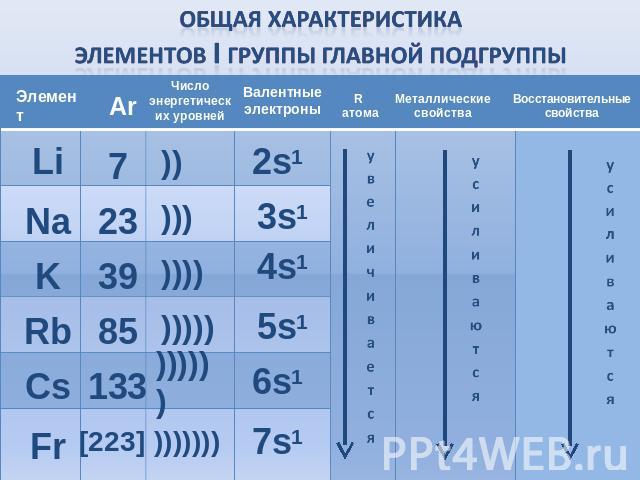
Общая характеристика элементов I группы главной подгруппы
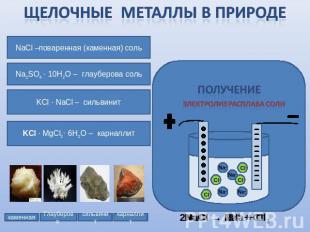
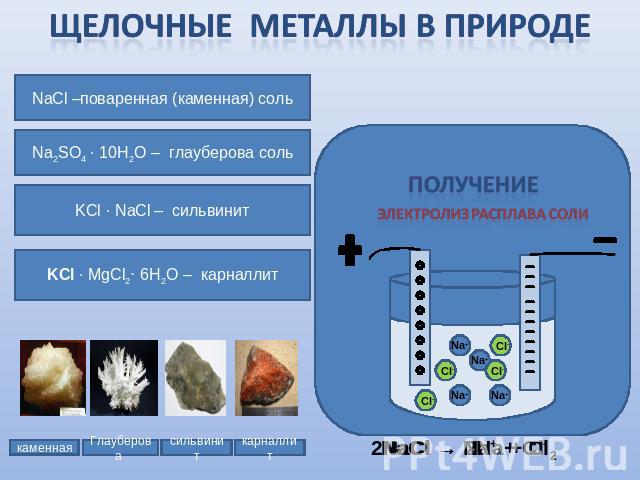
Щелочные Металлы в природе NaCl –поваренная (каменная) сольNa2SO4 ∙ 10H2O – глауберова сольKCl ∙ NaCl – сильвинитKCl ∙ MgCl2· 6H2O – карналлит

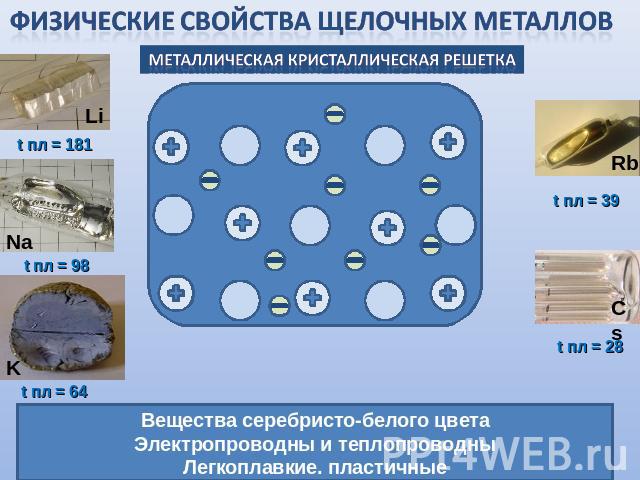
Физические свойства щелочных металловВещества серебристо-белого цветаЭлектропроводны и теплопроводныЛегкоплавкие. пластичные

химические свойства щелочных металловРЯД АКТИВНОСТИ МЕТАЛЛОВ / ЭЛЕКТРОХИМИЧЕСКИЙ РЯД НАПРЯЖЕНИЙПочему щелочные металлы не используют для реакции с растворами кислот и солей?Катионы щелочных металлов окрашивают пламя спиртовки

Биологическая роль и применение Соединений калия и натрияРаствор хлорида натрия (0,9%) применяется в медицине. Такой раствор называется физиологическимПитьевая сода применяется в кулинарии, для выпечки кондитерских изделий.Хлорид натрия - как добавка к пищеКалийные удобрения играю важную роль в жизни растений.

Проверь себя: ☺ Вычеркните неверное суждение о щелочных металлах:1. Число электронов на внешнем энергетическом уровне щелочных металлов равно 1.2. В реакциях щелочные металлы являются окислителями и восстановителями.3. При взаимодействии натрия с кислородом образуется пероксид натрия4. Щелочные металлы – это металлы IA группы Периодической системы химических элементов.5. Щелочные металлы получают электролизом расплавов их солей.6. Щелочные металлы не взаимодействуют с водой.7. Качественной реакцией на ионы щелочных металлов является их взаимодействие с кислородом.8. При переходе от лития к калию уменьшается радиус атома

Домашнее задание § 112. Выполнить цепочку химических превращений: Na →Na2O2→Na2O→Na2CO3 NaOH → NaCl

Спасибо за урок!!!

За основу презентации были взяты материалы Гальцевой О.Н.