Презентация на тему: Щелочные металлы 9 класс

ЩЕЛОЧНЫЕ МЕТАЛЛЫ

ЩЕЛОЧНЫЕ МЕТАЛЛЫ Щелочные металлы — элементы главной подгруппы I группы Периодической системы химических элементов Д. И. Менделеева: литий Li, натрий Na, калий K, рубидий Rb, цезий Cs и франций Fr. Эти металлы получили название щелочных, потому что большинство их соединений растворимо в воде. По-славянски «выщелачивать» означает «растворять», это и определило название данной группы металлов. При растворении щелочных металлов в воде образуются растворимые гидроксиды, называемые щёлочами.

Общая характеристика щелочных металлов В Периодической системе они следуют сразу за инертными газами, поэтому особенность строения атомов щелочных металлов заключается в том, что они содержат один электрон на внешнем энергетическом уровне: их электронная конфигурация ns1. Очевидно, что валентные электроны щелочных металлов могут быть легко удалены, потому что атому энергетически выгодно отдать электрон и приобрести конфигурацию инертного газа. Поэтому для всех щелочных металлов характерны восстановительные свойства. Это подтверждают низкие значения их потенциалов ионизации (потенциал ионизации атома цезия — один из самых низких) и электроотрицательности (ЭО).
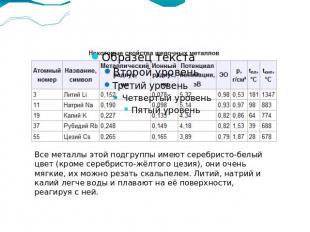
Все металлы этой подгруппы имеют серебристо-белый цвет (кроме серебристо-жёлтого цезия), они очень мягкие, их можно резать скальпелем. Литий, натрий и калий легче воды и плавают на её поверхности, реагируя с ней.

Химические свойства щелочных металлов Из-за высокой химической активности щелочных металлов по отношению к воде, кислороду, и иногда даже и азоту (Li, Cs) их хранят под слоем керосина. Чтобы провести реакцию со щелочным металлом, кусочек нужного размера аккуратно отрезают скальпелем под слоем керосина, в атмосфере аргона тщательно очищают поверхность металла от продуктов его взаимодействия с воздухом и только потом помещают образец в реакционный сосуд. 1. Взаимодействие с водой. Важное свойство щелочных металлов — их высокая активность по отношению к воде. Наиболее спокойно (без взрыва) реагирует с водой литий При проведении аналогичной реакции натрий горит жёлтым пламенем и происходит небольшой взрыв. Калий ещё более активен: в этом случае взрыв гораздо сильнее, а пламя окрашено в фиолетовый цвет.

2. Взаимодействие с кислородом. Продукты горения щелочных металлов на воздухе имеют разный состав в зависимости от активности металла. Только литий сгорает на воздухе с образованием оксида стехиометрического состава:При горении натрия в основном образуется пероксид Na2O2 с небольшой примесью надпероксида NaO2: В продуктах горения калия, рубидия и цезия содержатся в основном надпероксиды:

Для получения оксидов натрия и калия нагревают смеси гидроксида, пероксида или надпероксида с избытком металла в отсутствие кислорода: Для кислородных соединений щелочных металлов характерна следующая закономерность: по мере увеличения радиуса катиона щелочного металла возрастает устойчивость кислородных соединений, содержащих пероксид-ион О22−и надпероксид-ион O2−.Для тяжёлых щелочных металлов характерно образование довольно устойчивых озонидов состава ЭО3. Все кислородные соединения имеют различную окраску, интенсивность которой углубляется в ряду от Li до Cs:

Оксиды щелочных металлов обладают всеми свойствами, присущими основным оксидам: они реагируют с водой, кислотными оксидами и кислотами: Пероксиды и надпероксиды проявляют свойства сильных окислителей: Пероксиды и надпероксиды интенсивно взаимодействуют с водой, образуя гидроксиды:

3. Взаимодействие с другими веществами. Щелочные металлы реагируют со многими неметаллами. При нагревании они соединяются с водородом с образованием гидридов, с галогенами, серой, азотом, фосфором, углеродом и кремнием с образованием, соответственно, галогенидов, сульфидов, нитридов, фосфидов, карбидов и силицидов: При нагревании щелочные металлы способны реагировать с другими металлами, образуя интерметаллиды. Активно (со взрывом) реагируют щелочные металлы с кислотами.Щелочные металлы растворяются в жидком аммиаке и его производных — аминах и амидах: При растворении в жидком аммиаке щелочной металл теряет электрон, который сольватируется молекулами аммиака и придаёт раствору голубой цвет. Образующиеся амиды легко разлагаются водой с образованием щёлочи и аммиака:
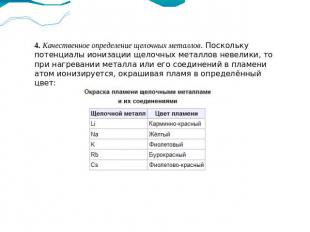
4. Качественное определение щелочных металлов. Поскольку потенциалы ионизации щелочных металлов невелики, то при нагревании металла или его соединений в пламени атом ионизируется, окрашивая пламя в определённый цвет:

Литий Самый легкий металл, имеет два стабильных изотопа с атомной массой 6 и 7; более распространен тяжелый изотоп, его содержание составляет 92,6% от всех атомов лития. Литий был открыт А.Арфведсоном в 1817 и выделен Р.Бунзеном и А.Матисеном в 1855. Он используется в производстве термоядерного оружия (водородная бомба), для увеличения твердости сплавов и в фармацевтике. Соли лития применяют для увеличения твердости и химической стойкости стекла, в технологии щелочных аккумуляторных батарей, для связывания кислорода при сварке.

Натрий Известен с древности, выделил его Х.Дэви в 1807. Это мягкий металл, широко применяются такие его соединения, как щелочь (гидроксид натрия NaOH), пищевая сода (бикарбонат натрия NaHCO3) и кальцинированная сода (карбонат натрия Na2CO3). Находит применение и металл в виде паров в неярких газоразрядных лампах уличного освещения.

Калий Известен с древности, выделил его также Х.Дэви в 1807. Соли калия хорошо известны: калиевая селитра (нитрат калия KNO3), поташ (карбонат калия K2CO3), едкое кали (гидроксид калия KOH) и др. Металлический калий также находит различное применение в технологии теплообменных сплавов.

Рубидий Рубидий был открыт методом спектроскопии Р.Бунзеном в 1861; содержит 27,85% радиоактивного рубидия Rb-87. Рубидий, как и другие металлы подгруппы IA, химически высокоактивен и должен храниться под слоем нефти или керосина во избежание окисления кислородом воздуха. Рубидий находит разнообразное применение, в том числе в технологии фотоэлементов, радиовакуумных приборов и в фармацевтике.

Цезий Соединения цезия широко распространены в природе, обычно в малых количествах совместно с соединениями других щелочных металлов. Минерал поллуцит силикат содержит 34% оксида цезия Cs2O. Элемент был открыт Р.Бунзеном методом спектроскопии в 1860. Основным применением цезия является производство фотоэлементов и электронных ламп, один из радиоактивных изотопов цезия Cs-137 применяется в лучевой терапии и научных исследованиях.

Выполнил Шляховой Владимир Франций Последний член семейства щелочных металлов франций настолько радиоактивен, что его нет в земной коре в более чем следовых количествах. Сведения о франции и его соединениях основаны на исследовании ничтожного его количества, искусственно полученного (на высокоэнергетическом ускорителе) при a-распаде актиния-227. Наиболее долгоживущий изотоп 22387Fr распадается за 21 мин на 22388Ra и b-частицы. Согласно приблизительной оценке, металлический радиус франция составляет 2,7 . Франций обладает большинством свойств, характерных для других щелочных металлов, и отличается высокой электронодонорной активностью. Он образует растворимые соли и гидроксид. Во всех соединениях франций проявляет степень окисления I.