Презентация на тему: Щелочные металлы

Муниципальное бюджетное общеобразовательное учреждение«Школа-интернат №1 среднего (полного) общего образования» городского округа город Стерлитамак Республики БашкортостанЩелочные металлы Выполнил учитель химии первой квалификационной категорииСафиканов Ахат Файзрахманович

Щелочные металлы

Периодическая система химических элементов Д.И.Менделеева
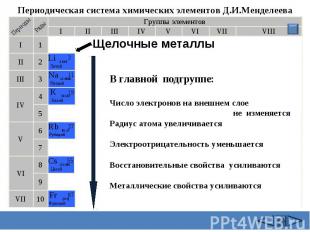
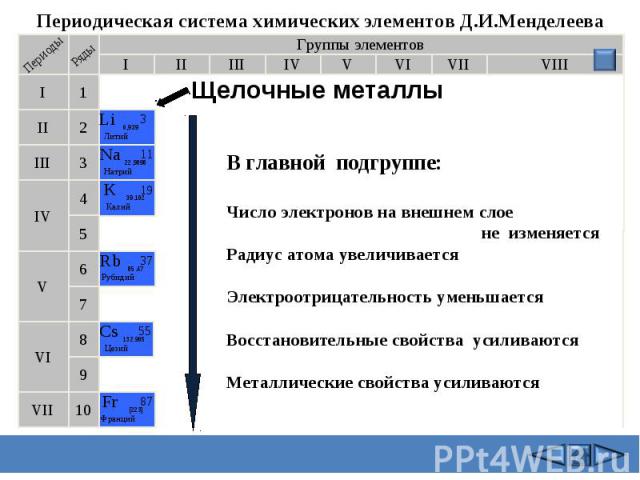
Периодическая система химических элементов Д.И.Менделеева Щелочные металлы В главной подгруппе:Число электронов на внешнем слое не изменяетсяРадиус атома увеличиваетсяЭлектроотрицательность уменьшаетсяВосстановительные свойства усиливаютсяМеталлические свойства усиливаются

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева

Периодическая система химических элементов Д.И.Менделеева
Щелочные металлы Литий Фрайций Цезий Рубидий Калий История открытия

История открытия лития Арфведсон Юхан Август(12 .01.1792 г. – 28 .10.1841 г.) Литий был открыт в 1817 г. А. Арфведсоном в минерале петалите. Берцелиус предложил назвать ее литионом (Lithion), поскольку эта щелочь впервые была найдена в "царстве минералов" (камней); название это произведено от греч.- камень. Металлический Литий впервые получен в 1818 г. Г. Дэви путем злектролиза щелочи. В 1855 г. Бунзен и Маттессен разработали промышленный способ получения металлического лития злектролизом хлорида лития.

История открытия натрия Гемфри Дэви (17.12.1778 г – 29.05.1829 г) Натрий (Natrium, от англ. и франц. Sodium, нем. Natrium от древнеевр. neter — бурлящее вещество. В 1807 г. Г.Дэви путем электролиза слегка увлажненных твердых щелочей получил свободный металл - натрий, назвав его содий (Sodium). В следующем году Гильберт предложил именовать новый металл натронием (Natronium); Берцелиус сократил последнее название до "натрий" (Natrium).

История открытия калия Калий (англ. Potassium, франц. Potassium, нем. Kalium) открыл в 1807 г. Г.Дэви, производивший электролиз твердого, слегка увлажненного едкого кали. Дэви именовал новый металл потассием (Potassium), но это название не прижилось. Крестным отцом металла оказался Гильберт, известный издатель журнала "Annalen deг Physik", предложивший название "калий"; оно было принято в Германии и России. Гемфри Дэви (17.12.1778 г – 29.05.1829 г)

История открытия рубидия Роберт Вильгельм Бунзен(31.03.1811 - 16.08.1899) Густав Роберт Кирхгоф (12.03.1824 – 17.10.1887) При спектроскопическом анализе минерала лепидолит (фторсиликат лития и алюминия) и обнаружились две новые красные линии в красной части спектра. Эти линии Р. Бунзен и Г.Кирхгофф правильно отнесли к новому металлу, который назвали рубидием (лат. rubidus - красный) из-за цвета его спектральных линий. Получить рубидий в виде металла Бунзену удалось в 1863 году.

История открытия цезия Цезий (англ. Cesium, франц. Cesium, нем. Caesium) - первый элемент, открытый с помощью спектрального анализа. Р.Бунзен и Г.Кирхгофф обнаружили спектральные линии нового элемента: одну слабо-голубую и другую ярко-голубую в области фиолетовой части спектра. Р.Бунзен назвал вновь открытый металл цезием (Casium) от лат. caesius -- голубой, светло-серый; в древности этим словом обозначали голубизну ясного неба. Чистый металлический цезий получен электролитическим путем в 1882 г. Роберт Вильгельм Бунзен(31.03.1811 - 16.08.1899) Густав Роберт Кирхгоф (12.03.1824 – 17.10.1887)

История открытия франция Этот элемент был предсказан Д.И.Менделеевым (как Эка-цезий), и был открыт (по его радиоактивности) в 1939 г. Маргаритой Пере, сотрудницей Института радия в Париже с порядковым номером Z = 87 и периодом полураспада 21 мин. Она же дала ему в 1964 г. название в честь своей родины – франций. . Микроскопические количества франция-223 и франция-224 могут быть химически выделены из минералов урана и тория. Другие изотопы франция получают искусственным путём с помощью ядерных реакций.




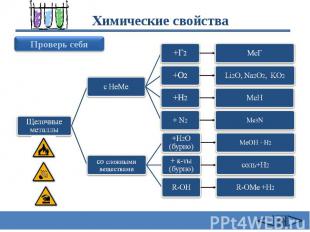

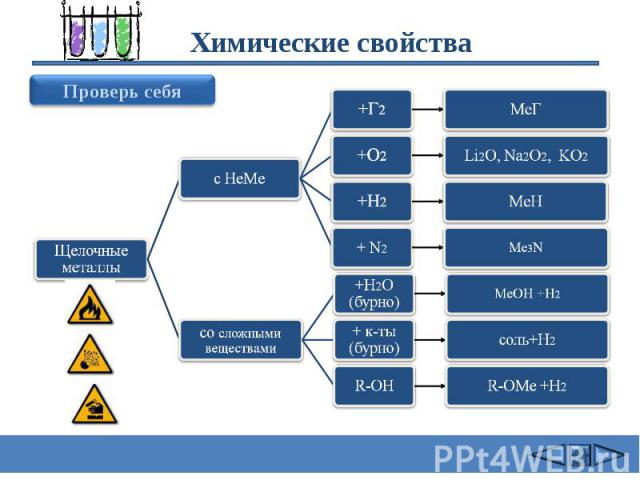
Химические свойства 2Na + Cl2 = 2NaCl (в атмосфере F2 и Cl2 щелочные Me самовоспламеняются) 4Li + O2 = 2Li2O 2Na + O2 = Na2O2 2K + 2O2 = K2O4 оксид Li пероксид Na надпероксид K 3) 2Na + Н2 = 2NaН (при нагревании 200-400oC)4) 6Li + N2 = 2Li3N (Li - при комнатной T, остальные щелочные Me -при нагревании)5) 2Na + 2Н2О = 2NaОН + Н2 (Li - спокойно, Na - энергично, остальные – со взрывом – воспламеняется выделяющийся Н2 Rb и Cs реагируют не только с жидкой Н2О, но и со льдом. .6) 2Na+ Н2SО4 = Na2SО4 + Н2 (протекают очень бурно)7) 2C2H5OH + 2Na = 2C2H5ONa + Н2 Щелочные металлы с водой

Качественное определение щелочных металлов Для распознавания соединений щелочных металлов по окраске пламени исследуемое вещество вносится в пламя горелки на кончике железной проволоки.Li+ - карминово-красный K+ - фиолетовый Cs+ - фиолетово-синийNa+ - желтый Rb + - красный

Получение щелочных металлов 1) Электролиз расплавов соединений щелочных металлов:2МеCl = 2Ме + Cl24МеOH = 4Ме + 2Н2О + О22) Восстановление оксидов и гидроксидов щелочных металлов:2Li2O + Si = 4Li + SiO2KOH + Na = NаOH + K Ванна состоит из стального кожуха с шамотной футеровкой, графитовым анодом А и кольцевым железный катодом К, между которыми расположена сетчатая диафрагма. Электролитом служит более легкоплавкая смесь его с 25% NaF и 12% КСl (что позволяет проводить процесс при 610–650°С). Металлический натрий собирается в верхней части кольцевого катодного пространства, откуда и переходит в сборник. По мере хода электролиза в ванну добавляют NaCl.
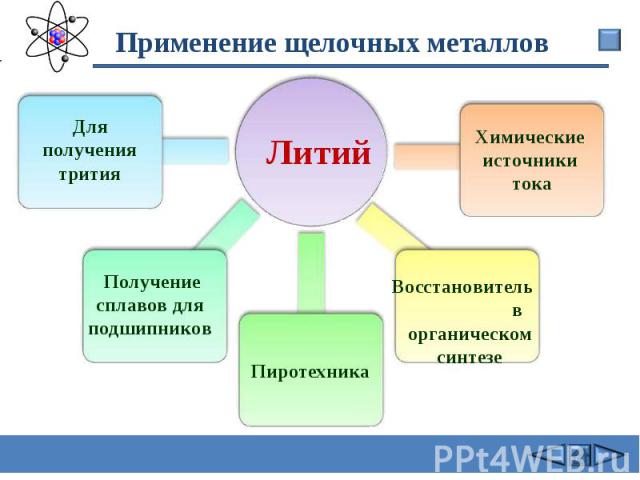
Применение щелочных металлов Литий Для получения трития Получение сплавов для подшипников Пиротехника Химические источники тока Восстановитель в органическом синтезе
Применение щелочных металлов НатрийВосстановитель в органическом синтезеТермическое получение металловПроизводство натриево-серных аккумуляторовГазоразрядныелампыКачественный анализ органических веществТеплоноситель в ядерных реакторах
Применение щелочных металлов Теплоноситель в ядерных реакторах Калийные удобренияВ гальванотехнике Термическое получение металлов Катализатор
Применение щелочных металлов
Применение щелочных металлов

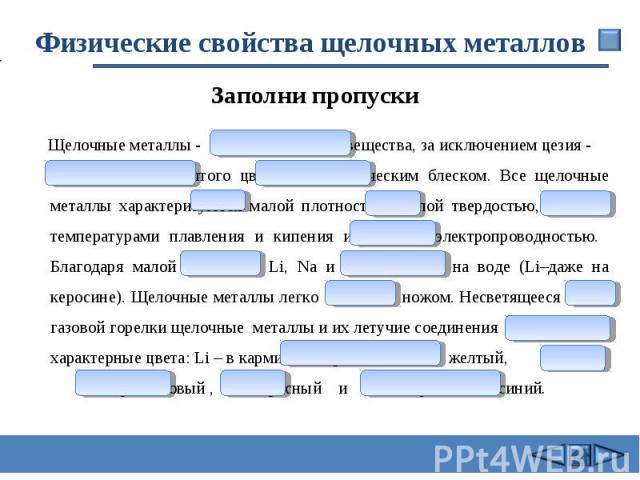
Физические свойства щелочных металлов Щелочные металлы - серебристо–белые вещества, за исключением цезия - серебристо-желтого цвета, с металлическим блеском. Все щелочные металлы характеризуются малой плотностью, малой твердостью, низкими температурами плавления и кипения и хорошей электропроводностью. Благодаря малой плотности Li, Na и К всплывают на воде (Li–даже на керосине). Щелочные металлы легко режутся ножом. Несветящееся пламя газовой горелки щелочные металлы и их летучие соединения окрашивают в характерные цвета: Li – в карминово–красный, Na – в желтый, К – фиолетовый , Rb - красный и Cs – в фиолетово-синий.

Тест «Щелочные металлы» 1. Предложил назвать калий от арабского «алкали» - щелочь И. Арфведсон Г.Деви Й. Берцеллиус 2. В ряду от лития к францию атомный радиус: уменьшается не изменяется увеличивается Степень окисления щелочных металлов равна: +1 -1 +2 4. Цвет пламени, в который его окрашивают ионы натрия фиолетовый красный желтый 5. Соединение NaOH называется. каустическая сода поташ кристаллическая сода
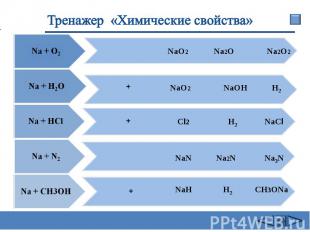
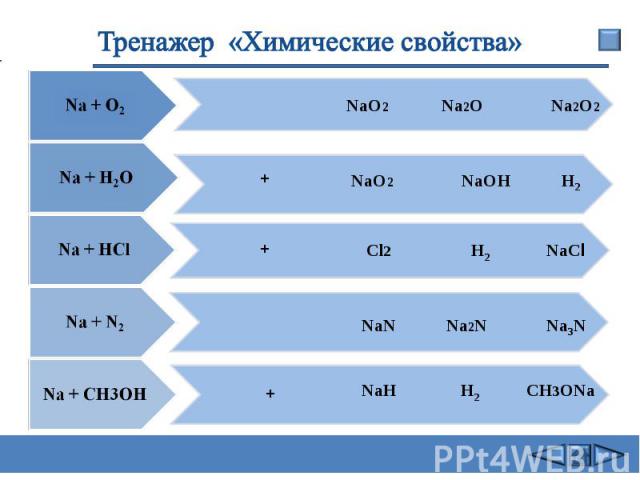
Тренажер «Химические свойства»

Габриелян О.С. Химия. 9 класс: Учеб. для общеобразоват.учебн. заведений.-М.: Дрофа, Ахметов Н. С. Общая и неорганическая химия. — М.: Высшая школа, 2001Лидин Р. А., Андреева Л. Л., Молочко В. А. Справочник по неорганической химии. — М.: Химия, 1987.Некрасов Б. В. Основы общей химии. — М.: Химия, 1974.Неорганическая химия. Весь школьный курс в таблицах,сост. МанкувичН.В., М. 2008г“Видеоопыты из диска "Splint. Химия для всех - XXI: Самоучитель решению химических задач"http://ru.wikipedia.org/wiki/%D0%A5%D0%B8%D0%BC%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9_%D1%8D%D0%BB%D0%B5%D0%BC%D0%B5%D0%BD%D1%82http://www.catalogmineralov.ru/http://www.xumuk.ru/encyklopedia/2/5263.htmlhttp://www.physchem.chimfak.rsu.ru/Source/History/Persones/

Спасибо за урок!Благодарю за сотрудничество.