Презентация на тему: ПРЕДЕЛЬНЫЕ ОДНОАТОМНЫЕ СПИРТЫ

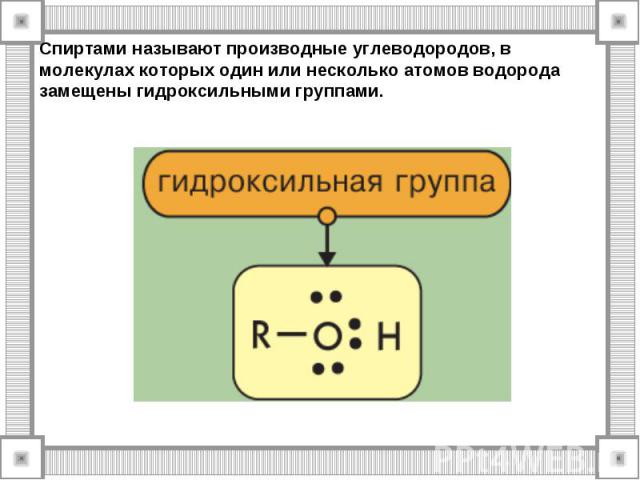
Предельные одноатомные спирты

Цели: Изучить строение, свойства, получение и применение спиртов; Уметь составлять уравнения химических реакций, характеризующих химические свойства спиртов. Уметь применять теоретические знания в осуществлении цепочек превращений и в выполнении тестовых заданий по подготовке учащихся к ЕГЭ по химии.

План: Классификация спиртов. Гомологический ряд. Номенклатура. Изомерия. Способы получения. Строение молекулы спиртов. Химические свойства спиртов. Применение спиртов.


2. По строению радикалов, связанных с атомом кислорода, различают спирты: предельные, или алканолы (например, СH3CH2–OH) непредельные, или алкенолы (CH2=CH–CH2–OH) аллиловый спирт. ароматические (C6H5CH2–OH). Бензиловый спирт. 3. Низшие и высшие спирты (от количества атомов углерода входящих в состав спирта) до С10 – низшие, свыше С10 – высшие. (С12H25–OH – лауриловый, С16H33–OH – цетиловый спирт.
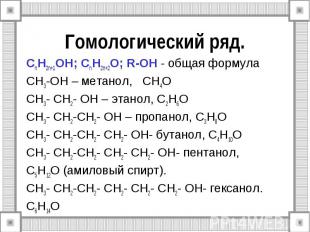
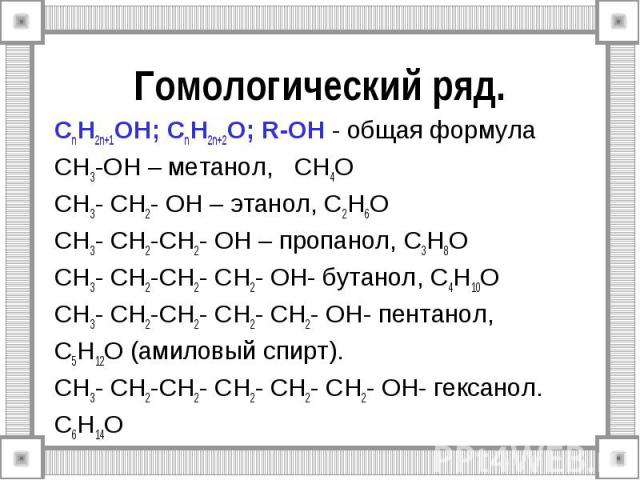
Гомологический ряд. СnH2n+1OH; СnH2n+2O; R-OH - общая формула CH3-OH – метанол, СH4O СH3- CH2- OH – этанол, С2H6O СH3- CH2-СH2- OH – пропанол, С3H8O СH3- CH2-СH2- СH2- OH- бутанол, С4H10O СH3- CH2-СH2- СH2- СH2- OH- пентанол, С5H12O (амиловый спирт). СH3- CH2-СH2- СH2- СH2- СH2- OH- гексанол. С6H14O

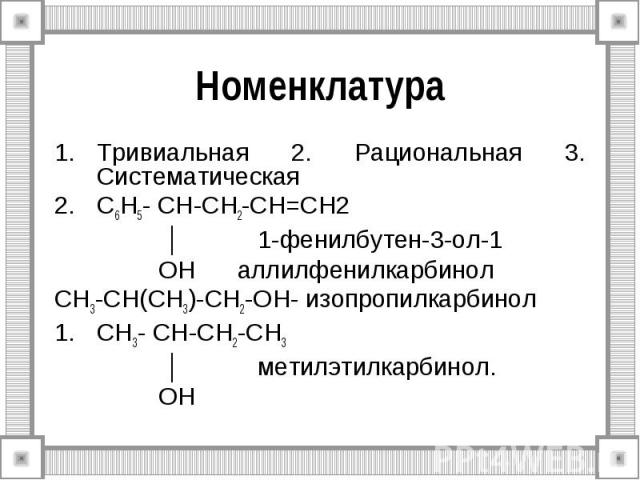
Номенклатура Тривиальная 2. Рациональная 3. Систематическая C6H5- CH-CH2-CH=CH2 │ 1-фенилбутен-3-ол-1 OH аллилфенилкарбинол CH3-CH(CH3)-CH2-OH- изопропилкарбинол CH3- CH-CH2-CH3 │ метилэтилкарбинол. OH


Способы получения предельных одноатомных спиртов. Гидратацией алкенов. Из природного газа. Смесь метана с водяным паром пропускают над катализатором.

3. Ферментативный синтез этанола. 3. Ферментативный синтез этанола. Этанол получают при брожении сахаров, вызываемом ферментами: Лабораторные способы: 1. Гидролиз галогеналканов – под действием водных растворов щелочей. СН3 – СН2 – Cl +NaOH→CH3-CH2-OH+NaCl 2. Из сложных эфиров – при кипячении с разбавленной кислотой или щелочью образуется карбоновая кислота или её соль и спирт. СH3-COOC2H5 + KOH → CH3 – COOK + C2H5OH

3. Восстановлением альдегидов, кетонов, карбоновых кислот. 3. Восстановлением альдегидов, кетонов, карбоновых кислот. СН3 – СО – СН3 + Н2 → СН3 – СНОН – СН3 4.Взаимодействие альдегидов и кетонов с реактивом Гриньяра. Н – СОН + R – MgCl → R – CH2 – OMgCl + H2O → R – CH2OH + MgOHCl


Спирты от С1 до С12 по агрегатному состоянию – жидкости, высшие спирты – твердые вещества. В отличие от углеводородов спиртов нет в газообразном состоянии. Это связано с образованием водородных связей. Спирты – растворители. С увеличением относительной молекулярной массы растворимость спиртов уменьшается. Твердые спирты в воде не растворимы. Температура кипения спиртов выше чем у углеводородов.

Строение молекулы спиртов CH3-CH2 → O←H H-O-H Атом кислорода наиболее электроотрицателен по сравнению с углеродом и водородом, поэтому связи C-O и O-H ковалентные полярные. Более полярна связь в гидроксильной группе. При химических реакциях она может гетеролитический разрываться с отщеплением катиона водорода. Легкость разрыва связи кислород-водород в гидроксидах зависит от природы и степени окисления атома, связанного с группой OH. Чем выше элекроотрицательность и степень окисления этого атома, тем сильнее кислотные свойства.

Невысокая Э.О. углерода и положительный индуктивный эффект этильной группы приводят к тому , что спирты проявляют более слабые кислотные свойства даже по сравнению с водой. Вывод: спирты проявляют очень слабые кислотные свойства, способны вступать в реакции нуклеофильного замещения, элиминирования, окисления.

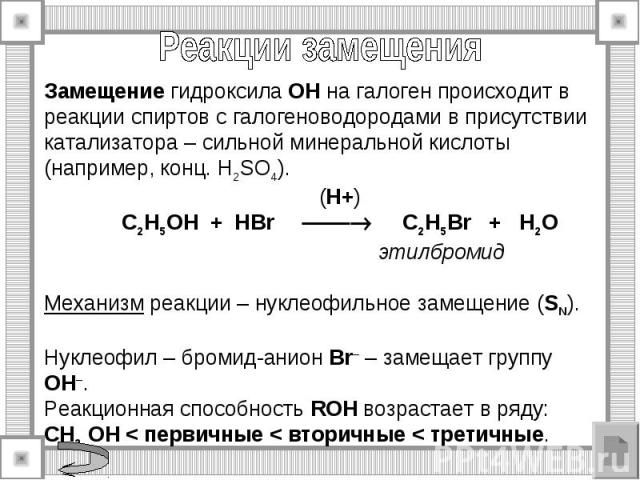
Общая характеристика: соединения реакционноспособны благодаря наличию двух ковалентных связей O-H; C-O. Можно выделить следующие типы реакции: с разрывом связи O-H и C-O.



Реакции взаимодействия спиртов с щелочными и щелочноземельными металлами протекает медленно чем с водой т.к. кислотные свойства выражены очень слабо. С увеличением углеводородного радикала, скорость этой реакции замедляется. В присутствии воды алкаголяты подвергаются гидролизу. C2H5ONa + H2O→ C2H5OH + NaOH Это доказывает, что спирты более слабые кислоты, чем вода.
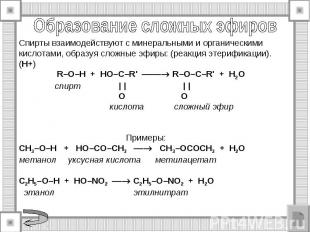
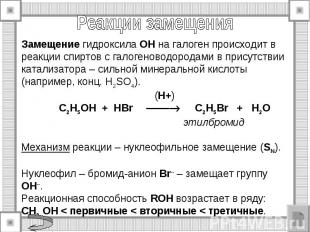

2. Взаимодействие с галогенидами фосфора. C2H5OH + PCl5→ C2H5Cl + POCl3 + HCl хлорокись фосфора 3C2H5OH + PBr3→3C2H5Br +H3PO3 C2H5OH + SOCl2 → C2H5Cl + SO2 + HCl хлористый тионил

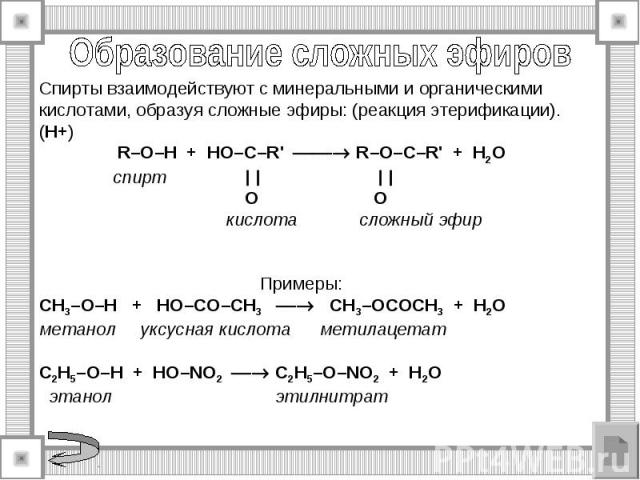
Окисление спиртов. Горение спиртов. Спирты горят на воздухе бледно – голубым пламенем. Спирты с большей молекулярной массой горят светящимся пламенем и после сгорания остается черный налет. C2H5OH + 3O2→2CO2 +3H2O + Q Качественная реакция на спирты. СH3-CH2-OH+CuO→CH3-COH + Cu +H2O CH3-CHOH-CH3 +[O] →CH3-CO-CH3 +H2O

Иодоформная реакция Ее проводят с помощью раствора – реактива Люголя, который получают растворением иода в растворе иодида калия. На первой стадии происходит окисление этилового спирта до уксусного альдегида. CH3-CH2-OH + I2→CH3-COH +2HI 2 cтадия. Замещение атомов водорода метильной группы на атомы иода: CH3-COH + 3I2→I3C-COH +3HI 3.В щелочной среде трииодацетальдегид разлагается на иодоформ и формиат натрия: I3C-COH + NaOH→CHI3 + HCOONa Признак наличия этанола – помутнение смеси и характерный запах иодоформа CHI3.


Дописать уравнения реакции. CH3- CH2-OH + K2Cr2O7 + H2SO4→ CH3- CH2-OH + KMnO4 +H2SO4→


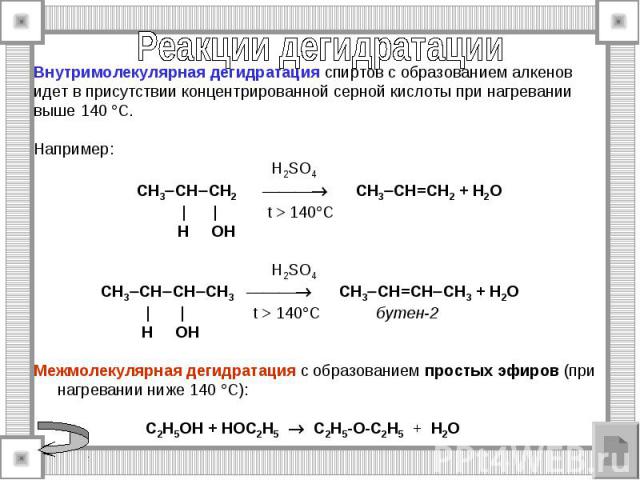
Каталитическое дегидрирование спиртов. CH3-CH2-OH→CH3-COH +H2 CH3-CH-OH-CH3→CH3-CO-CH3 + H2


Ядовитость спиртов. Метиловый спирт – сильный яд! Несколько граммов его, попав в организм человека, вызывает слепоту, а большее количество приводит к смерти. Поэтому метиловый спирт, используемый для технических нужд, объязательно должен носить название метанол – яд. Этиловый спирт(этанол) – бесцветная жидкость с характерным запахом. Спирт, содержащий 4-5% воды, называют ректификатом, а только доли процента – абсолютным спиртом. Этиловый спирт, получаемый брожением сахаристых веществ (в присутствии ферментов, например, дрожжей) называют пищевым или винным спиртом. Спирт, получаемый из глюкозы, которую получают гидролизом целлюлозы, называют гидролизным. Этиловый спирт – сильный наркотик. Спирт, применяемый для технических целей, специально загрязняют дурнопахнущими веществами. Такой спирт называют денатуратом.

Очень часто алкоголь является причиной смертельных отравлений. Особенно опасны всевозможные зарубежные и отечественные суррогаты (заменители) винно- водочного производства.