Презентация на тему: АЗОТНАЯ КИСЛОТА




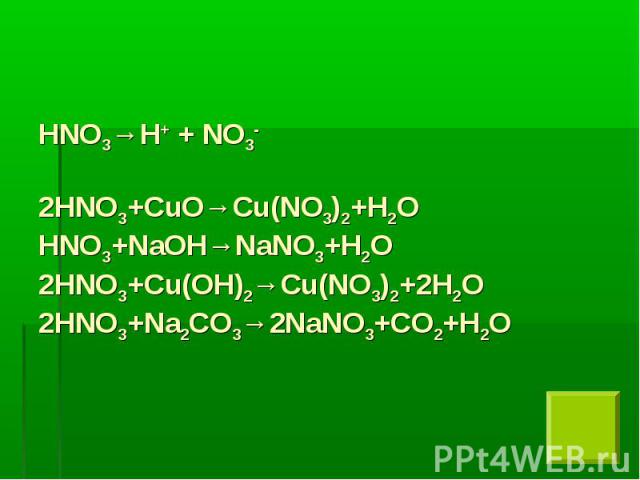
Заряды ионов Заряды ионов + - H NO3



Азотная кислота проявляет все типичные свойства сильных кислот: взаимодействует с оксидами и гидроксидами металлов, с солями (составьте соответствующие уравнения реакций). Азотная кислота проявляет все типичные свойства сильных кислот: взаимодействует с оксидами и гидроксидами металлов, с солями (составьте соответствующие уравнения реакций). С металлами она ведет себя по –особому – ни один из металлов не вытесняет из азотной кислоты водород, независимо от ее концентрации. Почему азотная кислота является сильным окислителем?
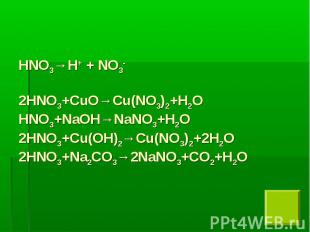

Продукт восстановления зависит от положения металлов в ряду напряжений, от концентрации кислоты и условий проведения реакции. Продукт восстановления зависит от положения металлов в ряду напряжений, от концентрации кислоты и условий проведения реакции. Например, при взаимодействии с медью концентрированная кислота восстанавливается до оксида азота(IV): Cu+HNO3→Cu(NO3)2+NO2+H2O? разбавленная – до оксида азота(ΙΙ): Cu+HNO3→Cu(NO3)2+NO+H2O (расставьте коэффициенты методом электронного баланса). Железо и алюминий при действии концентрированной HNO3 покрываются прочной оксидной пленкой, предохраняющей металл от дальнейшего окисления, т.е. кислота пассивирует их. В чем особенность реакций между металлами и азотной кислотой? Почему азотную кислоту, можно перевозить в стальных и алюминиевых баллонах?

Предложите две цепочки превращений, приводящих к получению азотной кислоты, исходя из азота и аммиака. Предложите две цепочки превращений, приводящих к получению азотной кислоты, исходя из азота и аммиака.



§27, статья «Соли азотной кислоты». §27, статья «Соли азотной кислоты». ? 3 и 7