Презентация на тему: Основные соединения серы

Тема:Cоединения серы и их значение. Урок химии 9 класс 5klass.net

Почему геохимик А.Е.Ферсман назвал серу «двигателем химической промышленности»?

Цели урока: Рассмотреть свойства важнейших соединений серы – сероводорода и её солей, оксидов серы, сероводородной и сернистой кислот Освоить навык определения ионов S2- и сульфит-ионов SО32- Развить способность эффективно использовать знаковые системы, наблюдения, сравнения, делать выводы
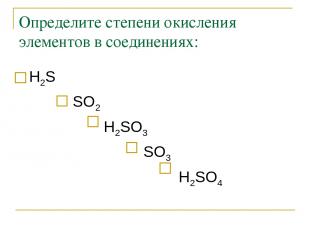
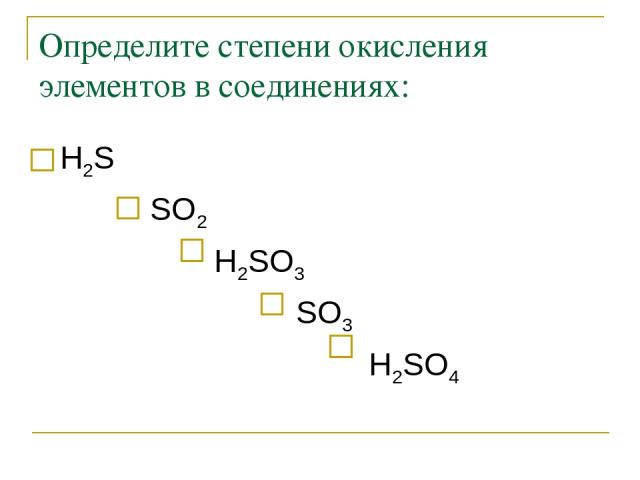
Определите степени окисления элементов в соединениях: Н2S SO2 Н2SO3 SO3 Н2SO4
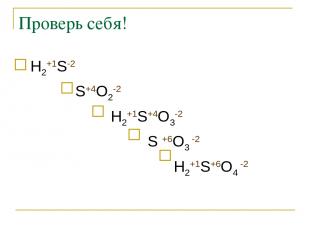
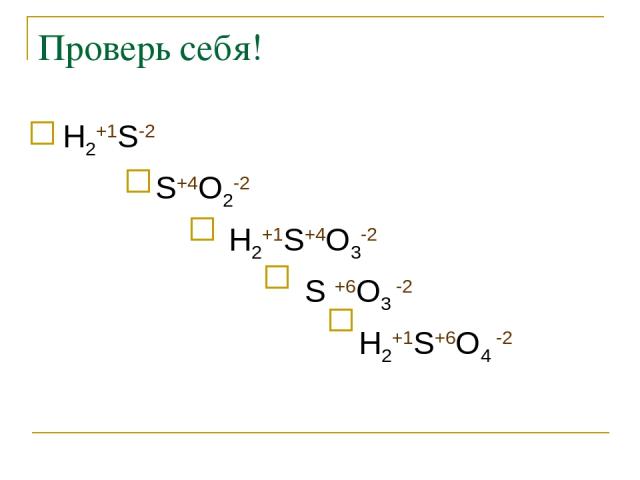
Проверь себя! Н2+1S-2 S+4O2-2 Н2+1S+4O3-2 S +6O3 -2 Н2+1S+6O4 -2

Сероводород Н2S-2(низшая степень окисления) Физические свойства: Бесцветный газ с запахом тухлых яиц, ядовит. Предельно допустимая концентрация в воздухе 10мг/м3 Водный раствор – сероводородная кислота

Пятигорск – природный музей минеральных вод Cероводородные источники. Классификация минеральных вод Пятигорска: углекисло-сероводородные сложного ионно-солевого состава, радоновые воды, углекислые воды (горячие, теплые, холодные), минеральные воды ессентукского типа (углекислые и углекисло-сероводородные)

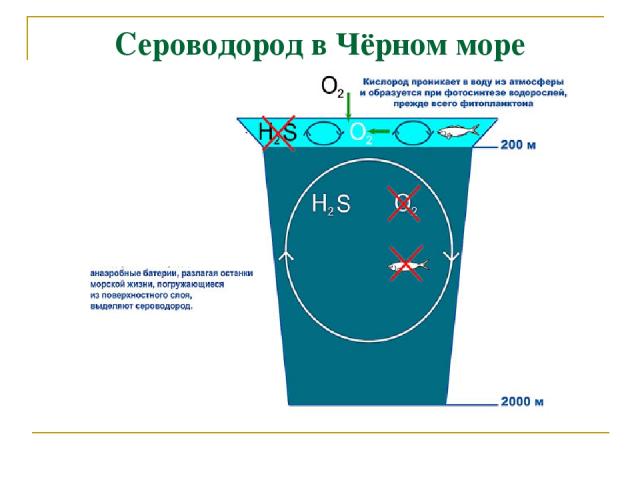
Сероводород в Чёрном море

Н2S-2 - сероводород Химические свойства: 1.Реакция взаимодействия с кислородом (определите степени окисления элементов, расставьте коэффициенты в уравнениях реакций, определите свойства Н2S c позиции окислительно-восстановительных процессов) Вариант -1. Н2S + O2 → S↓ + Н2O недостаток Вариант -2. Н2S + O2 → SО2+ Н2O избыток

Проверь себя! Н2S-2 – восстановитель Вариант -1. 2Н2S-2 + O20 = 2S0↓ + 2Н2O-2 Вариант -2. 2Н2S-2 + 3O20= 2S+4О2+ 2Н2O-2

Н2S -2 - восстановитель 2. Реакция взаимодействия с растворами галогенов: 2Н2S-2 +I20 = 2S0↓ + 2Н+1I-1 йод

Н2S – сероводородная кислота Неустойчивая, на свету мутнеет. Почему? 2,5V Н2S : 1V Н2О Н2S↔Н++ НS- гидросульфид-ион НS- ↔ Н++ S2- сульфид- ион

Cоли: гидросульфиды и сульфиды В природе – 200 минералов-сульфидов Сульфиды свинца (галенит или свинцовый блеск РbS), ртути (киноварь HgS), железа (пирит или железный колчедан FeS2) цинка ( cфалерит ZnS)

Качественная реакция на сульфид-ион S2- В пробирку с раствором соли сульфида натрия Na2S прилейте 1-2 мл раствора соли хлорида меди(II) СuCl2. Что наблюдаете? Рассмотрите реакцию с точки зрения ТЭД, запишите уравнение реакции в трех видах.

Качественная реакция на сульфид-ион S2- Na2S + СuCl2 =2NaCl + СuS↓(черный осадок) 2Na+ +S2- +Cu2+ + 2Cl- =2Na++ 2Cl- + СuS↓ Cu2+ + S2- = СuS↓

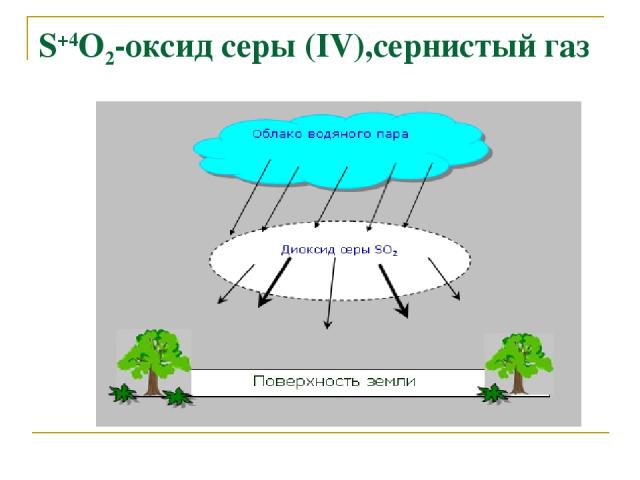
S+4O2-оксид серы (IV),сернистый газ(промежуточная степень окисления)

«Последний день Помпеи» К. П. Брюллов

S+4O2-оксид серы (IV),сернистый газ(промежуточная степень окисления) Физические свойства: бесцветный газ с резким запахом, ядовит. Предельно допустимая концентрация в воздухе 0,06мг/л Получение. S0 +O2 = S+4O2 ↑

Химические свойства: S+4O2 1.Реакция взаимодействия с кислородом (получение SO3) 2S+4O2 + O20= 2S+6O3(кислотный, бесцветная жидкость) 2. Реакция взаимодействия с углеродом S+4O2 +С0 =S0 +СO2
S+4O2-оксид серы (IV),сернистый газ

H2S+4О3- сернистая кислота Существует только в растворе, непрочное соединение 40V SО2 :1 V Н2О SО2 +Н2О ↔Н2 SО3 Н2 SО3 ↔Н+ + НSО3- гидросульфит - ион НSО3- ↔ Н+ + SО32- сульфит – ион

Качественная реакция на сульфит-ион SО32- Na2SО3 +2НСl= 2NaСl + Н2SО3 2Na+ + SО32- +2Н+ +2Сl- =2Na+ +2Сl- + Н2О+ SО2 2Н+ + SО32-= Н2О+ SО2

S+6O3 – оксид серы (VI), кислотный оксид (высшая степень окисления серы) S+6O3- бесцветная жидкость S+6O3 + Н2О =Н2 S+6O4 серная кислота

Как изменяются свойства веществ в зависимости от степени окисления? Почему геохимик А.Е.Ферсман назвал серу «двигателем химической промышленности»? Итоги урока 7-8 баллов- оценка 5 5-6 баллов - оценка 4
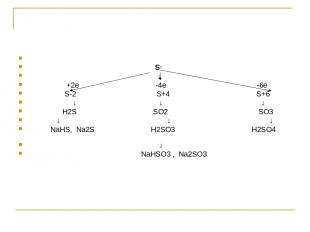
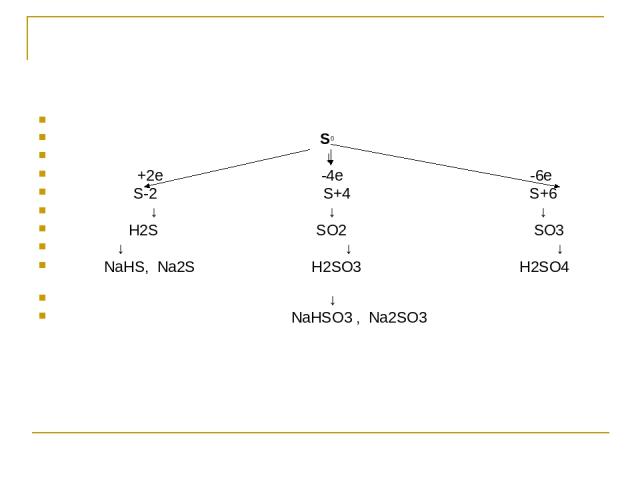
S0 ↓ +2e -4e -6e S-2 S+4 S+6 ↓ ↓ ↓ H2S SO2 SO3 ↓ ↓ ↓ NaHS, Na2S Н2SO3 H2SO4 ↓ NaНSО3 , Na2SО3