Презентация на тему: Основания химия

Основания Химия 8 класс И. Жикина 900igr.net
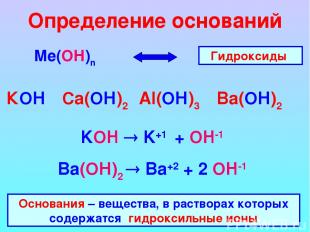
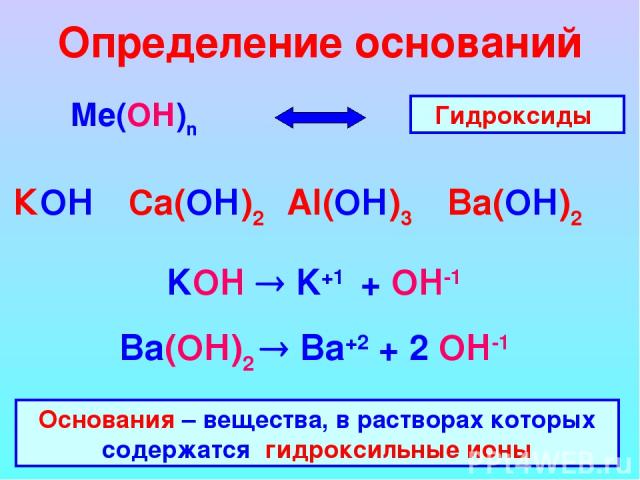
Определение оснований Ме(ОН)n КОН Ca(ОН)2 Al(ОН)3 Ba(ОН)2 Гидроксиды KOH K+1 + OH-1 Ba(ОН)2 Ba+2 + 2 OH-1 Основания – вещества, в растворах которых содержатся гидроксильные ионы
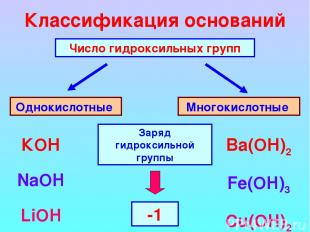
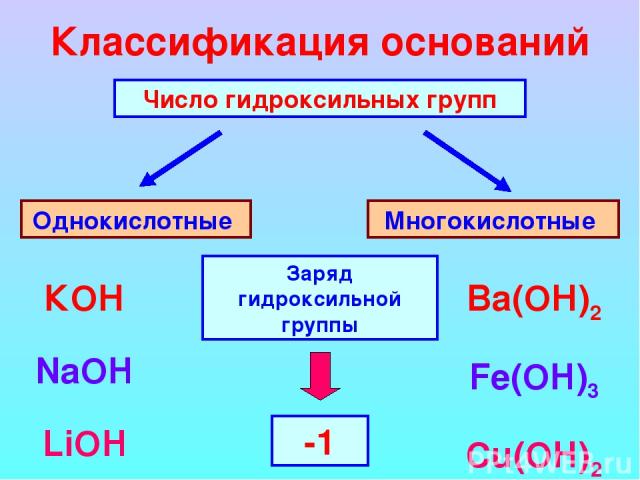
Классификация оснований Число гидроксильных групп Однокислотные Многокислотные КОН NaOH LiOH Ba(ОН)2 Fe(OH)3 Cu(OH)2 Заряд гидроксильной группы -1
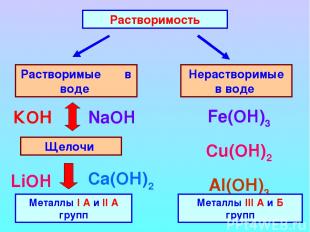
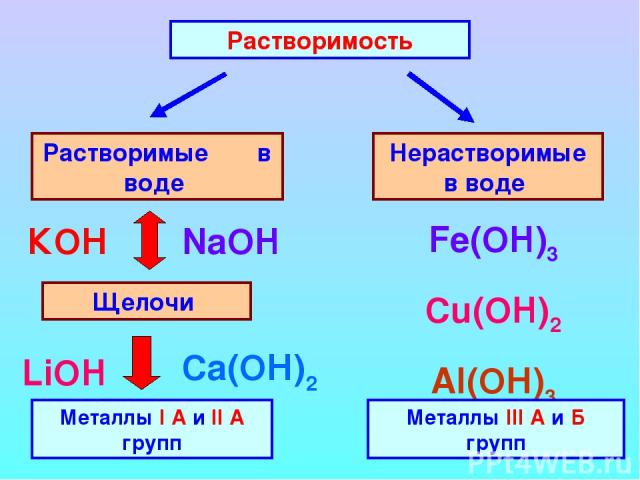
Растворимость Растворимые в воде Нерастворимые в воде Щелочи Металлы I А и II А групп КОН NaOH Ca(ОН)2 LiOH Fe(OH)3 Cu(OH)2 Al(ОН)3 Металлы III А и Б групп

Сильные и слабые основания

Получение оснований Щелочи 2Na + 2H2O 2NaOH + H2 K2O + H2O 2KOH Активный металл + вода Основной оксид + вода
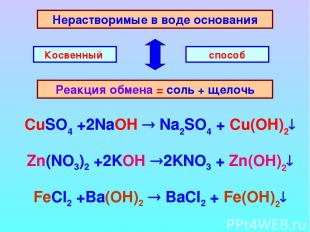
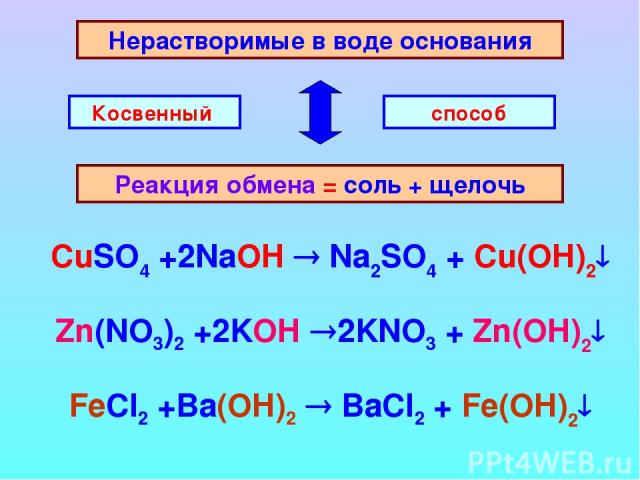
Нерастворимые в воде основания Реакция обмена = соль + щелочь Косвенный способ CuSO4 +2NaOH Na2SO4 + Cu(OH)2 Zn(NO3)2 +2KOH 2KNO3 + Zn(OH)2 FeCl2 +Ba(OH)2 BaCl2 + Fe(OH)2
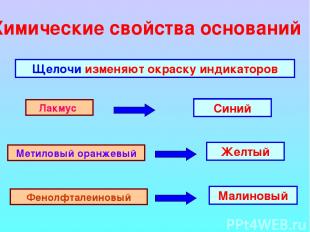
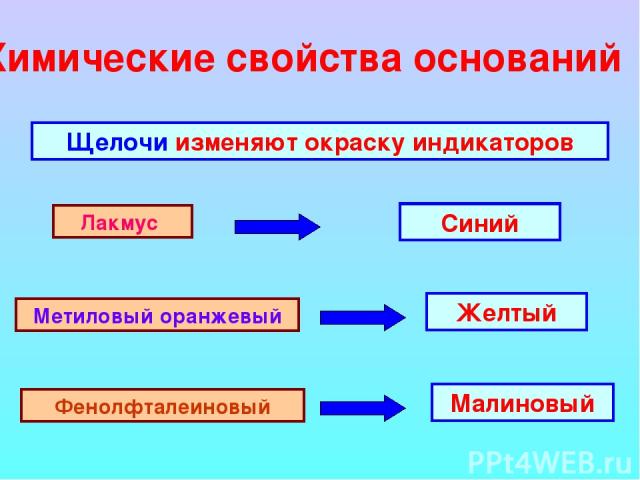
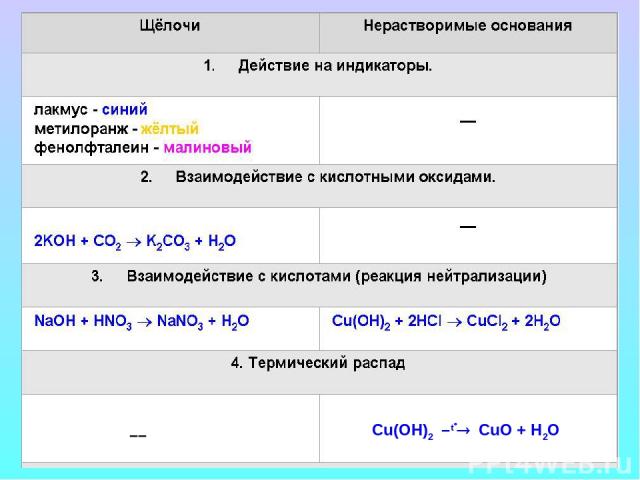
Химические свойства оснований Щелочи изменяют окраску индикаторов Лакмус Метиловый оранжевый Фенолфталеиновый Синий Желтый Малиновый
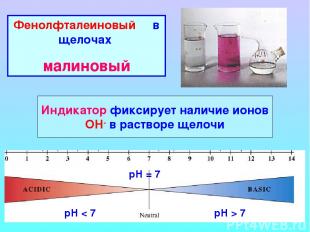
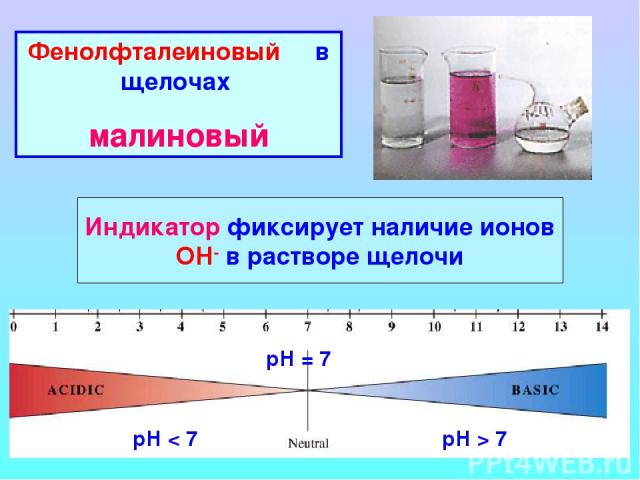
Фенолфталеиновый в щелочах малиновый Индикатор фиксирует наличие ионов ОН- в растворе щелочи рН < 7 рН = 7 рН > 7
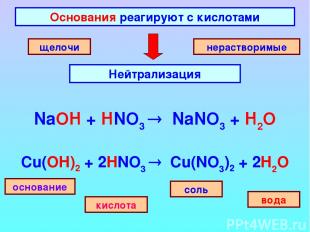
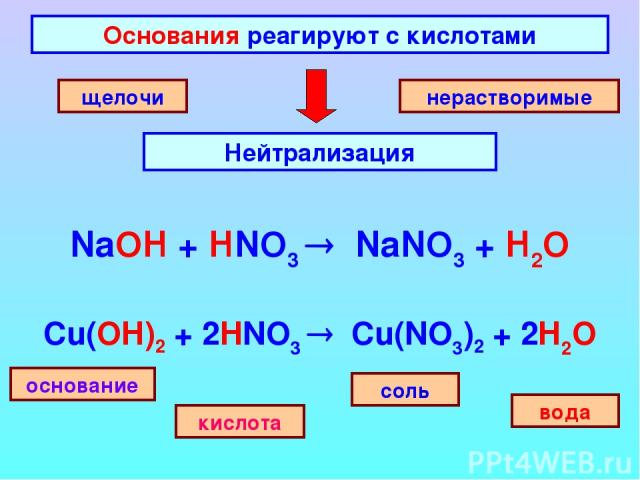
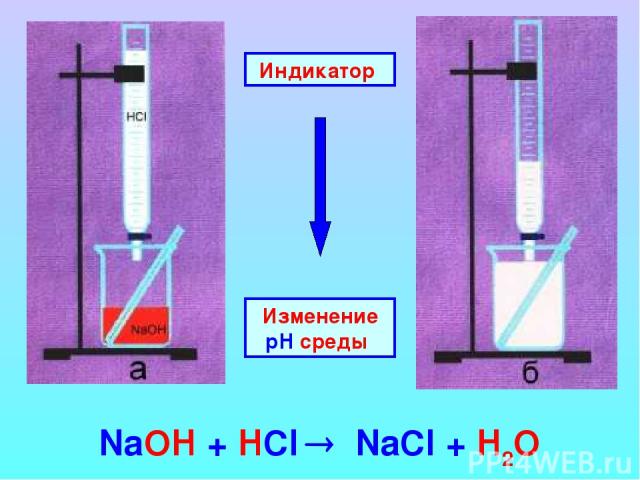
Основания реагируют с кислотами Нейтрализация щелочи нерастворимые основание соль кислота вода

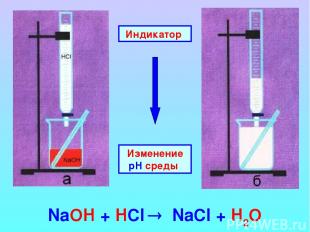
Индикатор Изменение рН среды
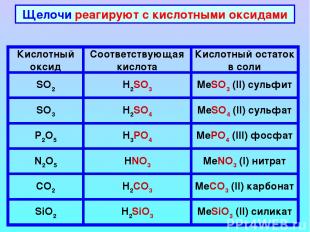
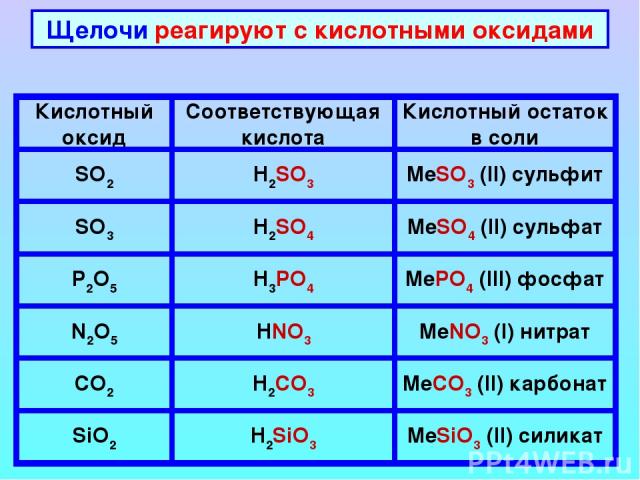
Щелочи реагируют с кислотными оксидами
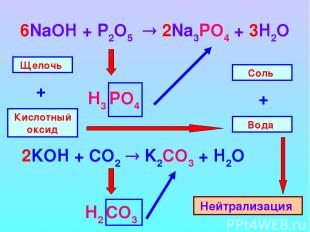
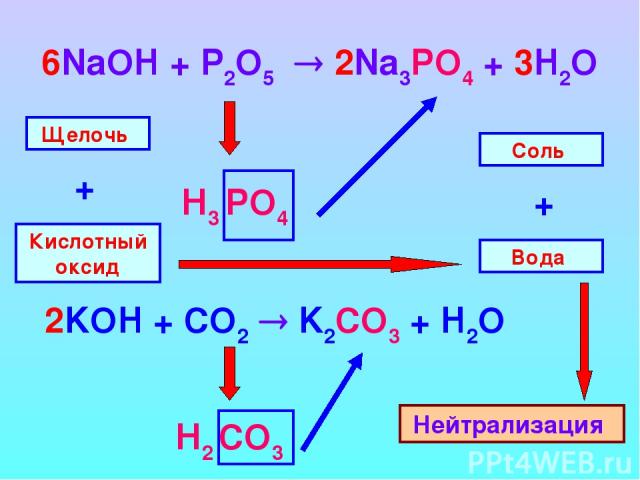
6NaOH + P2O5 2Na3PO4 + 3H2O Н3 PO4 Н2 CO3 Щелочь Кислотный оксид + Вода Соль + Нейтрализация
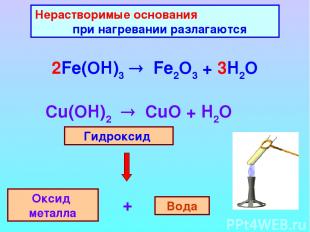
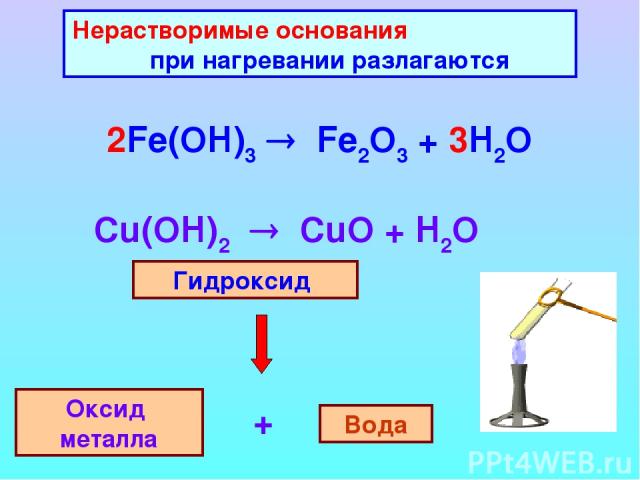
Нерастворимые основания при нагревании разлагаются 2Fe(OH)3 Fe2O3 + 3H2O Гидроксид Оксид металла Вода +
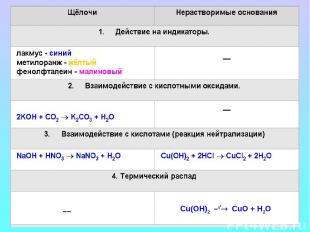
Cu(OH)2 –t°® CuO + H2O ––