Презентация на тему: Метод полуреакций или электронно-ионного баланса

Тема урока: «Метод полуреакций или электронно-ионного баланса»Подготовила и провелаучитель химии Новоникольской СОШКузнецова И.Н.

ЦЕЛИ УРОКА: ЗАКРЕПИТЬ И УГЛУБИТЬ ЗНАНИЯ О СУЩНОСТИ ОВР;ПОЗНАКОМИТЬСЯ С МЕТОДОМ ПОЛУРЕАКЦИЙ И ЕГО ПРИМЕНЕНИЕМ В НЕОРГАНИЧЕСКОЙ И ОРГАНИЧЕСКОЙ ХИМИИНАУЧИТЬСЯ СОСТАВЛЯТЬ УРАВНЕНИЯ ОВР С ИСПОЛЬЗОВАНИЕМ МЕТОДА ЭЛЕКТРОННО-ИОННОГО БАЛАНСА;РАЗВИТЬ НАВЫКИ В ИСПОЛЬЗОВАНИИ МЕТОДА Э.И.Б. ДЛЯ РЕШЕНИЯ РАЗЛИЧНЫХ ТИПОВ ЗАДАЧ, УПРАЖНЕНИЙ, ТЕСТОВ .

Продолжите… Окислительно-восстановительные реакции – это реакции……в ходе которых хотя бы один элемент изменил свою степень окисленияОкислитель – это….атом, молекула или ион принимающий электроны. Во время реакции они восстанавливаются.Восстановитель – это… атом, молекула или ион отдающий электроны. Во время реакции они окисляются.
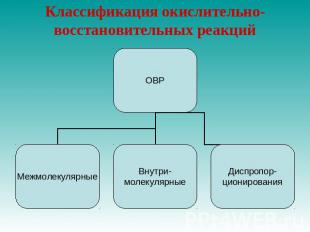
Классификация окислительно-восстановительных реакций

Выполните задание Допишите уравнения реакций, расставьте коэффициенты методом электронного балансаС6C5CH3 + KMnO4 + H2SO4 → C6H5COOH + ..+..+..K2Cr2O7 + K2S + H2O → S↓ +..+..

МЕТОДЫ СОСТАВЛЕНИЯ ОВР Метод электронного баланса Метод электронно - ионного баланса Метод Гарсиа Метод валентных связей

Основное требование Число электронов, отданных восстановителем= числу электронов, принятых окислителем

Электронно- ионный метод(МЕТОД ПОЛУРЕАКЦИЙ) Преимущество: при составлении полуреакцийрассматриваются реально существующие в растворе ионы и наглядно видна роль среды.

МЕТОД ПОЛУРЕАКЦИЙ: Алгоритм1. Записать в ионном виде восстановитель, окислитель и продукты их взаимодействия: Сильные электролиты записывают в виде ионов, а слабые электролиты - газы↑, нерастворимые вещества↓ - в виде молекул.

II. При составлении полуреакций окисления и восстановления следует учитывать следующее: 1. Если исходное вещество содержит больше атомов кислорода, чем продукт реакции, то освобождающийся кислород в форме О-2 связывается в кислых растворах ионами водорода (Н+) - в воду в нейтральных и щелочных растворах - в гидроксид-ионы.В кислых растворах: О-2 + 2Н+ = Н2ОВ нейтральных растворах: О-2 + Н+ (НОН) = ОН-В щелочных растворах : О-2 + НOH = 2ОН-

алгоритм 2. Если исходное вещество содержит меньше атомов кислорода, чем продукты реакции, то недостаток их восполняется в кислых и нейтральных растворах за счёт молекул воды ,в щелочных - за счёт гидроксид-анионов.В кислых растворах : Н2О = О-2 + 2Н+ В нейтральных растворах: Н2О = О-2 + 2 Н+ В щелочных растворах: 2ОН- = О-2 + Н2О

Алгоритм расстановки коэффициентов методом полуреакций Запишите схему реакции в молекулярной форме:KMnO4 + Na2SO3 + H2SO4MnSO4 + Na2SO4 + K2SO4 + H2O

2. Составьте схему реакции в полной ионной форме, подчеркнув восстановитель и окислитель K+ + MnO4- + 2Na+ + SO32- + 2 H+ + SO42-Mn 2+ + SO42- +2Na+ + SO42-+2 K+ + SO42- +H2O

3. Составьте сокращенную молекулярно-ионную схему MnO4- + SO32- + 2 H+ + SO42-Mn 2+ + SO42- + SO42-+ K+ + SO42- +H2O

4. Определите характер среды – кислая, щелочная, нейтральная Наличие Н+ – среда кислая

5. Выписать частицы, изменившие состав и заряд: MnO4- Mn 2+SO32- SO42-

6. Составьте молекулярно-ионные уравнения для процессов окисления и восстановления с учетом характера среды Проверьте число атомов (О) в левой и правой частях уравнений - Проверьте число атомов каждого элемента MnO4-+8H+=Mn2++4H2OSO32-+H2O=SO42-+2H+

Проверьте суммы зарядов ионов в левой и правой частях молекулярно-ионных уравнений: Если сумма зарядов исходных частиц больше суммы зарядов продуктов реакции, то к левой части надо добавить соответствующее число электронов, а если меньше — вычесть
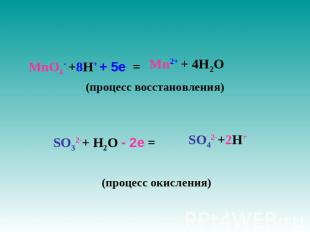
MnO4- +8H+ + 5е = (процесс восстановления) SO32-+ H2O - 2е = (процесс окисления)

8. Найдите коэффициенты восстановителя, окислителя и продуктов их превращения. Умножьте левую и правую части обоих уравнений на найденные коэффициенты MnO4-+ 8H+ + 5е = Mn2++4H2O SO32-+ H2O - 2е = SO42-+2H+

Составьте сокращенное ионное уравнение окислительно-восстановительной реакции. Для этого:сложите уравнения полуреакций сократите, если имеются, одинаковые частицыдобавьте в левую часть уравнения необходимое число сопутствующих противоположно заряженных ионов (см. стрелки) то же число тех же ионов добавьте в правую часть уравнения

2MnO4-+ 5SO32-+ + = 2Mn2+ + + 5SO42-+ ↑ ↑ ↑+2К+ + 10Nа+ + 3SO42- +2К+ + 10Nа+ + 3SO42-

10. Составьте полное молекулярно-ионное уравнение 2К+ +2MnO4-+ 10Nа+ + 5SO32-+6H+ + 3SO42- = = 2Mn2++ 2К+ + 10Nа+ + 8SO42- + 3H2O

11. По полному молекулярно-ионному уравнению составьте полное молекулярное уравнение 2KMnO4+5Na2SO3+3H2SO42MnSO4+ 5Na2SO4+K2SO4 + 3H2O