Презентация на тему: Кислород 8 класс

Кислород

Кислород как элемент. 1. Элемент кислород находится в VI группе, главной подгруппе, II периоде, порядковый номер №8, Ar = 16. 2. Строение атома: +8О ) ) 1S2S2 2P4 2 6 валентность II, степень окисления -2 (редко +2; +1; -1). 3. Входит в состав оксидов, оснований, солей, кислот, органических веществ, в том числе живых организмов. (Примеры?)

Кислород как элемент (продолжение). 4. В земной коре его 49%, в воде – 89%. 5. В составе воздуха (в виде простого вещества) – 20-21% по объёму. Состав воздуха: О2 – 20-21 %; N2 – 78%; CO2 – 0,03%, остальное приходится на инертные газы, пары воды, примеси. Дополнительно … Кислород является самым распространённым элементом нашей планеты. По весу на его долю приходится примерно половина общей массы всех элементов земной коры.

Способы получения и собирания кислорода. Способы получения и собирания кислорода.

Способы получения и собирания кислорода (продолжение). ! Катализатор – вещество, изменяющее скорость реакции, но само при этом не расходующееся. в) перманганата калия при нагревании: 2KMnO4 → K2MnO4 + MnO2 + O2 Разложение этой соли идёт при нагревании её выше 2000 С.

Опыты получения кислорода.

Проверка собравшегося кислорода
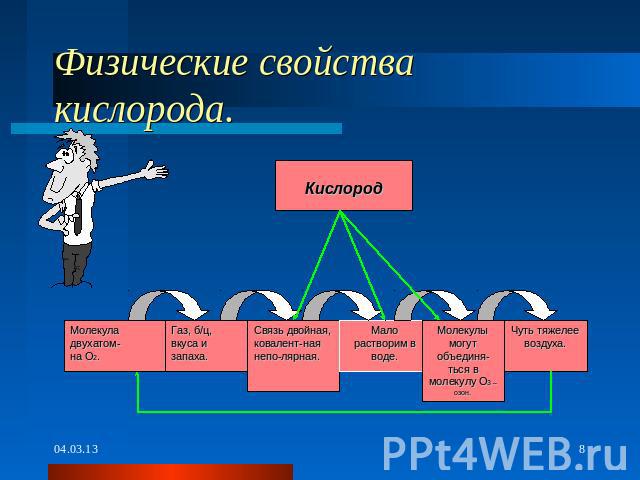
Физические свойства кислорода.

Химические свойства кислорода кислород обладает высокой электроотрицательностью; в реакциях выступает окислителем; поддерживает процессы горения и медленного окисления, к которым относится, например, дыхание.
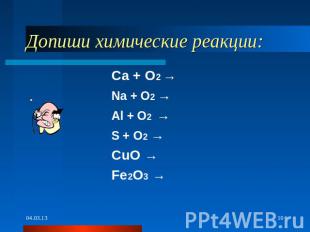
Допиши химические реакции: Ca + O2 → Na + O2 → Al + O2 → S + O2 → CuO → Fe2O3 →

Как погасить горящую древесину? Загоревшуюся на человеке одежду? Горящую на поверхности воды нефть?

Применение кислорода: Находит широкое применение в медицине и промышленности. При высотных полётах лётчиков снабжают специальными приборами с кислородом. При многих лёгочных и сердечных заболеваниях, а также при операциях дают вдыхать кислород из кислородных подушек. Кислородом в баллонах снабжают подводные лодки. Горение рыхлого горючего материала, пропитанного жидким кислородом, сопровождается взрывом, что даёт возможность применять кислород при взрывных работах. Жидкий кислород применяют в реактивных двигателях, в автогенной сварке и резке металлов, даже под водой.