Презентация на тему: Химические свойства предельных углеводородов

Предельные углеводороды

Алканы CnH2n+2

Химические свойства

1. Реакции замещения: 1. Реакции замещения: CH₄ + Cl₂ → CH₃Cl + HCl Реакции протекают по радикальному механизму.

3.Реакции дегидрирования: 3.Реакции дегидрирования: При t = 1500°С происходит межмолекулярное дегидрирование метана по схеме:
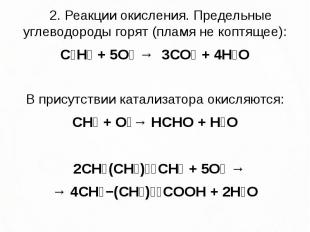
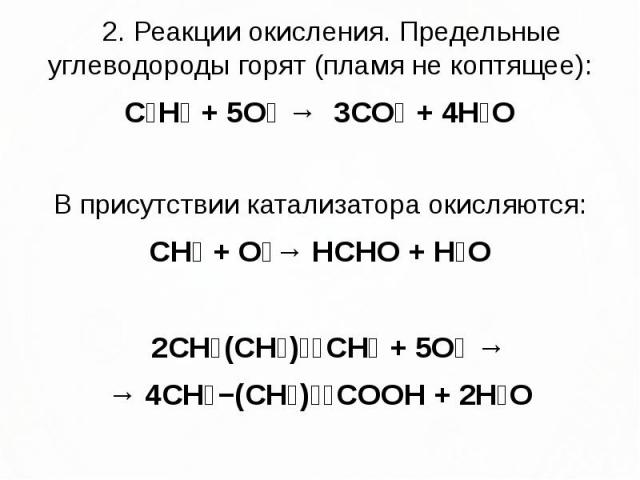
2. Реакции окисления. Предельные углеводороды горят (пламя не коптящее): 2. Реакции окисления. Предельные углеводороды горят (пламя не коптящее): C₃H₈ + 5O₂ → 3CO₂ + 4H₂O В присутствии катализатора окисляются: CH₄ + O₂→ HCHO + H₂O 2CH₃(CH₂)₃₄CH₃ + 5O₂ → → 4CH₃−(CH₂)₁₆COOH + 2H₂O
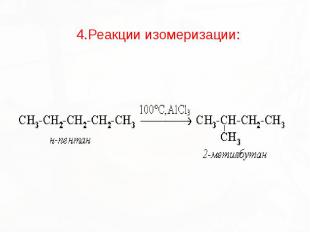
4.Реакции изомеризации:

Крекинг нефти и нефтепродуктов: C16H34 → C8H18 + C8H16 (t,катализатор) C8H18 → С4H10 +C4H8 (t,катализатор) С4H10 → C2H6 +C2H4 (t,катализатор)
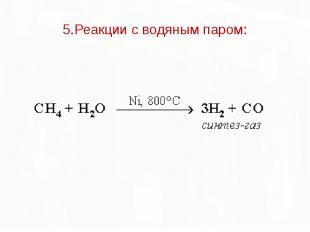
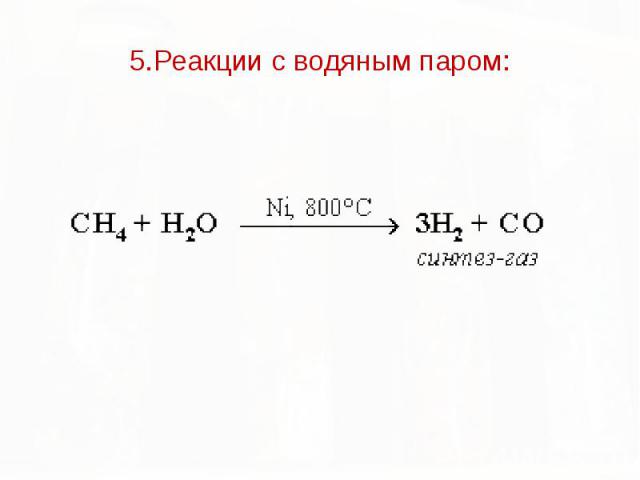
5.Реакции с водяным паром:

Применение

1.Широко используются в качестве топлива, в том числе для двигателей внутреннего сгорания. 1.Широко используются в качестве топлива, в том числе для двигателей внутреннего сгорания. 2.В органическом синтезе. Из них получают хлорпроизводные, метанол, формальдегид, органические кислоты. 3.Путем дегидрирования получают непредельные углеводороды, водород и сажу.