Презентация на тему: Фосфор

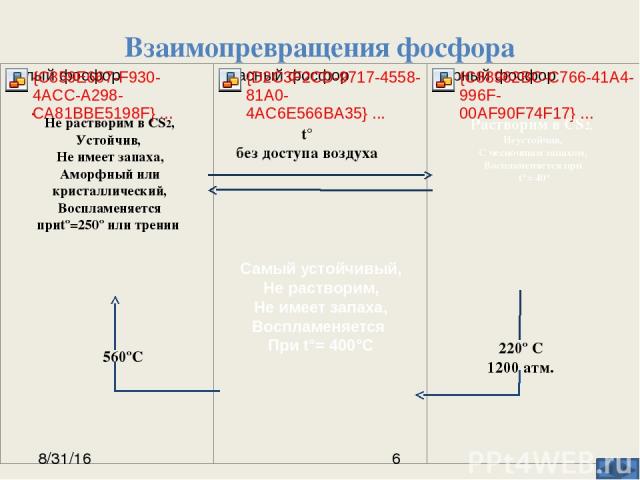
Взаимопревращения фосфора t° без доступа воздуха 220º С 1200 атм. 560ºС . Растворим в CS2, Неустойчив, С чесночным запахом, Воспламеняется при t°= 40° Самый устойчивый, Не растворим, Не имеет запаха, Воспламеняется При t°= 400°C Не растворим в CS2, Устойчив, Не имеет запаха, Аморфный или кристаллический, Воспламеняется приtº=250º или трении
Фосфор в природе Содержание в земной коре Нахождение в природе Фосфорит и апатит - Ca3(PO4)2 13-й по распространенности элемент
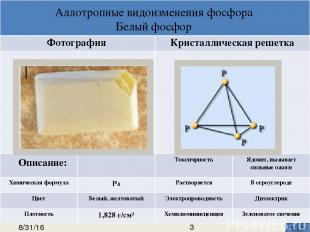
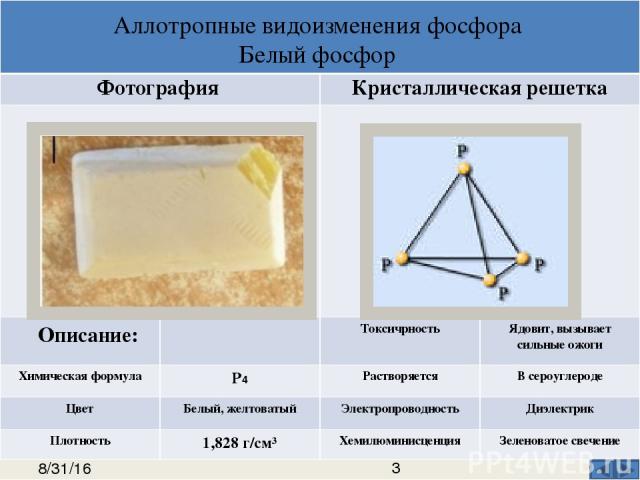
Аллотропные видоизменения фосфора Белый фосфор Описание: Фотография Кристаллическая решетка Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Токсичность Неядовит Химическаяформула (Р4)n Растворяется Втрибромидефосфора Цвет От темно-красного до фиолетового Электропроводность Диэлектрик Плотность От 2,0 до 2,4г/см³ Хемилюминисценция Отсутствует
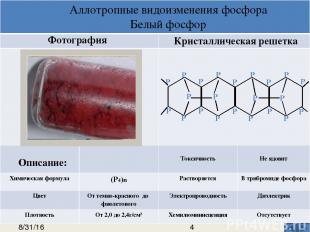
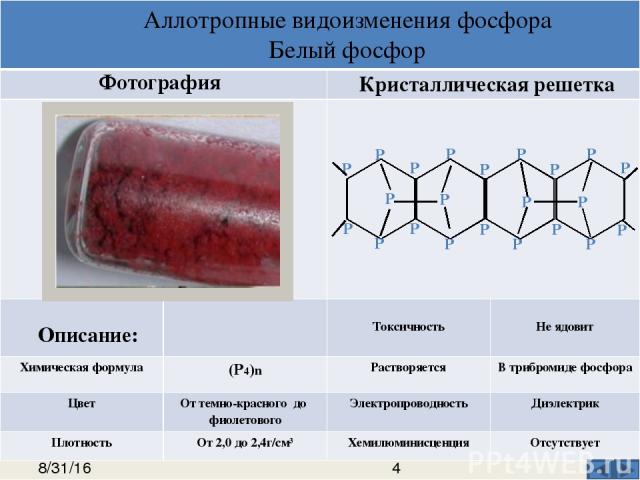
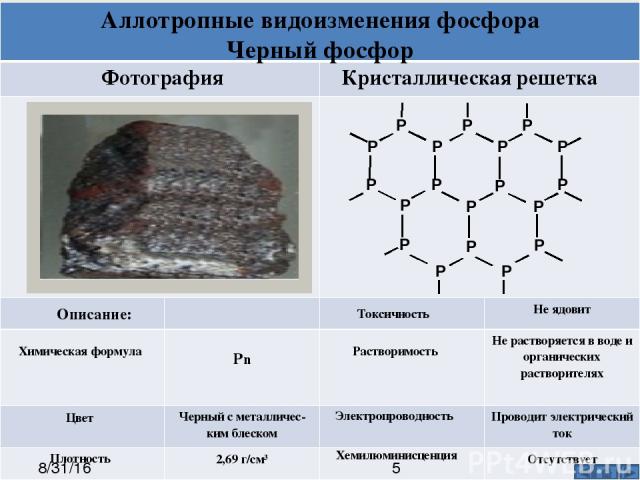
Описание: Химическая формула Цвет Плотность Кристаллическая решетка Фотография Токсичность Растворимость Электропроводность Хемилюминисценция Аллотропные видоизменения фосфора Черный фосфор Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Р Неядовит Рn Не растворяется в воде и органических растворителях Черныйсметалличес-кимблеском Проводит электрический ток 2,69 г/см³ Отсутствует
Химические свойства фосфора
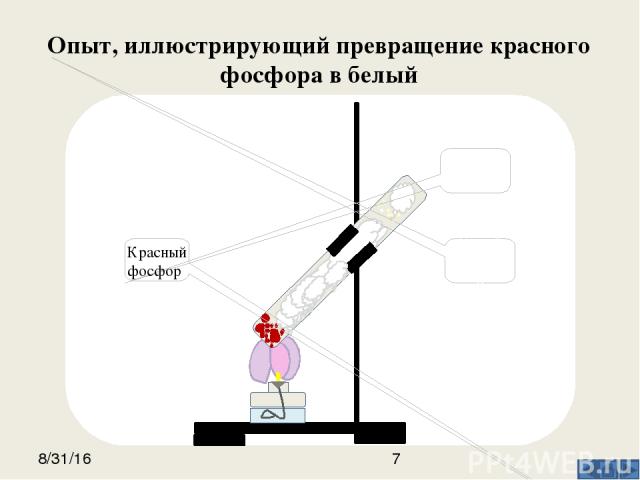
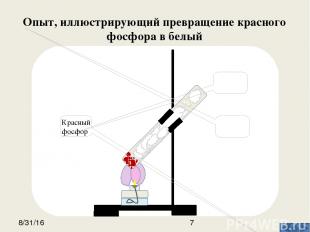
Опыт, иллюстрирующий превращение красного фосфора в белый Вата Белый фосфор Красный фосфор
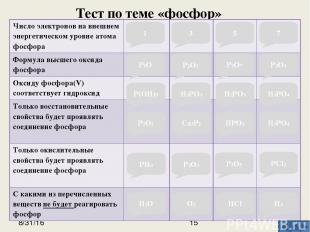
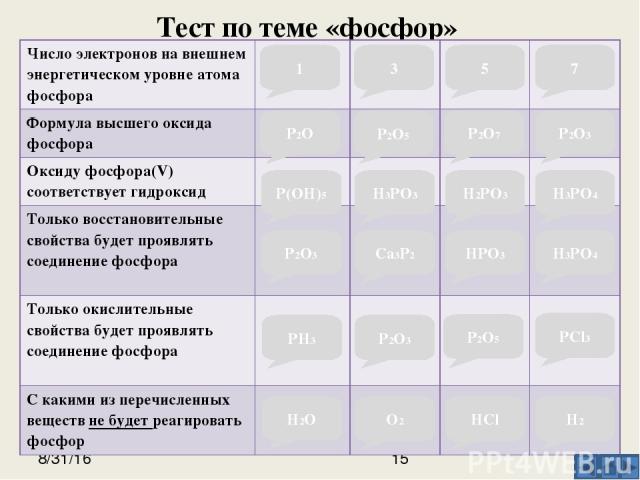
Тест по теме «фосфор» 1 5 7 3 P2O3 P2O7 P2O5 P2O P(OH)5 H3PO3 H2PO3 H3PO4 H3PO4 HPO3 Ca3P2 P2O3 PH3 P2O3 P2O5 PCl3 H2 HCl O2 H2O Число электронов на внешнем энергетическом уровне атома фосфора 1 3 5 7 Формула высшего оксида фосфора Ошибка! Верно! Ошибка! Ошибка! Оксиду фосфора(V)соответствуетгидроксид Ошибка! Ошибка! Ошибка! Верно! Только восстановительные свойства будет проявлять соединение фосфора Ошибка! Верно! Ошибка! Ошибка! Только окислительные свойства будет проявлять соединение фосфора Ошибка! Ошибка! Верно! Ошибка! С какими из перечисленных веществне будетреагировать фосфор Верно! Ошибка! Верно! Ошибка!

Получение Фосфора Фосфор получают из фосфоритов и апатитов, нагревая их в электрической печи без доступа воздуха:

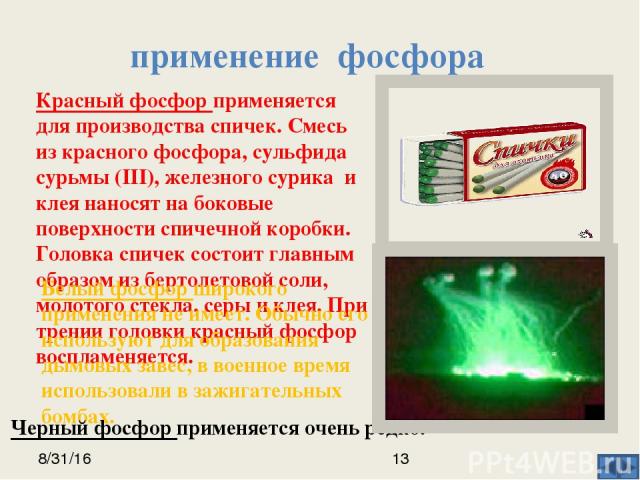
применение соединений фосфора
Источники информации: 1. Г.Е.Рудзитис, Ф.Г. Фельдман « Химия 9», М «Просвещение» 2009 http://images.yandex.ru/yandsearch?text=&stype=image 3.chemistry.narod.ru/himiya/uch_chem_neorgan06.htm http://ru.wikipedia.org/wiki/Фосфор http://images.yandex.ru/yandsearch?text=&rpt=image 6.http://www.udec.ru/udobreniya/fosfornye_udobrenia.php http://images.yandex.ru/yandsearch?text=H3PO4&rpt=image 8.http://images.yandex.ru/yandsearch?text=cgbxrb&rpt=image