Презентация на тему: СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ

ТЕМА УРОКА: СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ ЦЕЛЬ: Познакомиться с понятием «скорость химической реакции». ЗАДАЧИ: Выяснить суть понятия скорости химической реакции; Установить факторы, влияющие на скорость химической реакции в результате исследовательской работы.

Е С Е Ч И М И Н И Ь Е Т Р О Н А В О Ш З М Е Л Е К Е М Б А Е Н Щ Н И Е Ж Е Н Е В Е И З А Р И Л П Р О Е Н Д С Е И Н Е И Химическая реакция – это … одних веществ в другие. (1) Перечислите основные типы химических реакций?(2,3,4) Какие условия должны быть выполнены, чтобы началась химическая реакция? (5,6) 1 2 3 4 5 6 Химический кроссворд.
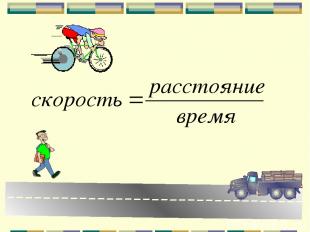

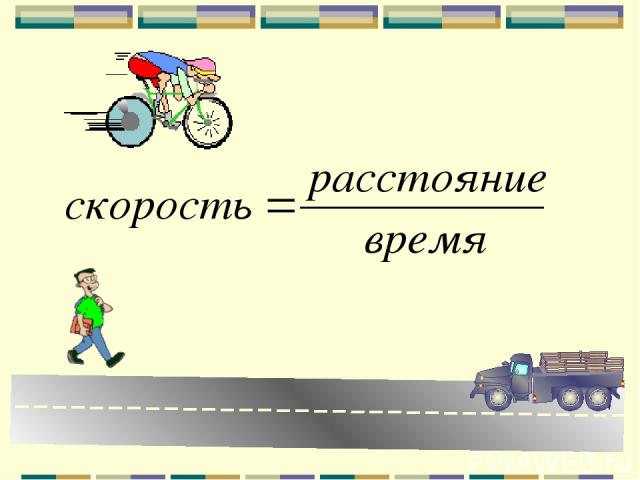
Скорость химической реакции Быстрота протекания химической реакции, т.е. превращения веществ в единицу времени.

Как вы считаете, все химические реакции протекают с одинаковой скоростью? Можно ли управлять скоростью протекания химической реакции?

Проведём исследование Каждая группа выполняет опыт строго следуя инструктивным картам !

Повторим основные правила техники безопасности. Если в руках у вас жидкое - не разлейте, порошкообразное - не рассыпьте. Если включили - выключите. Если открыли - закройте. Если разобрали - соберите. Если вы не можете собрать - позовите на помощь учителя. Если вы пользуетесь чем-либо, держите в чистоте и порядке. Если вы привели что-либо в беспорядок - исправьте. Если вы сдвинули что-нибудь - верните на место. Если вы хотите воспользоваться чем-либо, попросите разрешения. Если вы не знаете, как это действует, ради бога, не трогайте. Если вы не знаете, как это делается - сразу спросите. Если вы не можете что-либо понять - почешите в затылке.

Факторы влияющие на скорость реакции Концентрация Природа реагирующих веществ Температура Катализатор Площадь соприкосновения
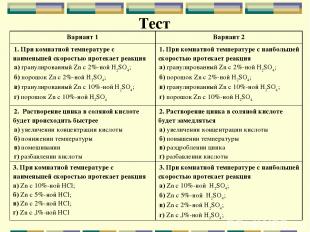
Тест Вариант 1 Вариант 2 1. При комнатной температуре с наименьшей скоростью протекает реакция а) гранулированный Zn с 2%-ной H2SO4; б) порошок Zn с 2%-ной H2SO4; в) гранулированный Zn с 10%-ной H2SO4; г) порошок Zn с 10%-ной H2SO4 1. При комнатной температуре с наибольшей скоростью протекает реакция а) гранулированный Zn с 2%-ной H2SO4; б) порошок Zn с 2%-ной H2SO4; в) гранулированный Zn с 10%-ной H2SO4; г) порошок Zn с 10%-ной H2SO4 2. Растворение цинка в соляной кислоте будет происходить быстрее а) увеличении концентрации кислоты б) понижении температуры в) помешивании г) разбавлении кислоты 2. Растворение цинка в соляной кислоте будет замедляться а) увеличении концентрации кислоты б) повышении температуры в) раздроблении цинка г) разбавлении кислоты 3. При комнатной температуре с наименьшей скоростью протекает реакция а) Zn с 10%-ной НСl; б) Zn с 5%-ной НСl; в) Zn с 2%-ной НСl; г) Zn c ,l%-ной HCl 3. При комнатной температуре с наибольшей скоростью протекает реакция а) Zn с 10%-ной H2SO4; б) Zn с 5%-ной H2SO4; в) Zn с 2%-ной H2SO4; г) Zn c ,l%-ной H2SO4;

КЛЮЧ ДЛЯ САМОПРОВЕРКИ ТЕСТА 1 ВАРИАНТ 1 – А, 2 – А, 3 – Г. 2 ВАРИАНТ 1 – Г, 2 – Г, 3 – А. Ключ к оценке качества выполнения теста: «5» - 0 ошибок; «4» - 1 ошибка «3» - 2 ошибки Ошибками являются неверные ответы.

Тема урока: СКОРОСТЬ ХИМИЧЕСКИХ РЕАКЦИЙ Задачи урока: Выяснить суть понятия «скорость химической реакции». Установить факторы, влияющие на скорость химической реакции. Скорость химической реакции – превращения веществ в единицу времени. Исследование: Факторы, влияющие на скорость реакции: 1. Природа реагирующих веществ. 2. Площадь соприкосновения реагирующих веществ. 3. Концентрация реагирующих веществ. 4. Температура. 5. Катализаторы. Домашнее задание:

Рефлексия: Зеленая - «урок понравился, я все понял» Синяя - « урок не очень понравился, я почти ничего не понял» Красная - «урок не понравился, я сомневаюсь, что все понял». Подумайте и поднимите ту сигнальную карту которая соответствует вашему настроению в данный момент. У вас на столах есть сигнальные карты (зеленая, красная, синяя).

Домашнее задание: Опорный конспект Повторить и заполнить опорный конспект: Количество вещества – это… Единицы измерения количества вещества - … Объем вещества- … Единицы измерения объема вещества - …

Спасибо за внимание! Желаю вам успехов! Удачи!