Презентация на тему: Фосфор, строение, свойства

Фосфор, строение, свойства Фосфор – элемент жизни и мысли.А.Е. Ферсман

План урока 1)СРАВНИТЕЛЬНАЯ ХАРАКТЕРИСТИКА АТОМОВ ФОСФОРА И АЗОТА;2)ФОСФОР, КАК ПРОСТОЕ ВЕЩЕСТВО ;АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ФОСФОРА;3)ИСТОРИЯ ОТКРЫТИЯ ФОСФОРА;4)ПОЛУЧЕНИЕ ФОСФОРА;5)ХИМИЧЕСКИЕ СВОЙСТВА ФОСФОРА;6)НАХОЖДЕНИЕ В ПРИРОДЕ;7)ПРИМЕНЕНИЕ ФОСФОРА.

1)Составьте сравнительную характеристику фосфора и азота, заполнив таблицу.

2)СРАВНИТЕ СВОЙСТВА АТОМА ФОСФОРА СО СВОЙСТВАМИ ЭЛЕМЕНТОВ, СТОЯЩИМИ РЯДОМ В ПЕРИОДЕ И ПОДГРУППЕ. N Si P S As
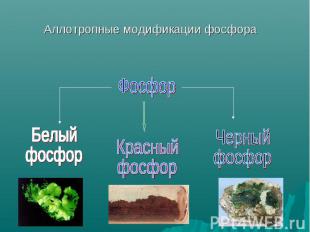
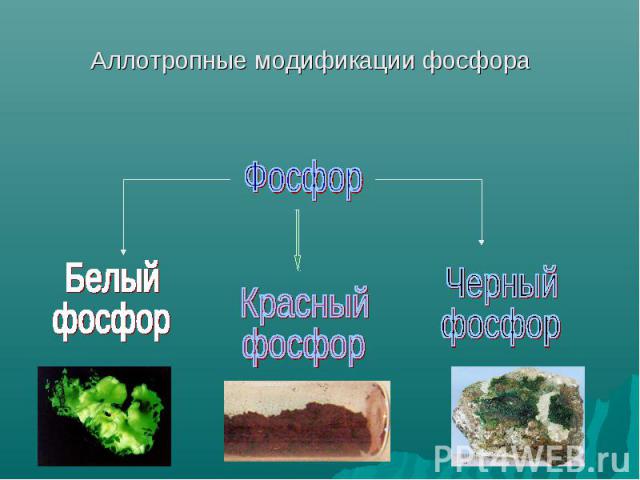
Аллотропные модификации фосфора Фосфор Белый фосфор Красныйфосфор Черный фосфор

Белый фосфор Наиболее распространен белый, или желтый, фосфор. Белый фосфор имеет молекулярную решетку, в узлах которой находятся тетраэдрические молекулы Р4. Это очень реакционноспособное, мягкое воскообразное вещество бледно-желтого цвета, с неприятным чесночным запахом, растворимое в сероуглероде и бензоле, нерастворимое в воде. Очень ядовит. Воспламеняется при трении, обладает уникальной способностью светиться в темноте за счет медленного окисления.Температура плавления – 44оС. В лаборатории его хранят под слоем воды. Смертельная доза– 0,1 г.При нагревании без доступа воздуха до 250-300 градусов белый фосфор превращается в красный.

Аморфный темно-малиновый порошок без запаха. Менее активен, чем белый фосфор, нерастворим в воде и сероуглероде, не светится в темноте и не самовоспламеняется, абсолютно безвреден. Температура возгорания – 260оС.Большое число атомов фосфора связано друг с другом в цепи , кольца …

Черный фосфор Имеет атомную кристаллическую решетку. По внешним признакам черный фосфор напоминает графит, имеет металлический блеск, обладает электропроводностью и теплопроводностью, довольно твердый.Наименее активный из всех модификаций. Ромбическая модификация

«Да! Это была собака, огромная, черная как смоль… Из ее отверстой пасти вырывалось пламя, глаза метали искры, по морде и загривку переливался мерцающий огонь.»

3)ИСТОРИЯ ОТКРЫТИЯ ФОСФОРА Свое название фосфор получил за способность светиться в темноте (греч. фосфор означает «светоносный»).В поисках философского камня , якобы способного превратить неблагородные металлы в золото ,гамбургский алхимик Г.Бранд в 1669г.при перегонке сухого остатка от выпаривании мочи впервые получил белый фосфор .Светоносный элемент принес Бранду немало денег (он показывал белый фосфор богатым людям за вознаграждение ).Позже Бранд продает секреты своего открытия дрезденскому алхимику Крафту .Изготовив достаточное количество фосфора, Крафт отправился в длительный вояж по Европе , где с большим успехом демонстрировал его свойства знатным особам , извлекая немалую выгоду .

Вскоре Ю. Ган и К.В. Шееле доказали, что в костях содержится много фосфора. В начале 70-х гг. XVIII в. великий французский ученый А. Лавуазье, сжигая фосфор в замкнутом объеме воздуха, доказал, что фосфор – самостоятельный химический элемент. В 1847 г. немецкий химик Шретер получил красный фосфор. В 1934 г. американский ученый Бриджмен выделил черный фосфор. Впоследствии были выделены фиолетовый и коричневый фосфор.

4)ПОЛУЧЕНИЕ ФОСФОРА;Свободный фосфор получают в электрических печах без доступа воздуха из фосфата кальция ,смешивая его с песком и углем: Ca3(PO4)2 + C + SiO2 → CaSiO3 + P + COРасставьте коэффициенты методом электронного баланса.

5)ХИМИЧЕСКИЕ СВОЙСТВА ФОСФОРА А) Взаимодействие с кислородом:Р + О2 →Б) Взаимодействие с бертолетовой солью:Р + KClO3 → P2O5 + KClВ) Взаимодействие с активными металлами:Mg + P →Допишите уравнения реакций. Какую роль выполняет фосфор в этих реакциях? Составьте электронный баланс к данным реакциям.

6)НАХОЖДЕНИЕ В ПРИРОДЕ Фосфор встречается в природе только в связанном состоянии. Массовая доля фосфора в земной коре – около 0,12%. Важнейшие минералы:Сa3(PO4)2 – фосфорит;3Сa3(PO4)2∙Ca(OH)2 – гидроксиапатит;3Сa3(PO4)2∙CaF2 – фторапатит. По содержанию в организме человека фосфор относится к макроэлементам (w(Р) = 0,95%).Фосфор входит в состав костной, нервной и мозговой тканей, крови, молока.Фосфором богаты яйца, мясо, молоко, хлеб.

Более половины объема мирового производства фосфора перерабатывается в соединения, используемые в синтетических моющих средствах.Соединения фосфора используют для получения антикоррозионных добавок к маслам и горючему для автомобилей.Сульфиды фосфора стали необходимы в сражении с ржавчиной в металлургии.Фосфор используется при производстве спичек.Из фосфора получают фосфорную кислоту, которая идет на производство удобрений .

Я светоносный элемент.Я спичку вам зажгу в момент.Сожгут меня – и под водойЯ сразу стану кислотой.Запишите уравнения реакций, о ко-торых идет речь в этом стихотворе-нии.
Что мы узнали о фосфоре?

Домашнее задание § 21, повторить § 15 и 16.Упр. 2-4, стр. 70, задания в тетради.