Презентация на тему: Фенолы

Фенолы

План урока Фенолы Классификация фенолов Номенклатура Строение молекулы Физические свойства фенола Химические свойства фенола Получение фенолов Применение фенола Генетическая связь
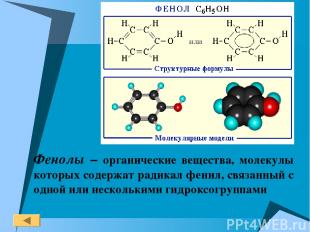
Фенолы – органические вещества, молекулы которых содержат радикал фенил, связанный с одной или несколькими гидроксогруппами
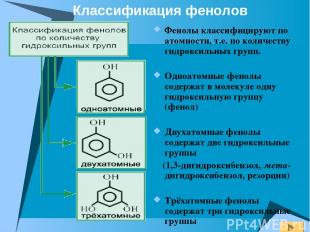
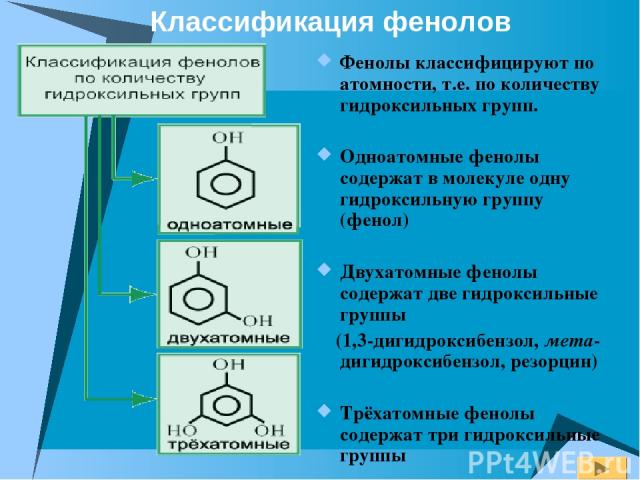
Фенолы классифицируют по атомности, т.е. по количеству гидроксильных групп. Одноатомные фенолы содержат в молекуле одну гидроксильную группу (фенол) Двухатомные фенолы содержат две гидроксильные группы (1,3-дигидроксибензол, мета-дигидроксибензол, резорцин) Трёхатомные фенолы содержат три гидроксильные группы Классификация фенолов
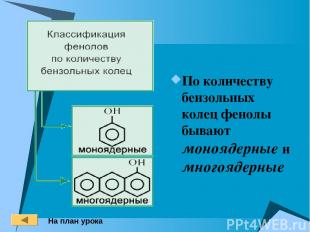
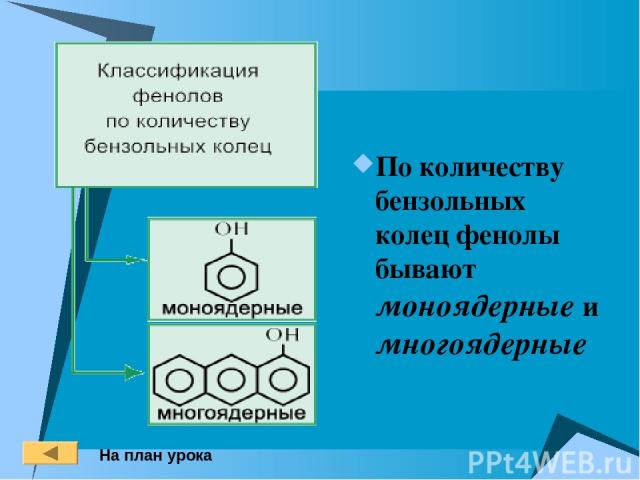
По количеству бензольных колец фенолы бывают моноядерные и многоядерные На план урока
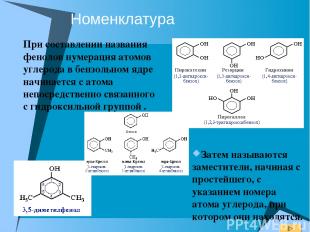
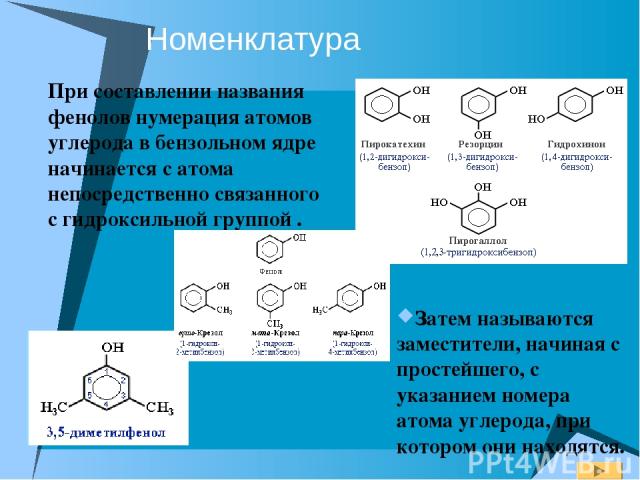
Номенклатура При составлении названия фенолов нумерация атомов углерода в бензольном ядре начинается с атома непосредственно связанного с гидроксильной группой . Затем называются заместители, начиная с простейшего, с указанием номера атома углерода, при котором они находятся.
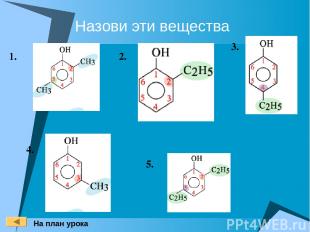
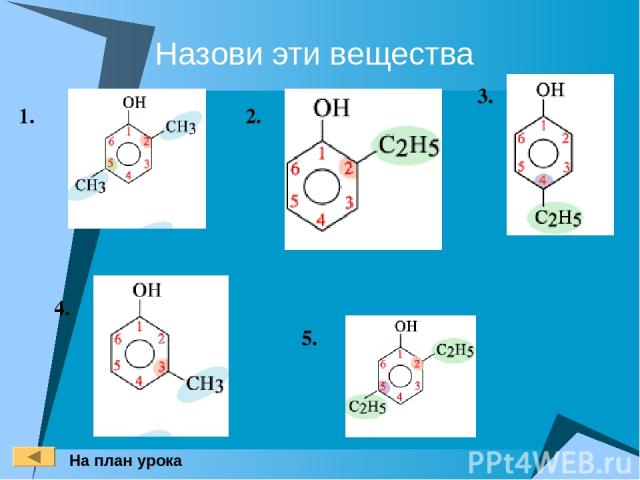
Назови эти вещества 1. 2. 3. 4. 5. На план урока

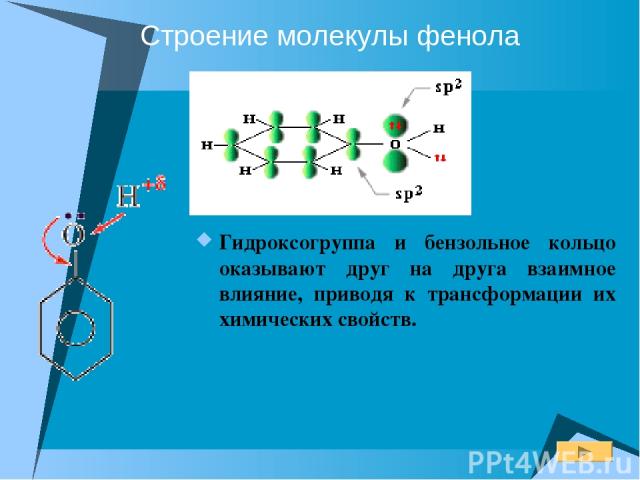
Строение молекулы фенола Гидроксогруппа и бензольное кольцо оказывают друг на друга взаимное влияние, приводя к трансформации их химических свойств.
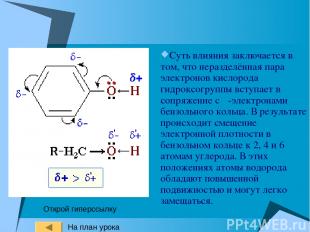
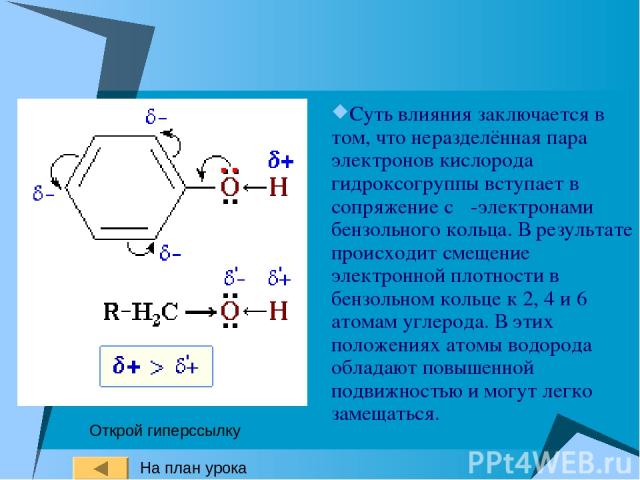
Суть влияния заключается в том, что неразделённая пара электронов кислорода гидроксогруппы вступает в сопряжение с π-электронами бензольного кольца. В результате происходит смещение электронной плотности в бензольном кольце к 2, 4 и 6 атомам углерода. В этих положениях атомы водорода обладают повышенной подвижностью и могут легко замещаться. Открой гиперссылку На план урока

Физические свойства фенола Фенол - твёрдое бесцветное кристаллическое вещество. Вследствие частичного окисления на воздухе он бывает окрашен в розовый цвет. Его температура плавления +42ºС, температура кипения +181ºС. Фенол обладает резким характерным запахом. В холодной воде он мало растворим, но уже при 70 ºС растворяется в любых отношениях. Фенол ядовит! При попадании на кожу вызывает ожоги поэтому с фенолом необходимо обращаться осторожно!

на план урока

Химические свойства фенола Химические свойства фенола обусловлены наличием в его молекуле гидроксильной группы бензольного ядра

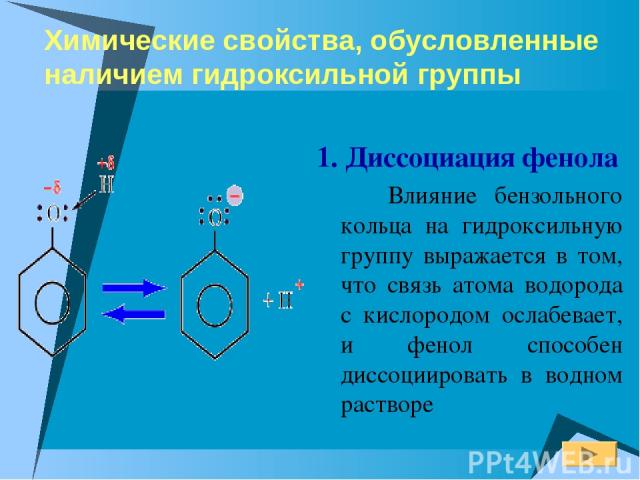
Химические свойства, обусловленные наличием гидроксильной группы 1. Диссоциация фенола Влияние бензольного кольца на гидроксильную группу выражается в том, что связь атома водорода с кислородом ослабевает, и фенол способен диссоциировать в водном растворе

2.Взаимодействие с натрием Фенол, как и спирты, взаимодействует с металлическим натрием с образованием соли (фенолята натрия) и водорода
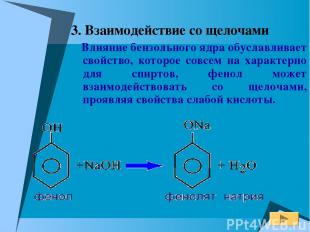
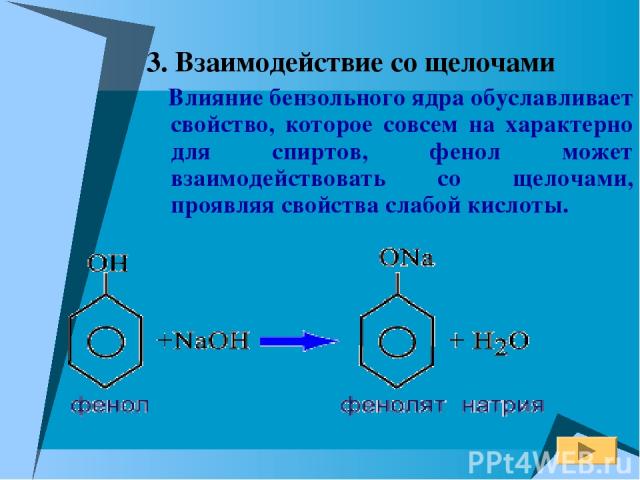
3. Взаимодействие со щелочами Влияние бензольного ядра обуславливает свойство, которое совсем на характерно для спиртов, фенол может взаимодействовать со щелочами, проявляя свойства слабой кислоты.


Карболовая кислота в 300 раз слабее угольной. Фенол – кислота довольно слабая, более сильные кислоты вытесняют фенол из фенолятов.

Химические свойства, обусловленные наличием бензольного ядра Отличия от ароматических углеводородов: 1. Реакции окисления Фенол окисляется кислородом воздуха, приобретая фиолетовую окраску.

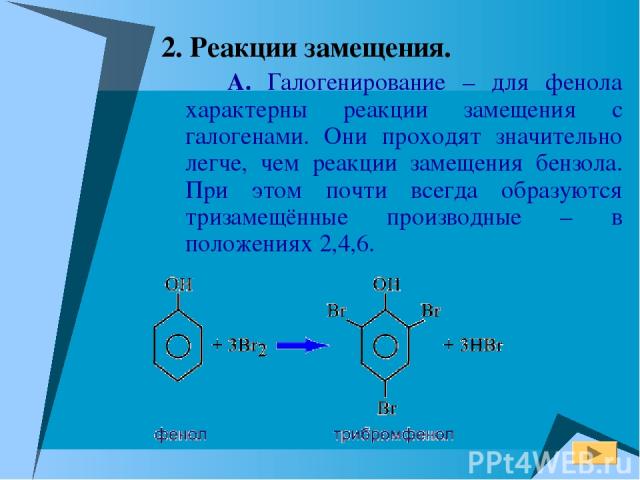
2. Реакции замещения. А. Галогенирование – для фенола характерны реакции замещения с галогенами. Они проходят значительно легче, чем реакции замещения бензола. При этом почти всегда образуются тризамещённые производные – в положениях 2,4,6.

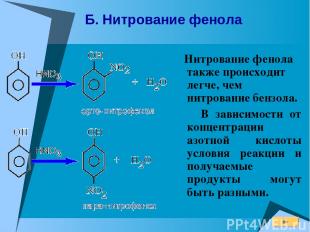
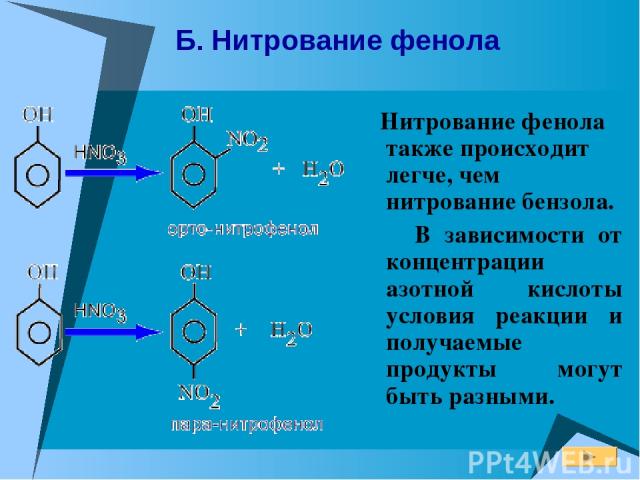
Б. Нитрование фенола Нитрование фенола также происходит легче, чем нитрование бензола. В зависимости от концентрации азотной кислоты условия реакции и получаемые продукты могут быть разными.

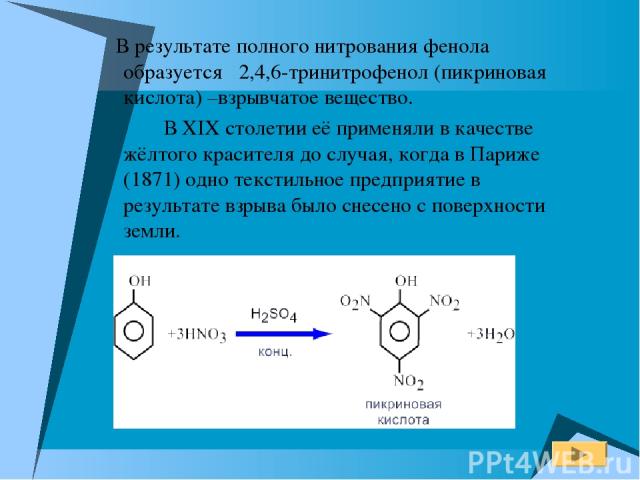
В результате полного нитрования фенола образуется 2,4,6-тринитрофенол (пикриновая кислота) –взрывчатое вещество. В XIX столетии её применяли в качестве жёлтого красителя до случая, когда в Париже (1871) одно текстильное предприятие в результате взрыва было снесено с поверхности земли.

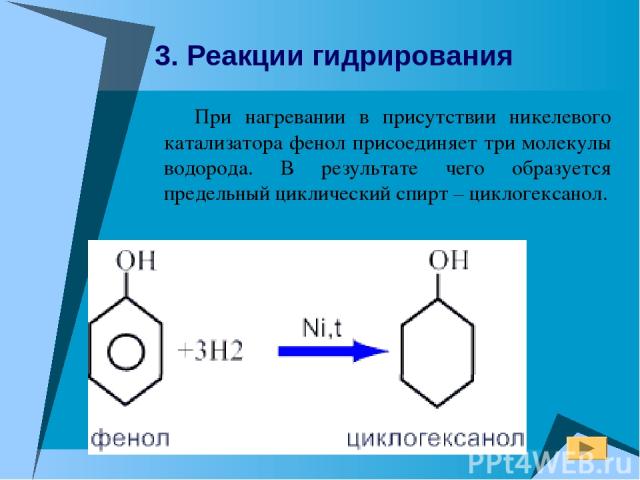
При нагревании в присутствии никелевого катализатора фенол присоединяет три молекулы водорода. В результате чего образуется предельный циклический спирт – циклогексанол. 3. Реакции гидрирования

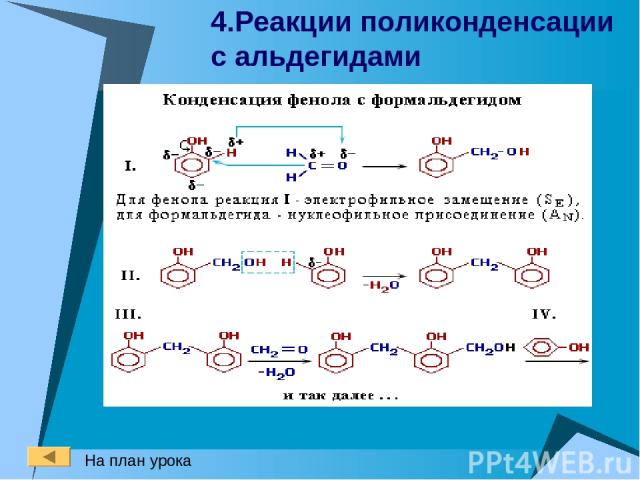
4.Реакции поликонденсации с альдегидами На план урока

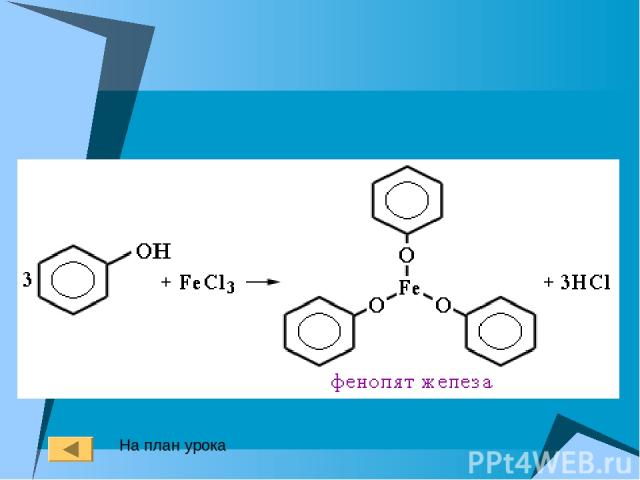
5. Качественная реакция на фенол
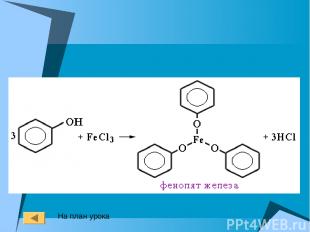
На план урока

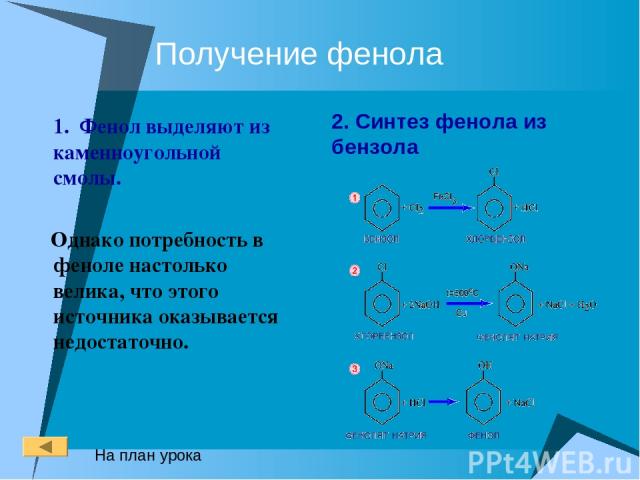
Получение фенола 1. Фенол выделяют из каменноугольной смолы. Однако потребность в феноле настолько велика, что этого источника оказывается недостаточно. 2. Синтез фенола из бензола На план урока

Применение фенола. Фенол применяют для производства фенолформальдегидных пластмасс, синтетического волокна капролактам, красителей, лекарств, взрывчатых веществ и других продуктов. Раствор фенола в воде обладает дезинфицирующими свойствами На план урока
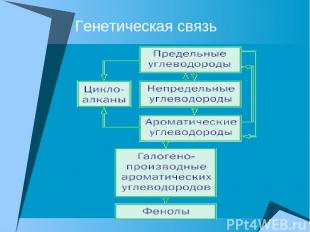
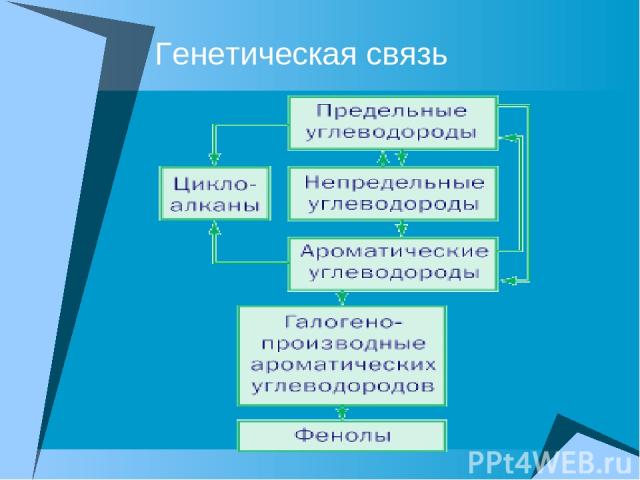
Генетическая связь